Оберіть свою мову
Оберіть свою мову
Ключові слова: первинний склерозуючий холангіт, автоімунний склерозуючий холангіт, лікування, біохімічна відповідь, індекс SCOPE, еластографія зсувної хвилі
Key words: primary sclerosing cholangitis, autoimmune sclerosing cholangitis, treatment, biochemical response, SCOPE index, shear wave elastography
Реферат
Первинний склерозуючий холангіт та аутоімунний склерозуючий холангіт у дітей – це рідкісні хронічні захворювання печінки, що супроводжуються прогресуючим ураженням жовчних проток, розвитком фіброзу та ризиком формування біліарного цирозу. Автоімунний склерозуючий холангіт розглядається як окремий фенотип первинного склерозуючого холангіту дитячого віку, який поєднує риси автоімунного гепатиту та склерозуючого холангіту. Попри схожість патогенетичних механізмів, ці захворювання відрізняються клінічним перебігом, терапевтичною відповіддю та прогнозом. Ефективність лікування цих захворювань залишається недостатньо високою, що пов’язано з прогресуванням фіброзу жовчних проток навіть на тлі терапії. Відсутність біохімічної відповіді в перші 6-12 місяців уважається несприятливим прогностичним фактором і має розглядатися як підстава для ескалації терапії або переходу на альтернативні методи лікування. Оцінювання ефективності терапії є важливою умовою вчасного ухвалення рішень щодо зміни тактики лікування. Метою дослідження було оцінити ефективність лікування первинного склерозуючого холангіту та автоімунного склерозуючого холангіту в дітей протягом 12 місяців на основі динаміки біохімічної відповіді, показників жорсткості печінки за даними еластографії та прогностичного індексу SCOPE. У дослідження включено 56 дітей віком 2-18 років, які проходили обстеження та лікування у 2016-2024 роках у відділенні дитячої гепатології: Серед них 38 – з автоімунним склерозуючим холангітом, 18 – з первинним склерозуючим холангітом. Пацієнти першої групи отримували комбіновану імуносупресивну терапію, другої – урсодезоксихолеву кислоту. Через 12 місяців повна біохімічна відповідь досягнута в 47% та 67% дітей відповідно (р=0,27), нормалізація гамма-глутамілтрансферази – у 63% та 83% (р=0,21). Індекс прогнозу достовірно знизився в обох групах, а зменшення жорсткості печінки було статистично значущим лише в дітей з автоімунним склерозуючим холангітом (р=0,002). Отримані результати свідчать про часткову ефективність терапії та підкреслюють важливість комплексного моніторингу результатів лікування для своєчасного перегляду терапевтичної стратегії.
Abstract
Evaluation of the effectiveness of treatment of primary sclerosing cholangitis and autoimmune sclerosing cholangitis in children and adolescents. Dyba M.B., Berezenko V.S., Mykhailiuk H.Z., Tkalyk O.M. Primary sclerosing cholangitis and autoimmune sclerosing cholangitis in children are rare chronic liver diseases characterized by progressive bile duct damage, fibrogenesis, and a risk of developing biliary cirrhosis. Autoimmune sclerosing cholangitis is considered a distinct pediatric phenotype of primary sclerosing cholangitis, combining clinical and morphological features of both autoimmune hepatitis and sclerosing cholangitis. Despite similar immunopathogenetic mechanisms, these diseases differ significantly in clinical course, therapeutic response, and long-term prognosis. The overall effectiveness of treatment remains suboptimal, which may be related to the ongoing progression of bile duct fibrosis even under therapy. Lack of biochemical response within the first 6-12 months is considered an unfavorable prognostic factor and should be regarded as an indication for treatment escalation or transition to alternative therapeutic strategies. Evaluation of treatment efficacy is essential for timely decision-making regarding therapeutic adjustments. The aim of this study was to evaluate the effectiveness of treatment in children with primary sclerosing cholangitis and autoimmune sclerosing cholangitis over a 12-month period based on the dynamics of biochemical response, liver stiffness measurements assessed by elastography, and the SCOPE prognostic index. A total of 56 children aged 2 to 18 years, who underwent evaluation and treatment between 2016 and 2024 at a pediatric hepatology department, were included in the study: 38 with autoimmune sclerosing cholangitis and 18 with primary sclerosing cholangitis. Patients in the first group received combined immunosuppressive therapy, while those in the second group were treated with ursodeoxycholic acid. After 12 months of treatment, complete biochemical response was achieved in 47% and 67% of children, respectively (p=0.27), and normalization of gamma-glutamyltransferase in 63% and 83% (p=0.21). The prognostic index significantly decreased in both groups, while liver stiffness reduction was statistically significant only in children with autoimmune sclerosing cholangitis (p=0.002). These findings indicate partial treatment effectiveness and highlight the importance of comprehensive monitoring to support timely modification of therapeutic strategies.
Первинний склерозуючий холангіт (ПСХ) – хронічне прогресуюче захворювання гепатобіліарної системи невідомої етіології, яке характеризується запаленням та перидуктулярним фіброзом внутрішньопечінкових та/або позапечінкових жовчних проток, що призводить до їх звуження, облітерації та розвитку вторинного біліарного цирозу. ПСХ є рідкісним захворюванням у дітей, його поширеність варіюється від 0,2 до 1,5 випадку на 100 000 дитячого населення [1, 2]. Зазвичай це захворювання асоціюється із запальними захворюваннями кишківника (ЗЗК) та характеризується різноманіттям клінічної симптоматики. Для первинного склерозуючого холангіту (ПСХ) у дітей характерна фенотипова варіабельність, що включає ураження як великих, так і дрібних жовчних проток, а також особливий варіант перебігу – автоімунний склерозуючий холангіт (АСХ), який поєднує ознаки ПСХ та автоімунного гепатиту (АІГ) і є притаманним саме дитячому віку. У сучасній термінології для позначення цього клінічного фенотипу також використовують термін "overlap-синдром АІГ/ПСХ", що вказує на наявність одночасних ознак обох захворювань – автоімунного гепатиту та первинного склерозуючого холангіту [1, 3, 4, 5]. За даними епідеміологічних досліджень, поширеність АСХ становить 0,1-0,6 випадку на 100 000 дітей у США та Канаді. За даними літератури, майже 50% дітей з АІГ мають ознаки АСХ [4, 6]. Існує точка зору, що АСХ є ранньою «запальною» фазою ПСХ, яка з часом може трансформуватися в класичний фенотип ПСХ у старшому віці [5]. Прогноз для пацієнтів з АСХ є гіршим, ніж з АІГ, оскільки стандартна імуносупресивна терапія не завжди забезпечує повну ремісію. Однак, завдяки менш вираженому ураженню жовчних проток та за умови своєчасної діагностики й лікування, він більш сприятливий, ніж у хворих з ПСХ. АСХ частіше зустрічається в дітей і має зв’язок з HLA-алелями, подібними до АІГ [2, 5, 7, 8, 9].
На сьогодні не існує єдиних стандартів лікування ПСХ та АСХ у дітей, що пов’язано з варіабельністю клінічного перебігу, фенотиповою гетерогенністю та труднощами діагностики. Дані літератури свідчать про обмеженість сучасних терапевтичних підходів. Незважаючи на те, що окремі препарати покращують показники печінкових проб у хворих з ПСХ, все ще не вирішеним є питання уповільнення в них темпів фіброгенезу, підвищення довгострокової виживаності без трансплантації та покращення якості життя [10, 11, 12, 13].
Урсодезоксихолева кислота (УДХК) є одним з найбільш вивчених препаратів, який застосовується в лікуванні ПСХ, однак її ефективність у педіатричних пацієнтів залишається дискусійною [2, 3, 14, 15]. Дослідження показують, що низькі та помірні дози УДХК (10-15 мг/кг/добу) можуть покращувати біохімічні показники, зокрема рівні лужної фосфатази та ГГТ, проте немає переконливих доказів її впливу на уповільнення фіброзу чи зниження ризику трансплантації. Деякі ретроспективні дослідження свідчать про стабілізацію клінічного стану при тривалому прийомі УДХК, однак без суттєвого впливу на кінцеві клінічні результати, такі як потреба в трансплантації печінки [1, 3, 10].
Світові дослідження підкреслюють необхідність проведення подальших проспективних рандомізованих досліджень для розроблення ефективніших методів лікування та покращення прогнозу в дітей із ПСХ. Нещодавно проведені дослідження вказують на потенційну ефективність ванкоміцину, який модулює кишкову мікробіоту, важливу в патогенезі ПСХ. У пацієнтів, рефрактерних до терапії УДХК, ванкоміцин сприяв зниженню рівня ГГТ. Проте його довгострокова ефективність ще потребує подальшого дослідження [16].
У лікуванні дітей з АСХ ключовою є комбінована імуносупресивна терапія – глюкокортикостероїди та азатіоприн. Хоча така терапія забезпечує біохімічну відповідь у пацієнтів, її вплив на фіброз жовчних проток є обмеженим, що породжує дискусії щодо доцільної тривалості її застосування.
Прогноз ПСХ у дітей залишається несприятливим через обмежену ефективність терапії, високий ризик розвитку цирозу печінки та холангіокарциноми. Основною метою лікування є досягнення біохімічної ремісії та сповільнення прогресування фіброзу. Відсутність біохімічного покращення в перші 6-12 місяців є негативним прогностичним фактором, однак чіткі рекомендації щодо ескалації терапії або переходу на альтернативні методи лікування досі не визначені. Тому актуальним завданням є стандартизація біохімічних та інших неінвазивних маркерів для оцінювання ефективності терапії та прогнозування її результатів.
Аналіз сучасної літератури підтверджує відсутність єдиних критеріїв оцінювання ефективності лікування ПСХ у дітей. Використання лише біохімічних показників, таких як ГГТ і ЛФ, не завжди корелює з гістологічними змінами чи клінічними ускладненнями. Тому сьогодні зусилля вчених спрямовані на створення комплексної системи оцінювання, яка включатиме візуалізаційні методи (МРХПГ), біомаркери запалення та фіброзу, а також показники якості життя.
Оцінювання ефективності лікування АСХ базується на міжнародних рекомендаціях, подібних до тих, що використовуються для АІГ [17]. Воно передбачає визначення повної біохімічної відповіді – нормалізацію рівнів АЛТ, АСТ та IgG протягом шести місяців після початку терапії, а також аналіз часткової чи відсутньої відповіді. Для ПСХ ключовим маркером ефективності лікування в дітей є рівень ГГТ: його зниження на ≥75% через 6-12 місяців лікування вказує на позитивну динаміку, тоді як недостатнє зниження свідчить про рефрактерність до терапії [16, 18].
Сучасні рекомендації пропонують використовувати індекс SCOPE (Simple Clinical Outcome Prediction Index for Primary Sclerosing Cholangitis) для оцінювання ефективності лікування та прогнозу ПСХ у дітей. Він враховує рівень білірубіну, альбуміну, тромбоцитів, ГГТ та результати МРХПГ, що дозволяє прогнозувати ризик ускладнень, потребу в трансплантації печінки та ймовірність несприятливого перебігу протягом 5 років. Використання цього інструмента допомагає персоналізувати лікування, своєчасно виявляти пацієнтів з високим ризиком прогресування та коригувати терапевтичну стратегію.
Підсумовуючи сучасні дані щодо лікування ПСХ та АСХ у дітей, стає очевидним, що оцінювання ефективності терапії є ключовим завданням для своєчасного коригування лікування та покращення прогнозу в дітей з цими захворюваннями. Зважаючи на вищезазначене, у цьому дослідженні проведено оцінювання ефективності лікування первинного склерозуючого холангіту та автоімунного склерозуючого холангіту в дітей протягом 12 місяців на основі динаміки біохімічної відповіді, показників жорсткості печінки за даними еластографії та прогностичного індексу SCOPE.
МАТЕРІАЛИ ТА МЕТОДИ ДОСЛІДЖЕНЬ
У ретроспективний аналіз було включено 83 дитини (віком 2-18 років) з ПСХ (n=31) та АСХ (n=52), які перебували на лікуванні у відділенні дитячої гепатології ДУ «Всеукраїнський центр материнства та дитинства Національної академії медичних наук України» в період з 2016 до 2024 р. До групи АСХ були включені також пацієнти, яким у попередні роки виставлявся діагноз overlap-синдрому (АІГ/ПСХ), відповідно до клінічних, біохімічних та морфологічних ознак поєднаного перебігу захворювання. Дослідження відповідало Гельсінській декларації, було схвалене етичним комітетом ДУ «ВЦМД НАМН України», а батьки надали письмову інформовану згоду. Згідно з критеріями включення та виключення, до дослідження увійшли 56 пацієнтів, розподілених на дві групи залежно від діагнозу: автоімунний склерозуючий холангіт (АСХ, n=38) та первинний склерозуючий холангіт (ПСХ, n=18).
Діагностика проводилася за сучасними рекомендаціями та включала клінічні, біохімічні, імунологічні, інструментальні й гістологічні дослідження. ПСХ діагностували за характерним холестатичним клінічним та біохімічним профілем (свербіж, підвищення γ-глутамілтрансферази), змінами на холангіограмах (мультифокальні стриктури, сегментарне розширення жовчних проток) та гістологічними ознаками (перидуктальний фіброз, фіброзно-облітеруючий холангіт) [20]. АСХ встановлювали за критеріями АІГ (підвищення IgG, позитивні автоантитіла, гістологічні зміни, зокрема інтерфейс-гепатиту, розеткоутворення, емперіполезу, портальної інфільтрації з переважанням лімфоцитів і плазматичних клітин) [21] у поєднанні з типовими для ПСХ змінами, встановленими за даними магнітно-резонансної холангіопанкреатографії (МРХПГ) та/або морфологічного дослідження печінки. Діагноз АСХ визначався за шкалою ESPGHAN: ≥8 балів – підтверджений АСХ, 7 балів – ймовірний АСХ [3]. Вірусні гепатити та спадкові метаболічні захворювання печінки було виключено на підставі результатів відповідних лабораторних та інструментальних обстежень.
У ретроспективному аналізі враховано дані рутинних лабораторних та інструментальних обстежень. Лабораторні показники включали загальний аналіз крові, коагулограму (міжнародне нормалізоване відношення – МНВ), біохімічний аналіз – рівні аспартатамінотрансферази (АСТ), аланінамінотрансферази (АЛТ), γ-глутамілтрансферази (ГГТ, гамма-глутамілтрансферази), лужної фосфатази (ЛФ), загального білірубіну, загального білка, альбуміну та γ-глобулінів, а також імунологічні маркери: рівень імуноглобуліну G (IgG) та автоантитіла – антинуклеарні антитіла (ANA), антитіла до гладеньких м’язів (SMA), антитіла до печінково-ниркового мікросому 1 типу (LKM-1), цитоплазматичні антинейтрофільні антитіла з перинуклеарним типом флуоресценції (pANCA), антитіла до печінково-цитозольного антигену типу 1 (LC1). Для оцінювання прогнозу в пацієнтів з ПСХ та АСХ використовували індекс SCOPE (Sclerosing Cholangitis Outcomes in Pediatrics), який дозволяє стратифікувати ризик прогресування захворювання на основі лабораторних параметрів, що включають рівні загального білірубіну, альбуміну, тромбоцитів, ГГТ та дані холангіографії на початку терапії та через 12 місяців (19) . Інструментальні дослідження включали ультразвукове дослідження (УЗД) для оцінювання структурних змін печінки, стану внутрішньо- та позапечінкових жовчних шляхів, а також виявлення ознак портальної гіпертензії. Ступінь фіброзу визначали методом еластографії за рекомендаціями EFSUMB [22]. Еластографію печінки у 2015-2019 рр. проводили на сканері «Радмир ULTIMA», а з 2019 року — на системі Aplio i800 (Canon Medical Systems) з використанням 2D-SWE. Магнітно-резонансну холангіопанкреатографію для візуалізації жовчних проток виконано в 62 пацієнтів (29 з ПСХ, 36 з АСХ). Біопсію печінки проведено в 38 пацієнтів з АСХ та 18 з ПСХ. Ілеоколоноскопія виконана у всіх пацієнтів з ПСХ та АСХ. Езофагогастродуоденоскопію проводили пацієнтам із цирозом печінки та/або тромбоцитопенією (≤150 тис./мкл) з метою діагностики варикозного розширення вен стравоходу (ВРВС). Використані методи забезпечили комплексну оцінку стану печінки, жовчних шляхів та ускладнень захворювання.
Критерії включення:
- Вік пацієнтів 2-18 років.
- Підтверджений діагноз ПСХ або АСХ на основі гістологічних, лабораторних чи інструментальних досліджень.
- Спостереження ≥ 12 місяців.
- Наявність лабораторних, морфологічних та інструментальних даних до початку лікування, на 6-му та 12-му місяцях терапії.
Критерії виключення:
- Вірусні гепатити B і C.
- Спадкові захворювання печінки.
- Спостереження <12 місяців або відсутність необхідних лабораторних даних для оцінювання ефективності лікування.
Для оцінювання ефективності лікування використовували рекомендації міжнародної групи з автоімунного гепатиту (AIH) [11]:
- Повна біохімічна відповідь: нормалізація трансаміназ (АЛТ, АСТ) та рівня IgG до верхньої межі норми (ВМН) протягом 6 та 12 місяців після початку терапії.
- Недостатня відповідь: відсутність повної біохімічної відповіді через 6 місяців лікування.
- Непереносимість лікування: реєструвалася при виникненні побічних ефектів, які призводили до припинення застосування препаратів.
А також оцінювали ефективність лікування за рівнем ГГТ в сироватці крові [16, 18]:
- Відповідь на лікування: зниження ГГТ ≥75% від початкового рівня через 6-12 місяців лікування.
- Відсутність відповіді: зниження ГГТ <75% від початкового рівня.
Усі пацієнти з АСХ та ПСХ отримували УДХК у дозі 10-20 мг/кг/добу. Системну імуносупресивну терапію преднізолоном отримували 81,6% (n=31) дітей з АСХ та 11,1% (n=2) дітей з ПСХ. Азатіоприн у комбінації з преднізолоном або як монотерапію отримували 76,3% пацієнтів з АСХ (n=29) та 18,2% (n=4) пацієнтів з ПСХ. Препарати 5-аміносаліцилової кислоти (5-АСА) застосовували у 68,4% (n=23) дітей з АСХ і 72,2% (n=13) з ПСХ. Мікофенолату мофетил отримували 10,5% (n=4) дітей з АСХ, циклоспорин –2,63% (n=1), які призначали в разі непереносимості або недостатньої ефективності азатіоприну. Антибактеріальну терапію (ципрофлоксацин, ванкоміцин або рифаксимін) отримували 34,2% (n=13) пацієнтів з АСХ та 27,8% (n=5) з ПСХ через недостатню ефективність базисного лікування.
Статистичні методи дослідження проведено з використанням програми GraphPad Prism 10 (GraphPad Software Inc., США, GraphPad Prism 10.4.1.627, серійний номер GPS-2722055-T). Перевірку нормальності розподілу проводили за критерієм Колмогорова-Смирнова. Безперервні змінні подано як середнє ± стандартне відхилення (SD) або медіану (Me) з міжквартильним інтервалом [Q25; Q75] залежно від характеру розподілу. Для порівняння середніх значень між групами використовували t-критерій Стьюдента або U-критерій Манна-Вітні. Для аналізу динамічних змін у залежних вибірках застосовували повторний дисперсійний аналіз (Repeated Measures ANOVA) або тест Фрідмана залежно від характеру розподілу. Частотні показники порівнювали за допомогою точного тесту Фішера. Статистично вірогідними вважали результати при значенні p<0,05 [23].
Робота є фрагментом науково-дослідних робіт:
- 2016-2018 рр. «Дослідження ролі вітамін D залежних механізмів розвитку адаптаційних можливостей організму в критичні періоди дитинства та патогенезі хронічної соматичної патології у дітей», № державної реєстрації: 01.16U001202. Дизайн дослідження узгоджено на засіданні комісії з питань біоетики ДУ «ІПАГ НАМН України» (протокол № 3 від 23.06.2015);
- 2019-2021 рр. «Дослідження ролі вітамін D залежних механізмів розвитку адаптаційних можливостей організму в критичні періоди дитинства та патогенезі хронічної соматичної патології у дітей», № державної реєстрації: 01.16U001202. Дизайн дослідження узгоджено на засіданні комісії з питань біоетики ДУ «ІПАГ НАМН України» (протокол № 4 від 15.05.2018);
- 2022-2023 рр. «Оптимізувати методи профілактики і корекції недостатності та дефіциту вітаміну D у здорових дітей з груп ризику та при ревматичних хворобах і хронічних гепатитах», № державної реєстрації: 01.16U001202. Дизайн дослідження узгоджено на засіданні комісії з питань біоетики ДУ «ІПАГ НАМН України» (протокол № 4 від 13.04.21).
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
Вік пацієнтів у досліджуваних групах суттєво не відрізнявся: у групі АСХ – 11,1 ± 4,1 року, у групі ПСХ – 10,7 ± 3,8 року (р>0,05), таблиця 1. У групі АСХ частка дівчат становила 47%, що було вищим порівняно з групою ПСХ (28%), (p=0,24). Ураження великих жовчних проток діагностовано в 15 (83,3%) дітей з ПСХ та у 23 (70%) з АСХ, без суттєвої відмінності між групами, р>0,05.
Параметри АСХ, n=38 ПСХ, n=18 Вік, роки (Mean ± SD) 11,1 ±4,1 10,7±3,8 Дівчатка , n (%) 18 (47) 5 (28) Тромбоцити, Me [Q25; Q75] 245 (169; 411) 306 (238; 385) АЛТ, Me [Q25; Q75] 383 (241; 768,5) 214 (89; 466) АСТ, Me [Q25; Q75] 320 (200; 741) 146(63; 435)* ГГТ, Me [Q25; Q75] 167 (81,5; 300) 134 (61; 285) Білірубін, Me (Q25; Q75) 32 (15; 80) 14 (10; 20)* Загальний білок, г/л Me [Q25; Q75] 87 (81; 93) 77 (68;83)* Альбумін, г\л Me [Q25; Q75] 36 (32; 40) 43 (40; 45 )* МНВ, Me [Q25; Q75] 1,4 (1,2; 1,7) 1,2 (1,1; 1,3) IgG, г/л, Me [Q25; Q75] 22 (16; 29) 12 (9; 16)* γ-глобуліни % [Q25; Q75] 30 (27; 46) 18 (16; 28) Фіброз ≤ 2 ст., n (%) 13 (34) 9 (50) Фіброз ≥ 3 ст., n (%) 25 (66) 9 (50) Еластографія печінки, кПА [Q25; Q75] 11 (8; 15) 8 (6;11)* Цироз печінки, n (%) 11 (29) 4 (22) Портальна гіпертензія, n (%) 11 (29) 2 (21) ВРВС, n (%) 4 (10,5) 2 (11) Ураження великих жовчних проток 23 (60,5) 15 (83) ЗЗК 26 (68) 13 (72) Примітки: n – кількість дітей у групі; Ме – медіана; Q25 – перший квартиль; Q75 – третій квартиль; * – статистично значущі відмінності між групами за U-критерієм Манна-Вітні (p<0,05).
Аналіз лабораторних показників виявив характерні лабораторні зміни в кожній групі пацієнтів, що відображають різні механізми ураження печінки. У дітей з ПСХ рівні АСТ були значно нижчими, ніж у пацієнтів з АСХ (р=0,026 для АСТ), що свідчить про менш значне пошкодження гепатоцитів. Пацієнти з ПСХ також демонстрували нижчі рівні білірубіну порівняно з АСХ (р=0,02), що може бути пов’язано з ранньою стадією захворювання без типових ознак холестазу. Вищі рівні альбуміну в дітей з ПСХ порівняно з АСХ (р=0,01) разом з нижчими МНВ (р>0,05) свідчать про збережену синтетичну функцію печінки в дітей на початкових стадіях ПСХ. Рівень ГГТ в пацієнтів з ПСХ не мав суттєвої різниці з АСХ (р=0,49), що зумовлено схожістю механізмів ураження жовчних проток при ПСХ і АСХ. Імунологічний профіль пацієнтів з АСХ та ПСХ мав значні відмінності. Рівні IgG та γ-глобулінів були вірогідно вищими в пацієнтів з АСХ порівняно з ПСХ (p=0,006 і p=0,01 відповідно), що підтверджує наявність більш вираженого автоімунного компонента при АСХ. За даними біопсії, частка пацієнтів зі стадіями фіброзу ≤2 за Metavir була вищою в групі ПСХ (50%) порівняно з АСХ (34%), однак ця різниця не досягла статистичної значущості (p>0,05). Частота цирозу печінки також не відрізнялася між групами, становлячи 29% у пацієнтів з АСХ та 22% у хворих на ПСХ (p>0,05). За даними еластографії, показники жорсткості печінки були достовірно вищими в дітей з АСХ порівняно з ПСХ (p=0,01), що може бути зумовлено вищою активністю гепатиту в дітей з АСХ. Частота портальної гіпертензії становила 29% у групі АСХ та 21% у групі ПСХ, без статистично значущих відмінностей (p>0,05). Подібна тенденція спостерігалася щодо ВРВС, яке виявляли в 10,5% пацієнтів з АСХ та 11% з ПСХ (p>0,05).
Запальні захворювання кишківника часто спостерігалися в дітей з АСХ та ПСХ: у 68% при АСХ та в 72% при ПСХ, без статистично значущої різниці між групами (p>0,05). Ці дані вказують на можливі спільні механізми розвитку захворювань та підтверджують важливу роль ЗЗК як супутнього стану при холангіопатіях, що може впливати на підхід до діагностики та лікування.
Результати оцінювання відповіді на лікування наведено в таблиці 2.
Параметри 6-й місяць n (%) 12-й місяць n (%) Повна біохімічна відповідь через 6 та 12 місяців лікування АСХ (n=38) 12 (32) 18 (47) ПСХ (n=18) 7 (39) 12 (67) ГГТ відповідь (зниження ГГТ >75%) через 12 місяців лікування АСХ (n=38) - 25 (66) ПСХ (n=18) - 16 (89) ГГТ ≤50 Од/л на 12-му місяці лікування АСХ (n=38) - 24 (63) ПСХ (n=18) - 15 (83)
Повна біохімічна відповідь через 6 місяців лікування
Через 6 місяців лікування повна біохімічна відповідь спостерігалася в 32% пацієнтів з АСХ та 39% пацієнтів з ПСХ, без статистично значущої різниці між групами (p>0,05). Низький рівень біохімічної відповіді в дітей з АСХ може бути пов’язаний із супутнім ураженням жовчних проток, що ускладнює контроль запального процесу. Імуносупресивна терапія при АСХ переважно спрямована на зменшення запалення в гепатоцитах, тоді як її вплив на патологічні зміни в жовчних протоках залишається обмеженим. У пацієнтів з ПСХ, які отримують монотерапію урсодезоксихолевою кислотою, оцінка ефективності лікування через 6 місяців не є ключовим показником. Дані щодо ПСХ в цей часовий проміжок наведено виключно для порівняння з пацієнтами з АСХ.
Повна біохімічна відповідь через 12 місяців лікування
Через 12 місяців лікування повну біохімічну відповідь спостерігали лише в 47% пацієнтів з АСХ та 67% пацієнтів з ПСХ (р=0,25). Нижчий показник у пацієнтів з АСХ вказує на труднощі лікування, пов’язані із супутнім ураженням жовчних проток, тоді як у групі ПСХ результати є кращими, ймовірно, через відмінності в тяжкості запалення.
ГГТ є важливим маркером холестазу та ураження жовчних проток у дітей. Пацієнти з ПСХ демонструють кращу біохімічну відповідь за рівнем ГГТ порівняно з пацієнтами з АСХ. Вищий відсоток ГГТ-відповіді (89% проти 66%, p=0,1) свідчить про кращу ефективність терапії щодо зниження холестазу в пацієнтів з ПСХ. Нормалізація рівня ГГТ через 12 місяців лікування також частіше досягалася в дітей з ПСХ порівняно з АСХ (83% проти 63%, p=0,21). Це може вказувати на варіабельність індивідуальної відповіді на лікування та вплив додаткових факторів на ефективність терапії, зокрема ступеня ураження жовчних проток і фіброзу печінки. Також можливим фактором, що впливає на зниження ГГТ, є відмінності в дозуванні урсодезоксихолевої кислоти (УДХК) між групами. Дітям з ПСХ зазвичай призначали УДХК в дозі 15-20 мг/кг/добу, тоді як пацієнтам з АСХ – 10-15 мг/кг/добу, що могло вплинути на ступінь біохімічної відповіді. Враховуючи можливий вплив дозування на ефективність терапії, цей аспект потребує подальших досліджень.
Прогностичний індекс SCOPE оцінює тяжкість перебігу захворювання та прогноз у пацієнтів з АСХ та ПСХ. Порівняння показників на початку лікування та через 12 місяців демонструє значне покращення стану пацієнтів в обох групах, таблиця 3.
Показник 0 міс 12 міс Значення р SCOPE АСХ (n=38) Me [Q25; Q75] 0-3 бали, n (%) 4-5 балів, n (%) 6-11 балів, n (%) 4 [3; 6]* 15 (39) 12 (32) 11 (29) 2 [1; 3] 32 (84) 5 (13) 1 (3) p<0,0001 ПСХ (n=18) Me [Q25; Q75] 0-3 бали, n (%) 4-5 балів, n (%) 6-11 балів, n (%) 4 [2–5]* 6 (33) 10 (56) 2 (11) 2 [1–2] 15 (83) 2 (11) 1 (6) p=0,001 Примітки: n – кількість дітей у групі; Ме – медіана; Q25 – перший квартиль; Q75 – третій квартиль; *— статистично значущі відмінності між групами за критерієм Вілкоксона для парних вибірок (p<0,05).
У дітей з АСХ на початку лікування медіана індексу SCOPE становила 4 [3; 6]; 39% мали низький ризик (0-3 бали), 32% – середній (4-5 балів), 29% – високий (6-11 балів). Через 12 місяців терапії медіана знизилася до 2 [1; 3], при цьому 84% пацієнтів перебували в групі низького ризику, 13% – середнього, 3% – високого. Динаміка SCOPE за рік лікування в групі АСХ була статистично значущою (p<0,0001).
У дітей з ПСХ на початку лікування медіана індексу SCOPE становила 4 [2-5]; 33% мали низький ризик прогресування, 56% – середній і 11% – високий. Через 12 місяців медіана знизилася до 2 [1-2], при цьому 83% пацієнтів мали низький ризик, 11% – середній і 6% – високий. Динаміка SCOPE за рік лікування в групі ПСХ також була статистично значущою (p=0,001).
Значне зниження показників SCOPE в пацієнтів з АСХ та ПСХ свідчить про високу ефективність лікування. Зменшення частки пацієнтів із середнім і високим ризиком прогресування захворювання вказує на зниження ймовірності розвитку ускладнень і покращення клінічного прогнозу в обох групах.
Ми також проаналізували динаміку жорсткості печінки, оціненої за допомогою еластографії, як потенційного критерію ефективності терапії. Порівняння показників на початку лікування та через 12 місяців виявило значне зниження жорсткості печінки в групі АСХ (p=0,002), тоді як у групі ПСХ статистично значущих змін не зафіксовано (p=0,1) (табл. 4).
У пацієнтів з АСХ жорсткість печінки, визначена еластографією, відображає як фіброзні зміни, так і запальну інфільтрацію, тому зниження цього показника на тлі імуносупресивної терапії свідчить насамперед про зменшення активності запалення. Натомість у хворих на ПСХ жорсткість печінки переважно зумовлена фіброзом і внутрішньопечінковим холестазом, а внесок запального компонента є незначним. У цьому контексті монотерапія УДХК, ефективність якої щодо зменшення фіброзу й контролю холестазу залишається обмеженою за даними численних досліджень, не забезпечує істотної динаміки показників жорсткості печінки.
Показник 0 міс Me [Q25; Q75] 12 міс Me [Q25; Q75] Значення р Еластографія, кПа ПСХ (n=20) 8 [6;11] 7 [5;9] р=0,10 АСХ (n=38) 11 [8;15]* 8 [7;11] р=0,002 Примітка. * – статистично достовірна відмінність у групі в динаміці спостереження (p<0,05, тест Вілкоксона для парних вибірок).
Визначення повної біохімічної ремісії, як нормалізації рівнів амінотрансфераз та IgG, набуває дедалі більшого значення як клінічно досяжний та прогностично значущий сурогатний маркер гістологічної активності в пацієнтів з АІГ. Згідно з даними Hartl et al. (2022), лише 18% пацієнтів з АІГ, які перебували в стабільній біохімічній ремісії, мали залишкову гістологічну активність, і жоден не мав високої активності запалення. Натомість серед пацієнтів без біохімічної ремісії 70% мали персистуюче запалення. Ці результати підтверджують, що досягнення повної біохімічної відповіді може вважатися надійним критерієм контролю активності захворювання та ефективності імуносупресивної терапії при АІГ. Як зазначають автори цього дослідження, важливим аспектом є визначення не тільки рівня трансаміназ, але й IgG, оскільки серед пацієнтів з частковою біохімічною ремісією (нормальні рівні амінотрансфераз, але підвищений IgG) у 50% виявлено високу гістологічну активність, що додатково підкреслює прогностичну значущість одночасного контролю обох показників – АЛТ і IgG – саме в контексті автоімунного гепатиту. Дослідження Hartl et al. (2018) також продемонструвало, що повна біохімічна ремісія (нормалізація амінотрансфераз і IgG) є не лише маркером низької гістологічної активності, але й незалежним прогностичним фактором регресу фіброзу при АІГ. За умов стабільної біохімічної ремісії протягом 5,7 року жоден пацієнт не мав прогресування фіброзу, тоді як 43% хворих без ремісії продемонстрували прогресування фіброзу печінки [24].
У контексті ПСХ результати дослідження Deneau et al. (2018) демонструють, що зниження рівня ГГТ є важливим предиктором сприятливого прогнозу [18]. Так, у пацієнтів з рівнем ГГТ <50 Од/л через рік після встановлення діагнозу 5-річна виживаність без подій становила 91% порівняно з 67% при рівні ГГТ ≥50. Найкращі результати спостерігались у дітей, у яких протягом першого року рівень ГГТ знизився на ≥75% відносно вихідного значення (виживаність без подій – 88%), тоді як при зниженні на ≤25% вона становила лише 61%. Наведені дані підтверджують доцільність розгляду ГГТ як потенційного сурогатного маркера ефективності лікування ПСХ в дітей. Концепція так званого «ймовірного сурогатного маркера» (тобто такого, що з великою ймовірністю відображає вплив лікування на клінічно значущий результат) офіційно визнається Управлінням з контролю за продуктами і ліками США (FDA) як основа для прискореного затвердження ліків при повільно прогресуючих захворюваннях, таких як ПСХ, за наявності вагомих епідеміологічних підтверджень [25].
Результати нашого дослідження свідчать про складність досягнення повної біохімічної відповіді в дітей з АСХ навіть за умов комбінованої імуносупресивної терапії. Через 12 місяців лікування лише 47% дітей з АСХ досягли повної біохімічної ремісії, що узгоджується з результатами дослідження Giorgio A.D. et al., 2020 р, проведеному в King's College Hospital (Лондон, Великобританія), у якому 55% дітей з АСХ досягли ремісії [14]. Хоча імуносупресивна терапія залишається стандартом лікування АСХ, її ефективність щодо впливу на біліарний компонент захворювання є обмеженою [6], що підтверджується і нашими даними. Значна частка пацієнтів з АСХ не досягла нормалізації рівня ГГТ. Наші результати показали, що нормалізацію ГГТ вдалося досягти лише в 63% пацієнтів з АСХ, тоді як у групі ПСХ цей показник становив 83%. Подальші дослідження мають бути спрямовані на вивчення механізмів резистентності холангіопатій до імуносупресії, а також на пошук нових терапевтичних стратегій, які б дозволяли ефективно впливати на біліарні ураження при АСХ та ПСХ.
Особливістю нашого дослідження є включення одночасного оцінювання біохімічної відповіді, ГГТ-відповіді, індексу SCOPE, оцінювання жорсткості печінки як взаємодоповнювальних інструментів моніторингу ефективності лікування дітей з АСХ та ПСХ. Використання індексу SCOPE як прогностичного інструменту при ПСХ в дітей обґрунтовано численними дослідженнями. Хоча роль індексу SCOPE в щоденній клінічній практиці ще не визначена остаточно, його розглядають як корисне доповнення до загальної клінічної оцінки [19, 26, 27]. Оцінка індексу SCOPE у нашій когорті продемонструвала виражене зниження прогнозованого ризику в дітей з АСХ та ПСХ вже через 12 місяців лікування. У групі АСХ медіана індексу знизилась з 4 [3-6] до 2 [1-3] балів (p<0,0001), при цьому частка пацієнтів з високим ризиком (6-11 балів) зменшилась з 29% до 3%. Аналогічні тенденції спостерігались у групі ПСХ: зниження медіани з 4 [2-5] до 2 [1-2] балів (p=0,001), зменшення частки пацієнтів з високим ризиком з 11% до 6%. Зниження показника SCOPE на ранніх етапах лікування, зокрема через 12 місяців, може слугувати маркером покращення клінічного прогнозу, навіть якщо формально індекс був розроблений для довгострокової стратифікації. У дослідженні Hensel et al. (2021) було показано, що обчислення індексу SCOPE через 5 років після встановлення діагнозу дозволяє краще передбачити розвиток ускладнень, порівняно з розрахунком на момент діагностики для прогнозу трансплантації печінки або летального результату [28]. Зниження показника SCOPE вже протягом першого року може свідчити про позитивну динаміку захворювання та слугувати додатковим критерієм ефективності терапії в дітей з АСХ та ПСХ. Це особливо важливо в педіатричній практиці, де терапевтичні рішення часто потрібно ухвалювати з урахуванням активного росту, гормональних змін і ризику швидкого прогресування фіброзу.
Важливою особливістю нашого дослідження є застосування еластографії як додаткового неінвазивного маркера оцінювання відповіді на терапію в дітей з АСХ та ПСХ. Зниження жорсткості печінки за даними еластографії протягом першого року лікування було достовірним лише в пацієнтів з АСХ: медіана жорсткості печінки (кПА) зменшилася з 11 кПа [8; 15] до 8 кПа [7; 11] (p=0,002). Це може відображати зниження запалення в печінці, що підтверджується літературними даними про взаємозв’язок між активністю гепатиту та показниками жорсткості [22, 24, 29]. Натомість у дітей з ПСХ змін жорсткості печінки в динаміці не виявлено (8 кПа [6; 11] → 7 кПа [5; 9], p=0,10). Це узгоджується з відомими особливостями ПСХ, де переважають фібротичний та холестатичний компоненти ураження, а запальна активність є менш вираженою. Наразі нам не вдалося виявити досліджень, які б оцінювали динаміку показників еластографії в пацієнтів з ПСХ як маркер ефективності терапії. Натомість у пацієнтів з АСХ динаміка жорсткості печінки може виступати додатковим маркером ефективності терапії. Такий підхід узгоджується з результатами інших дослідників, які підтримують використання еластографії як чутливого інструменту моніторингу змін у печінковій тканині у відповідь на лікування автоімунних захворювань печінки [24, 30, 31].У цьому контексті доцільним є підкреслення ролі еластографії не лише як одноразового діагностичного інструменту, а й як засобу динамічного моніторингу ефективності лікування. Регулярне вимірювання жорсткості печінки дозволяє оцінювати зміну стану тканини без необхідності повторної біопсії, що особливо важливо в педіатричній практиці. Перспективним напрямом подальших досліджень є встановлення порогових значень змін жорсткості печінки, які б достовірно корелювали з регресом гістологічної стадії фіброзу. Визначення таких порогів дозволить підвищити клінічну цінність еластографії як неінвазивного сурогатного маркера гістологічного поліпшення активності та фіброзу печінки. Такий підхід відкриває можливість формування персоналізованих стратегій моніторингу, орієнтованих на довготривалий прогноз, зменшення необхідності інвазивних процедур та оптимізацію терапевтичного супроводу дітей з автоімунними захворюваннями печінки.
На сьогодні не розроблено ефективного методу лікування імунних холангіопатій, таких як АСХ та ПСХ, що підтверджується як результатами нашого дослідження, так і численними публікаціями інших авторів. Раніше повідомлялось, що застосування УДХК в дозах 13-15 мг/кг/добу може призводити до нормалізації рівнів печінкових ферментів, однак при цьому не виявлено позитивного впливу на довготривалий прогноз [32]. У нещодавньому ретроспективному дослідженні не було виявлено суттєвої різниці в клінічних наслідках між групами, які отримували УДХК, не отримували терапії або застосовували пероральний ванкоміцин [33]. Крім того, перебіг ПСХ в дітей характеризується природними коливаннями біохімічної активності, і спонтанна нормалізація печінкових ферментів не є рідкісною [27]. Однак згідно з дослідженням Deneau et al., 2018, нормальний рівень ГГТ через 1 рік досягнуто у 53% пацієнтів, які отримували УДХК, і лише у 29% тих, хто її не отримував [18]. У нашому дослідженні УДХК отримували всі пацієнти з АСХ і ПСХ, а 4% отримували ванкоміцин. Проте ретроспективний дизайн не дозволяє однозначно оцінити ефективність цієї терапії.
Обмеженням нашого дослідження є ретроспективний дизайн, невелика вибірка пацієнтів з ПСХ, а також різна тривалість перебування на терапії до моменту включення в дослідження. Проте перевагами є динамічне спостереження впродовж 12 місяців і використання декількох комплементарних критеріїв ефективності (біохімічні показники, еластографія, індекс SCOPE).
ВИСНОВКИ
1. Ефективність терапії в дітей з автоімунним склерозуючим холангітом та первинним склерозуючим холангітом залишається помірною: повну біохімічну відповідь та нормалізацію рівня γ-глутамілтрансферази через 12місяців лікування досягнуто лише в 47% і 63% пацієнтів з автоімунним склерозуючим холангітом та в 67% і 83% з первинним склерозуючим холангітом відповідно, що свідчить про необхідність удосконалення терапевтичних підходів.
2. Визначення жорсткості печінки за допомогою еластографії є чутливим маркером ефективності лікування в перші 12місяців терапії в дітей з автоімунним склерозуючим холангітом і може розглядатися як додатковий критерій ефективності імуносупресивної терапії.
3. Оцінювання біохімічної відповіді, рівня γ-глутамілтрансферази та розрахунок прогностичного індексу SCOPE (Sclerosing Cholangitis Outcomes in Pediatrics) є неінвазивними інструментами, які доцільно включати до системи моніторингу ефективності лікування та оцінювання прогнозу в дітей з автоімунним і первинним склерозуючим холангітом.
Внески авторів:
Диба М.Б. – концептуалізація, методологія, дослідження, аналіз, написання статті, редагування;
Березенко В.С. – рецензування та редагування;
Михайлюк Х.З., Ткалик О.М. – дослідження.
Фінансування. Дослідження не має зовнішніх джерел фінансування.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів.
REFERENCES
Ключові слова: променева терапія, медичні зображення, оптична щільність, поглинена доза, невизначеності
Key words: radiotherapy, medical images, optical density, absorbed dose, uncertainties
Реферат
Якість променевої терапії значно покращилася завдяки використанню нових джерел та видів опромінення, а також сучасного тривимірного планування. Проте рівень променевих пошкоджень залишається суттєвим, що зумовлює необхідність аналізу точності інструментів, які забезпечують формування зображень і розрахунок доз. Метою роботи було визначення ймовірних невизначеностей, що виникають при використанні програмного забезпечення рентген-комп’ютерного томографа «TOSHIBA Asteion Super 4» та планувальних систем прискорювача електронів «Elekta Synergy» (Elekta Limited), а також пошук шляхів зменшення цих невизначеностей. Було проаналізовано 28 планів променевої терапії хворих, яка проводилася на прискорювачі електронів «Elekta Synergy» за останні чотири роки. Для оцінювання параметрів зображення аналізували дані рентген-комп’ютерної томографії з товщиною реконструкції 1,5 мм, оброблені програмою «eFilm». Визначали розмір пікселя, кількість пікселів у заданому фрагменті, площу та оптичну щільність різних ділянок зображення. Невизначеності дозового планування оцінювали в програмі «Monaco Treatment Planning System» на основі значень поглинутих доз у зонах з мінімальною оптичною щільністю всередині контурів об’єкта опромінення, у чорному фоні внутрішніх порожнин та за межами зовнішнього контура тіла. Встановлено факт некоректного визначення програмою «eFilm» геометричних параметрів зображення з похибкою 8-15%. Значення оптичної щільності в чорному фоні варіювали від -1000 HU біля меж об’єкта до -834 HU на більшій відстані. Показано значні коливання поглинутих доз у зонах низької щільності: при однакових умовах вимірювання доза могла становити як 0,0 Гр, так і 15,4 Гр. На відстані 4 мм від зовнішнього контура при щільності -1001 HU доза дорівнювала 5,9 Гр і зростала при наближенні до контура. Отримані результати свідчать, що похибки формування DICOM-зображень і розрахунку доз можуть зумовлювати істотні невизначеності, які впливають на точність планування та ефективність лікування. Удосконалення програмного забезпечення комп'ютерної томографії (КТ) та планувальних систем розглядається як перспективний шлях для зменшення таких похибок.
Abstract
The uncertainties in radiation therapy planning. Kikhtenko I.M., Khvorostenko Y.M., Filonenko N.Yu., Haldina O.M. The quality of radiation therapy has significantly improved due to the introduction of new irradiation sources, advanced delivery techniques, and modern three-dimensional treatment planning. However, the level of radiation-induced damage remains considerable, necessitating an assessment of the accuracy of tools responsible for image generation and dose calculation. The aim of the study was to identify potential uncertainties arising from the use of the TOSHIBA Asteion Super 4 computed tomography software and the planning systems of the Elekta Synergy linear accelerator (Elekta Limited), as well as to determine approaches for reducing these uncertainties. Twenty-eight patient radiotherapy plans carried out on the Elekta Synergy accelerator within the past four years were subjected to analysis. To evaluate image parameters, computed tomography data with a slice reconstruction thickness of 1.5 mm processed using the eFilm software were analysed. Pixel size, the number of pixels within a selected region, area, and optical density of various image segments were measured. Dose-planning uncertainties were estimated in the Monaco Treatment Planning System software based on absorbed-dose values in regions with minimal optical density inside the irradiation target contours, in the black-background cavities within the object, and outside the external body contour at various distances. The analysis revealed incorrect determination of image geometric parameters by eFilm, with an error of 8-15%. Optical-density values in the black background ranged from –1000 HU near the object boundary to -834 HU at greater distances. Significant variations in absorbed dose were observed in low-density regions: under identical conditions, dose values ranged from 0.0 Gy to 15.4 Gy. At a distance of 4 mm from the outer contour, an optical density of -1001 HU corresponded to a dose of 5.9 Gy, increasing with proximity to the contour. These findings indicate that errors in DICOM-image formation and dose calculation may introduce substantial uncertainties affecting treatment-planning accuracy and therapeutic outcomes. Improving computed tomography (CT) image-processing software and radiotherapy planning systems is considered a promising approach to reducing such uncertainties.
Захворюваність на онкологічну патологію у світі невпинно зростає. За даними ВООЗ, у 2022 році було зареєстровано 20 млн нових випадків раку, з яких 9,7 млн завершилися летально; кількість пацієнтів, що пережили п’ятирічний рубіж, становила 53,3 млн. За прогнозами, до 2050 року захворюваність зросте на 77% і досягне 35 млн випадків, при цьому в країнах з низьким індексом розвитку людського потенціалу приріст може становити до 142% порівняно з 2022 роком [1]. У США у 2025 році очікується близько 2 041 910 нових випадків раку (приблизно 5600 щодня), тоді як у світі цей показник перевищить 52 900 випадків на добу [2, 3].
В Україні зберігається світова тенденція зростання онкологічної захворюваності. Так, за даними Національного канцер-реєстру України, у 2024 році на обліку перебувало понад 1,1 млн пацієнтів з онкологічними захворюваннями. Серед хворих, що перебували під спостереженням упродовж п’яти років, чоловіки працездатного віку становили 39,9%, жінки – 48,1%, з яких 9,9% були репродуктивного віку; решта – особи пенсійного віку [4]. Пропорційно зростає також кількість пацієнтів, які отримують комбіноване спеціалізоване лікування, що включає хірургічний, променевий та хіміо-гормональний або імунний компоненти [5].
Променева терапія є ключовою складовою багатокомпонентного лікування раку [6, 7]. За даними ВООЗ, понад 50% онкологічних пацієнтів потребують променевої терапії при лікуванні найбільш поширених форм злоякісних новоутворень [8], і щороку близько 7 млн хворих у світі проходять відповідні курси лікування. Водночас навіть застосування сучасних променевих технологій не усуває ризику розвитку променевих ушкоджень нормальних тканин і вторинних злоякісних новоутворень [9]. Зокрема, від 74 до 100% жінок після опромінення з приводу раку молочної залози мають прояви ушкодження шкіри, серед яких променевий фіброз є тяжким, прогресуючим та незворотним пізнім ускладненням. Частота радіаційно-індукованих уражень легень становить 4,5-63% у проспективних і 0,9-30% у ретроспективних дослідженнях [10], а ризик розвитку серцевої недостатності внаслідок дифузного фіброзу міокарда зростає в 16 разів [11].
Таким чином, зростання кількості онкологічних пацієнтів й обсягів променевої терапії робить проблему променевих ушкоджень нормальних тканин особливо актуальною. Незважаючи на вдосконалення технологій опромінення та сучасне тривимірне планування, променеві ускладнення залишаються поширеними, що пов’язують з невизначеностями, притаманними багатокомпонентному процесу підготовки та проведення лікування із застосуванням складної апаратури [12]. Через це питання невизначеностей активно опрацьовують на національному та міжнародному рівні [13]. Сучасні підходи до оцінювання невизначеностей у променевій терапії базуються на рекомендаціях провідних міжнародних організацій, зокрема AAPM та IAEA [15-19]. Згідно з AAPM TG-132 [20] та TG-179 [21], геометричні та дозиметричні невизначеності можуть виникати на всіх етапах – від отримання зображень до планування та реалізації лікування. Також у цитованих документах підкреслюється критична роль точності визначення об’ємів, зв’язку між HU й електронною щільністю та акцентується увага на необхідності систематичного контролю якості, калібрування перетворення КТ-чисел у щільність та врахування алгоритмічних похибок TPS.
Результати досліджень розподілу доз на фантомних моделях свідчать про зменшення доз поза полем із віддаленням від його краю та зі збільшенням глибини [22], водночас на периферії поля може спостерігатися локальне зростання дози. Так, для прискорювача Oncor зафіксовано пік периферичної дози до 1,4% на відстані 6 см від краю поля 10×10 см² для електронних пучків 6 і 9 МеВ, а для 15 МеВ – до 2,3% за аналогічних умов [23]. Це зумовлено інтенсивним розсіюванням електронів у головці прискорювача, аплікаторах, вирізах і повітрі, що призводить до утворення фотонного випромінювання та електронів низької енергії і формування клінічно неприйнятної півтіні. Інші дослідження виявили піки периферичної дози на відстані 12-15 см за краєм поля [24], а максимальні значення – для електронних пучків з енергією 18 МеВ [25]. У літературі підкреслюється критична важливість контролю периферичних доз й оптимізації апаратного забезпечення з метою підвищення безпеки пацієнтів [26], а одним з резервів покращення результатів лікування вважається виявлення та мінімізація неврахованих невизначеностей [27].
Для планування променевої терапії найчастіше використовують дані рентген-комп’ютерної томографії, що зберігаються у форматі DICOM – міжнародному стандарті медичних зображень, підтримуваному провідними виробниками радіологічного обладнання [28, 29]. Одним з поширених програмних продуктів для їх аналізу є «eFilm». Проведений нами аналіз КТ-зображень показав, що навіть за дослідження однієї й тієї ж анатомічної ділянки на одному апараті та за однакових режимів вимірювані параметри можуть відрізнятися за розмірністю пікселя та щільністю [30]. З огляду на те, що в окремих випадках межу між нормою і патологією визначають десяті частки міліметра та кілька одиниць Хаунсфілда, а піксель (воксель) є базовою структурною одиницею планування конформної променевої терапії, доцільним є детальне дослідження його характеристик [31] та особливостей розподілу поглинутих доз у системах планування і гарантії якості радіотерапії.
Сучасний розвиток технологій штучного інтелекту суттєво трансформує процеси планування променевої терапії, зокрема етап сегментації та контурингу [32]. Сучасні алгоритми реконструкції КТ-зображень, зокрема ітеративної реконструкції зображень та реконструкції КТ-зображень на основі глибинного навчання (deep learning-based reconstruction, DLR) [33], можуть змінювати значення HU, зменшувати шум та згладжувати границі структур, що потенційно впливає на точність сегментації та дозиметричних розрахунків. За даними сучасних досліджень [34-37], відхилення HU при використанні DLR можуть досягати клінічно значущих величин, особливо на межах тканин. Це створює додаткові джерела систематичних невизначеностей у плануванні променевої терапії.
Метою цієї роботи було наукове обґрунтування та експериментальне дослідження впливу геометричних і дозиметричних невизначеностей, пов’язаних із характеристиками пікселів і вокселів DICOM-зображень рентген-комп’ютерної томографії, на формування планів променевої терапії та визначення поглинутих доз у зонах клінічного інтересу.
МАТЕРІАЛИ ТА МЕТОДИ ДОСЛІДЖЕНЬ
Рентген-комп’ютерну томографію (РКТ) пацієнтів з пухлинами мозку виконували на комп’ютерному томографі TOSHIBA Asteion Super 4. Аналізували поперечні зрізи з товщиною реконструкції 1,5 мм за допомогою програми обробки DICOM-файлів «eFilm» («Phillips Medical MXLiteView Version 1.22 MS»), яка дозволяє визначати розміри пікселя, кількість пікселів у заданій області, площу та оптичну щільність зображення.
На площині зрізу прямокутним маркером ROI Rectangle виділяли ділянки пухлини розміром 1-28 суміжних пікселів, розташованих у ряд. На одному зрізі аналізували шість таких ділянок – максимальну кількість, що допускається програмою, кожну з яких маркували окремим кольором. Розміри полів, їх площа, кількість пікселів та оптична щільність автоматично визначалися програмою і відображалися у вигляді цифрових значень, які заносили до таблиць для подальшого порівняння з результатами ручних вимірювань.
Крім того, визначали оптичну щільність ділянок поза межами об’єкта дослідження (чорний фон). Для цього квадратним маркером виділяли шість ділянок розміром один піксель кожна на різній відстані по променю від краю контура зображення. Отримані дані також табулювали та аналізували.
Невизначеності, що виникають при плануванні променевої терапії на електронному прискорювачі Elekta Synergy з використанням планувальної системи Monaco TPS, оцінювали за даними розподілу поглинутих доз на поперечних зрізах. Аналіз проводили в зонах з мінімальною оптичною щільністю всередині контурів об’єкта, у чорному фоні порожнин, а також у ділянках поза зовнішніми контурами тіла пацієнта на різних відстанях.
Клінічні методи обстеження (інструментальні та лабораторні) застосовувалися відповідно до сучасних рекомендацій [14-16, 38-42]. Рандомізоване дослідження проведено за даними комп’ютерного планування у 28 хворих зі злоякісними новоутвореннями молочної залози, головного мозку, гортані та стравоходу.
Кількісні та якісні дані були подані відповідно до загальноприйнятих статистичних підходів. Статистичний аналіз даних 28 планів променевої терапії проводився із застосуванням критерію χ², критерію Вілкоксона – Манна – Вїтні та пермутаційного підходу [43, 44]. Для всіх оцінок використовувався рівень довірчої ймовірності 97,5%, що забезпечує високу надійність інтервалів. Обчислення виконувалися в програмному середовищі Python 3.14.2 (Python Software Foundation License, вільне програмне забезпечення) за допомогою хмарного застосунку Google Colab, Free License) з використанням модуля stats бібліотеки SciPy (безкоштовна бібліотека Python з відкритим кодом, яка використовується для наукових та технічних обчислень, що не передбачає індивідуального номера ліцензії).
Дослідження схвалені комісією з питань біомедичної етики ДДМУ (витяг з протоколу № 32 від 11.11.2025 р.) та проведені згідно з письмовою згодою учасників і відповідно до принципів біоетики, викладених у Гельсінській декларації «Етичні принципи медичних досліджень за участю людей» та «Загальній декларації про біоетику та права людини (ЮНЕСКО)».
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
Дані вимірювання розміру пікселів на знімках хворої К. подано на рисунку 1.
Отримані дані програмного визначення розміру пікселя, довжини виділеної ділянки зображення, її площі, а також розрахункового розміру пікселя, довжини та площі зображення внесені до таблиці 1.
Кількість Пікселі (мм) Площа (мм2) розмір (програма) розмір (розрахунок) розмір (програма) розмір (розрахунок) 1 0,5 0,5 0,2 0,25 2 1 1 0,5 0,5 3 1,5 1,5 0,7 0,75 4 2,0 2,0 1,0 1,0 5 2,4 2,5 1,2 1,25 6 2,9 3,0 1,4 1,5
В іншої пацієнтки Ів., у якої поперечні зрізи головного мозку були виконані на тому ж апараті та за аналогічних умов, було отримано результати, подані на рисунку 2.
Отримані дані програмного визначення розміру пікселя, довжини та площі виділеної ділянки зображення, а також розрахункових значень розміру пікселя, довжини та площі зображення внесено до таблиці 2.
Кількість Пікселі (мм) Площа (мм2) розмір (програма) розмір (розрахунок) розмір (програма) розмір (розрахунок) 1 0,4 0,4 0,2 0,16 2 0,9 0,8 0,4 0,32 3 1,3 1,2 0,6 0,48 4 1,8 1,6 0,8 0,64 5 2,2 2,0 1,0 0,8 6 2,7 2,4 1,2 0,96
На рисунку 3 наведено результати вимірювання інструментами програми eFilm значень оптичної щільності чорного фону вздовж променя від краю зображення поперечного зрізу головного мозку пацієнтки К.
Розрахункові дані внесено до таблиці 3.
Ділянки Щільність (HU) % відповідності Відстань (мм) Різниця відстані (разів) 1 -1000 - 17,1 - По променю 2 -834 83,4 18,1 6,24 3 -1000 2,9 По променю 4 -876 87,6 20,5 7,07 5 -1000 2,9 6 -1000 - 22,4 -
На рисунку 4 а, б, в наведено результати визначення поглинутих доз та оптичної щільності програмою планувальної системи на різних відстанях від зовнішнього контура.
Результати вимірювання поглинутої дози поза межами зовнішнього контура поперечного зрізу наведено в таблиці 4.
Номер заміру Відстань від зовнішнього контура поперечного зрізу (мм) Оптична цільність (HU) Поглинута доза (Гр) 1 4,0 –1001 5,9 2 3,5 –999 8,6 3 3,0 –979 16 4 1,5 –535 28
Наступні зображення (рис. 5 а, б) демонструють різні значення поглинутої дози в чорному фоні поза межами зрізу за однакових значень оптичної щільності.
На рисунку 6 наведено зображення поперечного зрізу пацієнта з раком носоглотки.
Сьогодні в плануванні променевої терапії засоби обробки та аналізу інформації на основі DICOM-файлів використовуються понад 30 років і стали міжнародним стандартом медичного зображення [28, 29]. МАГАТЕ (2021) наголосила на застосуванні DICOM-файлів на всіх етапах променевої терапії – діагностиці, дозиметрії, плануванні та реалізації лікування [45, 31].
Раніше нами були наведені результати щодо невизначеностей у рівномірності опромінення тканин за рахунок значущої розбіжності значень оптичної щільності суміжних пікселів та вокселів [30]. Аналіз даних вимірювання розміру пікселів та їхніх похідних у пацієнтки К. (рис. 1, табл. 1) показав таке.
Програмою визначено довжину сторони одного пікселя – 0,5 мм. До четвертого пікселя включно розмір відрізка залишався коректним, але між четвертим та п’ятим пікселем відстань мала бути 2,5 мм, тоді як фактично вона дорівнювала 2,4 мм. Виявлено також розбіжності між результатами визначення площі пікселя програмою (зображення 2, рис. 1) та ручним розрахунком. Програма показала площу 0,2 мм2, але з урахуванням розміру сторони пікселя (зображення 1, рис. 1) площа мала б становити 0,25 мм2. Для ділянок з двох та чотирьох пікселів площа, визначена програмою, збігалася з ручними розрахунками. Для ділянки з трьох пікселів відмінність становила 7,1%, з п’яти – 4,2%, з шести – 7,1%. Цілком можливо, що при збільшенні розмірів ділянки похибка виявить системність характеру, але точність планування променевої терапії ґрунтується на характеристиках вокселя, який складається з окремих пікселів, тому будь-які похибки в DICOM-файлах, що вважаються «золотим стандартом» якості медичного зображення, – неприпустимі.
В іншої пацієнтки (рис. 2, табл. 2) отримано інші результати, але теж з відмінностями. Як видно з даних, наведених у таблицях, в обох випадках спостерігається некоректне визначення програмою «eFilm» розмірів пікселя, довжини виділеної ділянки зображення та її площі, значення яких перевіряли ручними арифметичними розрахунками.
Так, у першому випадку на зрізі пацієнтки К. розмір пікселя становив 0,5 см, однак розмір відрізка з шести пікселів зменшився між четвертим та п’ятим пікселем (2,0 мм-2,4 мм), тобто замість 0,5 мм становив 0,4 мм, після чого знову дорівнював 0,5 мм (2,4 мм-2,9 мм). При аналізі програмного розрахунку площі виявилася певна закономірність. Площа з першого по другий піксель змінилася на 0,3 мм2, з другого по третій – на 0,2 мм2 , з третього по четвертий – знов на 0,3 мм2, з четвертого по п’ятий – на 0,2 мм2, з п’ятого по шостий – знов на 0,2 мм2, порушивши попередню послідовність. Можливо, при збільшенні кількості вимірювань та розрахунків закономірність виявилася би більш чіткою, але на цьому етапі її слід вважати відсутньою, а похибку програми – випадковою [14].
У пацієнтки Ів. аналіз даних, наведених у таблиці 2, виявив системну похибку 10% щодо площі зображення пікселів та 11% – щодо розмірів пікселів. При цьому фізичні умови томографії обох хворих були однаковими. Загалом проведений непараметричний аналіз програмних та розрахункових даних щодо геометричних невизначеностей виявив похибку 8-15% (статистична значущість визначалася за порогом p<0,025) залежно від того, яка ділянка розглядається – у центрі чи на периферії.
Слід зазначити, що в самому стандарті DICOM (https://www.dicomstandard.org/current) наведено перелік можливих причин порушень при відтворенні зображень. Найбільш схильними до геометричних спотворень є зображення, отримані МРТ (магнітно-резонансна томографія). У центрі поля зору (isocenter) типове середнє спотворення становить близько 0,4-0,8 мм, на периферії (на відстані 200 мм від центру) спотворення може зростати до 2-5 мм і більше. Для стереотаксичної радіохірургії критично важлива точність – похибка понад 1 мм для малих цілей (менше 20 мм) може вважатися клінічно неприйнятною (втрата якості/точності понад 5% в індексах планування). КТ (комп'ютерна томографія) та рентгенографія мають набагато менші геометричні спотворення, ніж МРТ, за винятком ефектів проекції (наприклад, видовження або вкорочення кісток на звичайному рентгенівському знімку через кут зйомки). При КТ спотворення можуть спричиняти різницю в розрахунках об'єму певних структур мозку (наприклад, кори) до 5,5% при порівнянні скоригованих і нескоригованих зображень. Відносне спотворення може бути від менше ніж 1% (у добре каліброваних системах КТ або в центрі поля зору МРТ) до понад 10-20% відносного відхилення розміру на периферії зображення. Це не просто «втрата якості» в загальному розумінні, а критична втрата геометричної точності (зміна розмірів пікселів/вокселів), що впливає на клінічну достовірність зображення [46].
Таким чином, у проведеному дослідженні спостерігали зміну розміру пікселів/вокселів в отриманих зображеннях – неточність, яка вже закладена в самому стандарті та може призвести до дуже серйозних наслідків при плануванні лікування.
Особливу увагу слід звернути на значення оптичної щільності поза зовнішніми контурами зображення об’єкта (чорний фон). Аналіз даних (рис. 3 та табл. 3) показав, що оптична щільність поза зображенням досліджуваної області («чорний фон», «нуль пікселів зображення») у першій парі по променю (2, 3) на відстані 18,1 мм дорівнює -834 HU, а на відстані 2,9 мм вона становить -1000 HU, тобто менша оптична щільність чорного фону знаходиться в 6,24 раза ближче до краю зображення поперечного зрізу черепа, ніж оптична щільність -834 HU, що суперечить очікуваній закономірності. У другій парі (4, 5) ця відстань ще більша – 7,07 раза.
Отже, оптична щільність чорного фону змінюється по променю від -1000 HU поблизу межі об'єкта, що досліджується, до -834 HU на відстані в 7 разів далі. Наявність ділянок різнорідної щільності поза зображенням зрізу, на тлі «абсолютного нуля», не виключає можливість аналогічних артефактів і на головному об'єкті – зображенні поперечного зрізу пацієнта. Це може негативно впливати на оцінку результатів лікування, а також на формування плану подальшої терапії, якщо в основу будуть покладені некоректні дані, оскільки дози для фотонної променевої терапії безпосередньо пов'язані зі значеннями Хаунсфілда (HU), отриманими з комп'ютерної томографії [47].
При аналізі результатів поглинутих доз та оптичної щільності, які визначила програма планувальної системи (рис. 4 а, б, в, табл. 4), можна констатувати, що на відстані 4 мм від зовнішнього контура поперечного зрізу при оптичній щільності зображення -1001 HU поглинута доза дорівнює 5,9 Гр. При зменшення відстані – доза зростає. Але зовнішній контур зображення поперечного зрізу, який окреслює лікар, є межею, де дія програми мала б припинитися. Разом з тим цього не відбувається і програма продовжує формувати план майбутнього опромінення. Отже аналогічні дії програми можуть відбуватися і за межами інших контурів, критично важливих – PTV, GTV та нормальних тканин. Така невизначеність може стати причиною некоректних значень поглинутих доз в об’ємах інтересу та призвести до погіршення результатів лікування пацієнта.
Привертає увагу наявність різних значень поглинутої дози в чорному фоні поза межами зрізу з однаковим значенням оптичної щільності (рис. 5 а, б). При однаковій оптичній щільності чорного фону -992 HU, на одному поперечному зрізі поглинута доза в одному вимірюванні дорівнювала 0,0 Гр, що відповідає фізичним закономірностям поглинання енергії випромінювання, тоді як в іншому вимірюванні вона становила 15,4 Гр, що пояснити складно.
Наступний приклад стосується поглинутої дози в повітрі порожнини основної пазухи (рис. 6). Якщо попередні результати складно пояснити, але вони не впливали на опромінення тканин хворого, бо знаходилися поза межами зовнішнього контура зрізу, то в цьому випадку виміряна поглинута доза в повітрі порожнини основної пазухи знаходиться всередині поперечного зрізу, поряд з пухлиною та критичними тканинами. Невизначеність полягає у великій поглинутій дозі – 56,2 Гр, яку визначає програма планувальної системи в повітряній порожнині основної пазухи. При цьому розміри порожнини досить великі, 3,05×2,3 см, а оптична щільність -994 HU.
Дослідження периферичних доз у пацієнтів є важливою задачею, оскільки буде вплив на сусідні органи та тканини, що знаходяться в зоні ризику. Слід зазначити, що під час лікування з використанням іонізуючого випромінення має вплив розсіювання, яке виникає як від компонентів прискорювача (утворюючи клінічно неприйнятну півтінь), так і від самого пацієнта. Це може сприяти збільшенню дози опромінення в тканинах за межами області лікування [48].
Резюмуючи, слід зазначити, що нами здійснено спробу визначити чинники, які можуть впливати на точність планування променевої терапії онкологічних хворих з використанням наведеної технології та відповідних засобів. Розбіжність між принципом недопущення перевищення толерантної дози для нормальних тканин і високою частотою променевих ушкоджень у більшості пацієнтів у світі може бути зменшена шляхом виявлення та усунення невизначеностей на будь-якому етапі радіаційної технології лікування. У перспективі планується системне дослідження невизначеностей у різних планувальних системах, проведення калібрування HU, аналіз впливу розміру вокселя та геометричних похибок на дозиметричні параметри, а також оцінювання потенціалу застосування штучного інтелекту для підвищення точності планування.
ВИСНОВКИ
1. Проведений аналіз показав, що програма формування зображень у форматі DICOM та програмне забезпечення планування променевої терапії на електронному прискорювачі можуть давати результати з різними видами похибок. Ці похибки зумовлюють невизначеності у визначенні поглинутих доз, що потенційно може призвести до зниження ефективності лікування онкологічних хворих.
2. Ймовірним шляхом зменшення похибок може бути удосконалення програмного забезпечення для обробки та аналізу DICOM-файлів рентген-комп’ютерної томографії, а також програмного забезпечення планувальних систем променевої терапії. Інтеграція технологій штучного інтелекту в процес планування променевої терапії відкриває нові можливості для підвищення ефективності та стандартизації, однак водночас формує нові джерела невизначеності, що потребують ретельного контролю якості та експертної оцінки.
Внески авторів:
Кіхтенко І.М. – концептуалізація, методологія, написання – початковий проєкт;
Хворостенко Ю.М. – дослідження, ресурси, курація даних, візуалізація;
Філоненко Н.Ю. – методологія, формальний аналіз, написання – рецензування та редагування;
Галдіна О.М. – формальний аналіз, написання – рецензування та редагування.
Фінансування. Дослідження не має зовнішніх джерел фінансування.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів.
REFERENCES
1. World Health Organization. Global cancer burden growing amidst mounting need for services [Internet]. 2024 [cited 2025 Dec 12]. Available from: https://www.who.int/news/item/01-02-2024-global-cancer-burden-growing--amidst-mounting-need-for-services
2. Siegel RL, Kratzer TB, Giaquinto AN, Sung H, Jemal A. Cancer statistics, 2025. CA Cancer J Clin. 2025;75(1):10-45. doi: https://doi.org/10.3322/caac.21871
3. Liu B, Zhou H, Tan L, Siu KTH, Guan XY. Exploring treatment options in cancer: tumor treatment strategies. Signal Transduct Target Ther. 2024;9:175. doi: https://doi.org/10.1038/s41392-024-01856-7
4. Fedorenko ZP, Gorokh Ye, Ryzhov A, Soumkina O. [Cancer in Ukraine, 2023-2024: Incidence, Mortality, and Performance Indicators of the Oncology Service]. Bull Natl Cancer Regist Ukr. Vol. 26. [Internet]. Kyiv; 2025 [cited 2025 Dec 12]. Ukrainian. Available from: http://www.ncru.inf.ua/publications/BULL_26/PDF_E/0-titul.pdf
5. Zafar A, Khatoon S, Khan MJ, Abu J, Naeem A. Advancements and limitations in traditional anti-cancer therapies: a comprehensive review. Discov Onc. 2025;16:607. doi: https://doi.org/10.1007/s12672-025-02198-8
6. Desai I, Thakur S, Pagariya P. Current advances in immunotherapy for cancer. Oral Oncol Rep. 2024;12:100652. doi: https://doi.org/10.1016/j.oor.2024.100652
7. Portik D, Lacombe D, Faivre-Finn C, Achard V, Andratschke N, Correia D, et al. The 2024 State of Science report from the the European Organisation for Research and Treatment of Cancer’s Radiation Oncology Scientific Council. Eur J Cancer. 2025;220:115334. doi: https://doi.org/10.1016/j.ejca.2025.115334
8. World Health Organization/IAEA. New WHO/IAEA publication provides guidance on radiotherapy equipment to fight cancer [Internet]. 2021 [cited 2025 Dec 12]. Available from: https://www.who.int/news/item/05-03-2021-new-who-iaea-publication-provides-guidance-on-radiotherapy-equipment-to-fight-cancer
9. Majeed H, Gupta V. Adverse effects of radiation therapy. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan [cited 2025 Dec 12]. Available from: https://www.ncbi.nlm.nih.gov/books/NBK563259/
10. Catalano O, Fusco R, Carriero S, Tamburrini S, Granata V. Ultrasound findings after breast cancer radiation therapy. Korean J Radiol. 2024;25(11):982-91. doi: https://doi.org/10.3348/kjr.2024.0672
11. Moisander M, Skyttä T, Kivistö S, et al. Radiotherapy-induced diffuse myocardial fibrosis in early-stage breast cancer patients. Radiat Oncol. 2023;18(1):124. doi: https://doi.org/10.1186/s13014-023-02319-z
12. Singh P, Mishra A, Mishra SK. Challenges and potential side effects of radiation therapy for palliative cancer treatment. Med Palliative. 2024;23(2):75-91. doi: https://doi.org/10.1016/j.medpal.2023.12.002
13. Ohno T, Kamiguchi A, Honda M, Shimohigashi Y, Kuraoka A, Toyota M, et al. Enhancing patient positioning precision: a comparative analysis of surface-guided radiation therapy systems. Radiol Phys Technol. 2025 Sep;18(3):833-50. doi: https://doi.org/10.1007/s12194-025-00937-8
14. International Atomic Energy Agency. Accuracy requirements and uncertainties in radiotherapy. [Internet]. Vienna: International Atomic Energy Agency; 2016 [cited 2025 Dec 12]. (IAEA Human Health Series. No. 31). Available from: https://www-pub.iaea.org/MTCD/Publications/PDF/P1679_HH31_web.pdf
15. International Atomic Energy Agency. Handbook of basic quality control tests for diagnostic radiology. [Internet]. Vienna: International Atomic Energy Agency; 2023 [cited 2025 Dec 12]. (IAEA Human Health Series. No. 47). Available from: https://www-pub.iaea.org/MTCD/Publications/PDF/PUB2021_web.pdf
16. International Atomic Energy Agency. Absorbed dose determination in external beam radiotherapy. [Internet]. Vienna: International Atomic Energy Agency; 2024 [cited 2025 Dec 12]. (Technical Reports Series. No. 398 (Rev. 1)). Available from: https://www-pub.iaea.org/MTCD/Publications/PDF/TRS398_scr.pdf
17. International Atomic Energy Agency. Dosimetry in Brachytherapy – An International Code of Practice for Secondary Standards Dosimetry Laboratories and Hospitals. [Internet]. Vienna: International Atomic Energy Agency; 2023 [cited 2025 Dec 12]. (Technical Reports Series. No. 492). Available from: https://www-pub.iaea.org/MTCD/Publications/PDF/DOC-010-492_web.pdf
18. American Association of Physicists in Medicine. Physical Uncertainties in the Planning and Delivery of Light Ion Beam Treatments: The Report of AAPM Task Group 202. [Internet]. Alexandria (VA): AAPM; 2020 [cited 2025 Dec 12]. 124 p. (AAPM Report. No. 202). Available from: https://www.aapm.org/pubs/reports/RPT_202.pdf
19. Siochi RA, Balter P, Bloch CD, Santanam L, Blodgett K, Curran BH, et al. Report of Task Group 201 of the American Association of Physicists in Medicine: quality management of external beam therapy data transfer. Med Phys. 2021;48:e86-114. doi: https://doi.org/10.1002/mp.14868
20. Brock KK, Mutic S, McNutt TR, Li H, Kessler ML. Use of image registration and fusion algorithms and techniques in radiotherapy: report of the AAPM Radiation Therapy Committee Task Group No. 132. Med Phys. 2017;44:e43-76. doi: https://doi.org/10.1002/mp.12256
21. Bissonnette JP, Balter PA, Dong L, Langen KM, Lovelock DM, Miften M, et al. Quality assurance for image-guided radiation therapy utilizing CT-based technologies: a report of the AAPM TG-179. Med Phys. 2012;39:1946-63. doi: https://doi.org/10.1118/1.3690466
22. Matuszak N, Kruszyna-Mochalska M, Skrobala A, Ryczkowski A, Romanski P, Piotrowski I, et al. Nontarget and out-of-field doses from electron beam radiotherapy. Life. 2022;12(6):858. doi: https://doi.org/10.3390/life12060858
23. Maharaj KD, Dass J, Ibrahim M, Mahmood T, Rowshanfarzad P. Peripheral Doses Beyond Electron Applicators in Conventional C-Arm Linear Accelerators: A Systematic Literature Review. Technology in Cancer Research & Treatment. 2024;23:15330338241239144. doi: https://doi.org/10.1177/15330338241239144
24. Gul OV. Experimental evaluation of out-of-field dose for different high-energy electron beams and applicators used in external beam radiotherapy. Radiat Phys Chem. 2024;215:111345. doi: https://doi.org/10.1016/j.radphyschem.2023.111345
25. Maharaj KD, Sabet M, Dass J, Ibrahim M, Mahmood T, Rowshanfarzad P. Comprehensive analysis of peripheral dose in electron beam therapy with a Varian TrueBeam Linac. Radiat Med Prot. 2025;6(1):28-36. doi: https://doi.org/10.1016/j.radmp.2024.10.003
26. Maharaj KD, Dass J, Ibrahim M, Mahmood T, Rowshanfarzad P. Peripheral doses beyond electron applicators in conventional C-arm linear accelerators: a systematic literature review. Technol Cancer Res Treat. 2024;23:1-9. doi: https://doi.org/10.1177/15330338241239144
27. van den Berg CAT, Meliadò EF. Uncertainty assessment for deep learning radiotherapy applications. Semin Radiat Oncol. 2022;32(4):304-18. doi: https://doi.org/10.1016/j.semradonc.2022.06.001
28. Yang L. DICOM standard and its application in radioinformatics. Int J Comput Sci Inf Technol. 2024;2(1):384-90. doi: https://doi.org/10.62051/ijcsit.v2n1.40
29. Larobina M. Thirty years of the DICOM standard. Tomography. 2023;9:1829-38. doi: https://doi.org/10.3390/tomography9050145
30. Khvorostenko MI, Kikhtenko IM, Khvorostenko YM. [Influence of tumor tissue heterogeneity on the quality of radiotherapy planning]. [Internet]. Ukr Radiol J. 2016 [cited 2025 Dec 12];24(2):67-72. Ukrainian. Available from: https://irbis-nbuv.gov.ua/cgi-bin/irbis_nbuv/cgiirbis_64.exe?C21COM=2&I21DBN=UJRN&P21DBN=UJRN&IMAGE_FILE_DOWNLOAD=1&Image_file_name=PDF/URLZh_2016_24_2_16.pdf
31. Moeller TB, Reif E. Normal findings in CT and MRI [Internet]. Stuttgart: Thieme; 2000 [cited 2025 Dec 12]. 256 p. Available from: https://radoir.org/en/wp-content/uploads/2018/06/NFCTMRI.pdf
32. Rasmussen ME, Akbarov K, Titovich E, et al. Potential of e-learning interventions and artificial intelligence-assisted contouring skills in radiotherapy: the ELAISA study. JCO Glob Oncol. 2024;10:e2400173. doi: https://doi.org/10.1200/GO.24.00173
33. Maduro Bustos LA, Sarkar A, Doyle LA, Andreou K, Noonan J, Nurbagandova D, et al. Feasibility evaluation of novel AI-based deep-learning contouring algorithm for radiotherapy. J Appl Clin Med Phys. 2023;24(11):e14090. doi: https://doi.org/10.1002/acm2.14090
34. Hu Y, Nguyen H, Smith C, Chen T, Byrne M, Archibald-Heeren B, et al. Clinical assessment of a novel machine-learning automated contouring tool for radiotherapy planning. J Appl Clin Med Phys. 2023;24(7):e13949. doi: https://doi.org/10.1002/acm2.13949
35. D'Aviero A, Re A, Catucci F, Piccari D, Votta C, Piro D, et al. Clinical Validation of a Deep-Learning Segmentation Software in Head and Neck: An Early Analysis in a Developing Radiation Oncology Center. Int J Environ Res Public Health. 2022;19(15):9057. doi: https://doi.org/10.3390/ijerph19159057
36. Finnegan RN, Quinn A, Horsley P, Chan J, Stewart M, Bromley R, et al. Geometric and dosimetric evaluation of a commercial AI auto-contouring tool on multiple anatomical sites in CT scans. J Appl Clin Med Phys. 2025;26(6):e70067. doi: https://doi.org/10.1002/acm2.70067
37. Soltaninejad A, Shahbazi-Gahrouei D, Khorasani A, Hemati S. Evaluation of CNN-based deep learning models for auto-contouring in glioblastoma radiotherapy: a review. Radiat Oncol. 2025;20(1):169. doi: https://doi.org/10.1186/s13014-025-02748-y
38. International Atomic Energy Agency. Setting Up a Radiotherapy Programme. [Internet]. Vienna: International Atomic Energy Agency; 2008 [cited 2025 Dec 12]. Available from: https://www-pub.iaea.org/MTCD/Publications/PDF/pub1296_web.pdf
39. International Atomic Energy Agency. A Handbook for the Education of Radiation Therapists (RTTs). [Internet]. Vienna: International Atomic Energy Agency; 2014 [cited 2025 Dec 12]. (Training Course Series. No. 58). Available from:
https://www-pub.iaea.org/MTCD/Publications/PDF/TCS-58_web.pdf
40. Brown SR, Van Hemelrijck M, Price G, Oppong FB, Verhoeff JJC, Faivre-Finn C. Novel methodologies for clinical research in radiation oncology: Time to think outside of the box? A narrative review. Radiother Oncol. 2025 Dec 9:111311. doi: https://doi.org/10.1016/j.radonc.2025.111311
41. Green H, Rieu R, Slevin F, Ashmore L, Bulbeck H, Gkogkou P, et al. CTRad Working Group 4. Best practice for patient-centred radiotherapy in clinical trials and beyond: A national multidisciplinary consensus. Clin Oncol (R Coll Radiol). 2025;39:103732. doi: https://doi.org/10.1016/j.clon.2024.103732
42. Schaue D, McBride WH. Opportunities and challenges of radiotherapy for treating cancer. Nat Rev Clin Oncol. 2015 Sep;12(9):527-40. doi: https://doi.org/10.1038/nrclinonc.2015.120
43. Schober P, Vetter TR. Nonparametric Statistical Methods in Medical Research. Anesth Analg. 2020;131(6):1862-3. doi: https://doi.org/10.1213/ANE.0000000000005101
44. Bonnini S, Assegie GM, Trzcinska K. Review about the Permutation Approach in Hypothesis Testing. Mathematics. 2024;12(17):2617. doi: https://doi.org/10.3390/math12172617
45. World Health Organization. Technical specifications of radiotherapy equipment for cancer treatment. [Internet]. Geneva: WHO; 2021 [cited 2025 Dec 12]. Available from: https://www.oncologysystems.com/wp-content/uploads/2021/03/2021-Handbook-on-Radiotherapy-Equipment.pdf
46. Mabizela S. Navigating parametric and non-parametric statistical analyses: a practical guide in health sciences research. Wits J Clin Med. 2025;7(1):41-4. doi: https://doi.org/10.18772/26180197.2025.v7n1a9
47. Mohan R. A review of proton therapy – Current status and future directions. Prec Radiat Oncol. 2022;6:164-76. doi: https://doi.org/10.1002/pro6.1149
48. Mendes RMS, Silva MG, Rebello WF, Oliveira CL, Stenders RM, Medeiros MPC, et al. Influence of radiotherapy room shielding on ambient dose equivalent due to photons H(10)p and neutrons H(10)n in the patient’s plane. Appl Radiat Isot. 2022;181:110095. doi: https://doi.org/10.1016/j.apradiso.2021.110095
Key words: chronic heart failure, coronary artery disease, type 2 diabetes mellitus, obesity, lipid metabolism, GAS6
Ключові слова: хронічна серцева недостатність, ішемічна хвороба серця, цукровий діабет 2 типу, ожиріння, ліпідний обмін, GAS6
Abstract
Chronic heart failure (CHF) remains a critical problem, the relevance of which is growing against the background of cardiometabolic polymorbidity. Comorbid conditions such as type 2 diabetes mellitus (T2DM) and obesity have common pathogenetic mechanisms that accelerate myocardial remodelling and fibrosis. The GAS6 (Growth Arrest-Specific 6) protein, as a ligand for the TAM family of receptors, is a central regulator of inflammation, cell survival, and vascular remodelling. Establishing a link between GAS6 levels and specific lipid metabolism disorders in the context of CHF is critical for improving risk stratification. The aim of the study was to investigate the activity of GAS6 protein and its relationship with lipid metabolism indicators in patients with ischaemic CHF, as well as to determine its potential prognostic value for risk stratification depending on the presence of concomitant metabolic pathology. The study included 225 patients with ischemic CHF and 30 healthy individuals (control group). The patients were divided into 4 groups: Group 1 (n=75) – coronary artery disease (CAD) + T2DM + obesity; Group 2 (n=50) – CAD + T2DM; Group 3 (n=50) – CAD + obesity; Group 4 (n=50) – CAD without metabolic pathology. Lipid metabolism indicators (total cholesterol (TC), triglycerides (TG), high-density lipoprotein cholesterol (HDL-C), low-density lipoprotein cholesterol (LDL-C), very low-density lipoprotein cholesterol (VLDL-C), atherogenicity coefficient (AC)) and serum GAS6 levels (using the ELISA kit Cusabio, USA) were determined. Spearman's rank correlation coefficient was used to determine correlations, with a critical significance level of p<0.05. According to the results of the study, the GAS6 protein content was highest in Group 1 (31.64±18.71 ng/ml), exceeding the control values by 66.3% (p<0.001), which indicates the cumulative effect of combined pathology. GAS6 levels in Group 3 and Group 2 were significantly higher than the control (by 41.8% and 31.1% , respectively). When analysing the correlations in Group 1, strong and significant positive correlations were found between GAS6 and BMI (r=0.68) and proatherogenic lipid metabolism fractions (LDL-C (r=0.54), VLDL-C (r=0.51), TG (r=0.47)). GAS6 is a sensitive marker, the activation of which is closely associated with the number and type of concomitant metabolic disorders. The established strong direct relationship between GAS6 and BMI and proatherogenic lipid fractions confirms that this protein is a powerful biochemical mediator that reflects the degree of dyslipidaemia and exacerbates atherosclerosis processes in patients with cardiometabolic polymorbidity. The level of GAS6 can serve as an important diagnostic and prognostic marker for early stratification of patients with ischaemic heart failure.
Реферат
Білок GAS6 та дисфункція ліпідного обміну: потенційний біомаркер стратифікації ризику в пацієнтів з ішемічною хронічною серцевою недостатністю та метаболічними порушеннями. Боровик К.М., Кравчун П.Г., Кадикова О.І., Бабаджан В.Д. Хронічна серцева недостатність (ХСН) залишається критичною проблемою, актуальність якої зростає на тлі кардіометаболічної поліморбідності. Коморбідні стани у вигляді цукрового діабету (ЦД) 2 типу та ожиріння мають спільні патогенетичні механізми, що прискорюють ремоделювання міокарда та фіброз. Білок GAS6 (Growth Arrest-Specific 6), як ліганд рецепторів сімейства TAM (Tyro3, Axl, MerTK), є центральним регулятором запалення, клітинного виживання та судинного ремоделювання. Встановлення зв'язку між рівнем GAS6 та специфічними порушеннями ліпідного обміну на тлі ХСН є критично важливим для покращення стратифікації ризику. Метою дослідження стало дослідити активність білка GAS6 та його взаємозв'язок з показниками ліпідного обміну в пацієнтів з хронічною серцевою недостатністю ішемічного генезу, а також визначити його потенційне прогностичне значення для стратифікації ризику залежно від наявності супутньої метаболічної патології. Дослідження охопило 225 хворих з ХСН ішемічного генезу та 30 здорових осіб (контрольна група). Хворі були розподілені на 4 групи: група 1 (n=75) – ІХС + ЦД 2 типу + ожиріння; група 2 (n=50) – ІХС + ЦД 2; група 3 (n=50) – ІХС + ожиріння; група 4 (n=50) – ІХС без метаболічної патології. Проводили визначення показників ліпідного обміну (загальний холестерин (ЗХС), тригліцериди (ТГ), холестерин ліпопротеїнів високої щільності (ХС ЛПВЩ), холестерин ліпопротеїнів низької щільності (ХС ЛПНЩ), холестерин ліпопротеїнів дуже низької щільності (ХС ЛПДНЩ), коефіцієнт атерогенності (КА)) та сироваткового рівня GAS6 (імуноферментним методом, «Cusabio», США). Для встановлення потенційного прогностичного значення GAS6 та стратифікації ризику було використано кореляційний аналіз Спірмена при критичному рівні значущості p<0,05 та ROC-аналіз. За результатами проведеного дослідження вміст білка GAS6 був найвищим у групі 1 (31,64±18,71 нг/мл), перевищуючи показники контролю на 66,3% (p<0,001), що свідчить про кумулятивний вплив поєднаної патології. Рівні GAS6 у групі 3 та групі 2 були достовірно вищими за контроль (на 41,8% та 31,1% відповідно). При аналізі кореляційних зв'язків у групі 1 виявлено сильні та достовірні позитивні кореляції GAS6 з індексом маси тіла (ІМТ) (r=0,68) та проатерогенними фракціями ліпідного обміну (ХС ЛПНЩ (r=0,54), ХС ЛПДНЩ (r=0,51), ТГ (r=0,47)). GAS6 є чутливим маркером, активація якого тісно асоційована з кількістю та типом супутніх метаболічних порушень. Установлений сильний прямий зв'язок GAS6 з ІМТ та проатерогенними фракціями ліпідів підтверджує, що цей білок є потужним біохімічним посередником, який відображає ступінь дисліпідемії та посилює процеси атеросклерозу у хворих з кардіометаболічною поліморбідністю. Рівень GAS6 може слугувати важливим діагностично-прогностичним маркером для ранньої стратифікації пацієнтів з хронічною серцевою недостатністю ішемічного генезу.
Chronic heart failure (CHF) remains one of the most pressing problems in modern cardiology and healthcare, reaching pandemic proportions and affecting more than 64 million people worldwide [1]. The most common form is ischaemic CHF, which develops as a result of coronary artery disease (CAD). Epidemiological data show that CHF is associated with high mortality and rehospitalisation rates, and its economic burden is extremely high [2].
It is well known that lipid metabolism dysfunction, in particular dyslipidaemia, is not only a cause of CAD, but also aggravates the course of existing CHF, exacerbating inflammation, myocardial remodelling and cardiovascular damage [3]. Thus, identifying new links in the cardiometabolic connection is critical for improving risk stratification and developing targeted therapies.
The GAS6 (Growth Arrest-Specific 6) protein is a vitamin K-dependent ligand of the TAM (Tyro3, Axl, MerTK) receptor family and is widely expressed in the body, localizing in particular in intestinal cells, bone marrow, fibroblasts and endothelial cells [4]. The functional spectrum of the GAS6 protein covers a number of critical biological processes, acting as a central regulator of cell survival, proliferation, inflammation, and immune regulation [5, 6, 7]. Elevated levels of GAS6 have been detected in both acute coronary syndrome [8] and CHF, indicating its involvement in vascular and myocardial remodelling processes [9].
Currently there are discrepancies regarding the role of GAS6 in the cardiometabolic continuum, and the relationship between GAS6 levels and specific lipid metabolism disorders in the context of CHF remains poorly understood, especially in the context of concomitant metabolic pathology.
The aim was to investigate the activity of the GAS6 protein and its relationship with lipid metabolism indicators in patients with ischaemic сhronic heart failure, as well as to determine its potential prognostic value for risk stratification depending on the presence of concomitant metabolic disorders (type 2 diabetes mellitus and/or obesity).
MATERIALS AND METHODS OF RESEARCH
The research involved 225 hospitalized individuals receiving cardiac care at Kharkiv City Hospital No. 27. These participants were stratified into four cohorts to evaluate the impact of metabolic comorbidities on CHF. The first cohort (n=75) consisted of patients suffering from CHF and CAD complicated by both T2DM and obesity. The second and third cohorts (n=50 each) focused on CHF patients with either T2DM or obesity alone, respectively. A comparison group (Group 4, n=50) – patients with CHF and CAD but without metabolic disturbances. Additionally, a baseline was provided by a control group of 30 healthy volunteers. Statistical analysis confirmed the demographic homogeneity of the groups, particularly regarding mean age (63.44±17.84, 64.47±13.29, 60.59±17.18, and 63.27±12.16 years, respectively; p>0.05). The distribution of patients by gender was comparable across all study groups (χ²=1.84, p=0.61). In Group 1, there were 42 men (56.0%) and 33 women (44.0%); in Group 2 – 27 men (54.0%) and 23 women (46.0%); in Group 3 – 22 men (44.0%) and 28 women (56.0%); in Group 4 – 26 men (52.0%) and 24 women (48.0%). Comparison was performed using Pearson’s chi-square test.
In order to ensure scientific reliability and avoid systematic selection bias, the clinical groups formed were comparable in terms of key characteristics of heart failure. All groups were dominated by patients with HF stage II A (72% to 82% depending on the group) and NYHA functional class II (72.0%-84.0%), which allowed the sample to be standardized according to the severity of haemodynamic disorders. The comparability of the groups in terms of the main study objective was also confirmed by a unified approach to pharmacotherapy: all patients received basic treatment in accordance with the current protocols of the Ministry of Health of Ukraine and the ESC guidelines (2024). The use of quadruple therapy, which included sodium-dependent glucose co-transporter-2 inhibitors (100% of patients in all groups), β-blockers (97.3–100%), statins and antiplatelet agents (100%), ensured a uniform therapeutic background. This made it possible to neutralise the impact of differences in treatment on the study results and to identify concomitant T2DM and obesity as the main independent factors influencing changes in regulatory biomarkers.
The verification of CAD was performed in compliance with current international and domestic guidelines, specifically the European Society of Cardiology (ESC) standards and the Unified Clinical Protocol of the Ministry of Health of Ukraine "Stable Coronary Artery Disease" (Order No. 2857, dated December 23, 2021). The diagnosis of CHF followed the classification established by the Working Group on Cardiac Insufficiency of the Association of Cardiologists of Ukraine, with functional class (FC) determination based on the NYHA (New York Heart Association) system. T2DM was identified according to the Unified Clinical Protocol of the Ministry of Health of Ukraine "Diabetes Mellitus" (Order No. 1300, dated July 24, 2024). Abdominal obesity was assessed via anthropometric measurements, including waist and hip circumferences and the body mass index (BMI), the latter calculated as:
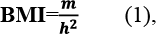
where
BMI – body mass index (kg/m2 );
m – body weight (kg);
h – height (m).
Potential participants were eligible if they were over 18 years of age, had CAD with clinical signs of CHF (with or without accompanying metabolic disorders such as T2DM and grade 1-3 obesity), and provided informed written consent. To ensure the integrity of biomarker assessment and cardiometabolic data, the study excluded pregnant women, individuals with acute infections, autoimmune disorders, or oncological conditions. Patients with hypothalamic-pituitary axis diseases, chronic kidney disease (GFR<35 mL/min/1.73 m²), or symptomatic hypertension were also excluded. Furthermore, the exclusion criteria covered patients who had experienced acute coronary syndrome or cerebrovascular events within the preceding six months, those with acute or exacerbated inflammatory conditions, and individuals with a history of psychiatric disorders or substance abuse. Non-citizens of Ukraine and patients unlikely to follow the research protocol were not enrolled.
Lipid profile evaluation, including total cholesterol (TC) and high-density lipoprotein cholesterol (HDL-C), was conducted using the peroxidase technique with Cholesterol Liquicolor reagents (Human, Germany) in heparin-stabilized serum. Triglyceride (TG) concentrations were measured via an enzymatic colorimetric method (Triglycerides 105 GPO, Human, Germany). The atherogenic coefficient (AC), very low-density lipoprotein cholesterol (VLDL-C), and low-density lipoprotein cholesterol (LDL-C) were calculated using standard formulas:
AC = (TC – HDL-C)/HDL-C (2)
VLDL-C = TG/2.2 × 0.45, (mmol/L) (3)
LDL-C = TC – (VLDL-C + HDL-C), (mmol/L) (4)
Serum GAS6 levels were quantified using an enzyme-linked immunosorbent assay (ELISA) with a commercial kit (Cusabio, USA) on a Labline-90 immunoenzymatic analyzer (Austria Lab Technologies). All laboratory tests were performed at the Central Research Laboratory of Kharkiv National Medical University.
Qualitative data are presented as absolute numbers and percentages (n, %). The comparison methods for quantitative data included Student's t-test or Mann-Whitney test; for qualitative data the χ² (Сhi-square) test was used. Statistical data processing was performed using parametric statistics methods with Microsoft Excel 2010 (Licence: Microsoft 365 Subscription 16.104.1 (26010228)). The normality of the distribution of quantitative variables was assessed using the Kolmogorov–Smirnov criterion. All normally distributed data are presented as M±SD (mean ± standard deviation). The comparison of mean values was performed using Fisher's criterion (F). Statistical analysis was performed using Spearman's correlation coefficient to evaluate the relationship between GAS6 and lipid profile parameters. To determine the potential prognostic value of GAS6 and its effectiveness in risk stratification, ROC (Receiver Operating Characteristic) analysis was conducted. The critical level of significance was set at p<0.05 [10].
The study was approved by the Ethics and Bioethics Committee of Kharkiv National Medical University (Protocol No. 2, dated 12.10.2022). All research procedures were conducted in strict accordance with international bioethical standards, including the Declaration of Helsinki and the UNESCO Universal Declaration on Bioethics and Human Rights. All patients provided their voluntary written informed consent to participate in the study.
RESULTS AND DISCUSSION
The evaluation of lipid profile parameters and serum GAS6 concentrations across the study cohorts demonstrated substantial variations. These findings strongly correlate with the progressive decline in patients' metabolic stability. A detailed overview of the metabolic parameter dynamics and GAS6 levels, highlighting the statistical significance of these shifts, is consolidated in Table.
Indicator, Patients with CHF control group CAD+T2DM+ obesity (n=75) CAD+ CAD+obesity (n=50) CAD without BMI, kg/m2 36.70±18.01 24.30±10.25 38.40±9.40 22.60±8.27 23.10±6.74 p1-2 <0.05 p2-3 <0.05 p2-4 >0.05 p2-5 >0.05 p1-3 >0.05 p3-4 <0.05 p3-5 <0.05 p1-4 <0.05 p4-5 >0.05 p1-5 <0.05 TC, mmol/l 6.41±0.69 5.38±0.49 5.42±0.78 5.29±0.64 3.72±0.60 p1-2 <0.05 p2-3 >0.05 p2-4 >0.05 p2-5 <0.001 p1-3 <0.05 p3-4 >0.05 p3-5 <0.001 p1-4 <0.05 p4-5 <0.001 p1-5 <0.001 TG, mmol/l 2.84±0.61 1.81±0.57 1.91±0.64 1.44±0.35 1.31±0.16 p1-2 <0.05 p2-3 >0.05 p2-4 <0.05 p2-5 <0.05 p1-3 <0.05 p3-4 <0.05 p3-5 <0.05 p1-4 <0.05 p4-5 <0.05 p1-5 <0.001 HDL-С, mmol/l 1.15±0.26 1.77±0.28 1.74±0.21 2.47±0.49 2.86±0.27 p1-2 <0.05 p2-3 >0.05 p2-4 <0.05 p2-5 <0.05 p1-3 <0.05 p3-4 <0.05 p3-5 <0.05 p1-4 <0.05 p4-5 <0.05 p1-5 <0.001 LDL-С, mmol/l 4.68±0.43 2.74±0.28 2.94±0.42 2.35±0.28 0.82 ± 0.16 p1-2 <0.001 p2-3 >0.05 p2-4 <0.05 p2-5 <0.001 p1-3 <0.001 p3-4 <0.05 p3-5 <0.001 p1-4 <0.001 p4-5 <0.001 p1-5 <0.001 VLDL-C, mmol/l 0.58±0.43 0.37±0.28 0.39±0.21 0.30±0.28 0.16±0.22 p1-2 <0.05 p2-3 >0.05 p2-4 <0.05 p2-5 <0.05 p1-3 <0.05 p3-4 <0.05 p3-5 <0.05 p1-4 <0.05 p4-5 <0.05 p1-5 <0.001 AC 4.57±0.35 2.04±0.35 2.15±0.49 1.14±0.42 0.51±0.22 p1-2 <0.001 p2-3 >0.05 p2-4 <0.001 p2-5 <0.001 p1-3 <0.001 p3-4 <0.001 p3-5 <0.001 p1-4 <0.001 p4-5 <0.001 p1-5 <0.001 GAS6, ng/ml 31.64±18.71 24.95±10.11 26.98±12.52 23.87±14.50 19.03±7.07 p1-2 ˂ 0.05 p2-3 >0.05 p2-4 >0.05 p2-5 =0.003 p1-3 ˂0.05 p3-4 ˂0.05 p3-5 <0.001 p1-4 ˂0.05 p4-5 <0.05 p1-5 <0.001
units
Measurement
(n=30)
T2DM (n=50)
metabolic pathology (n=50)
The most pronounced disturbances in the blood lipid spectrum were observed in patients of the main group (Group 1), where the combination of CAD with T2DM and obesity led to significant metabolic destabilisation. In particular, the TC level in patients of this group exceeded the control group indicators by 72.3% (p<0.001) and was also significantly higher than the levels in patients with CAD and T2DM by 19.1% and CAD with obesity by 18.3% (p<0.05).
Compared to the Group 4 (with isolated CAD) and the control group, the lipid profile indicators in the main group changed as follows: there was an increase in TG concentrations by almost 2.0 and 2.2 times (p<0.001), LDL-C content by 2.0 and 5.7 times (p<0.001), VLDL-C by 1.93 and 3.6 times (p<0.001), and CA by 4.0 times and 9.0 times, respectively. At the same time, the level of HDL-C was significantly lower by 53.4% compared to patients with isolated CAD and by 59.8% compared to healthy volunteers (p<0.001).
Among patients with CAD and concomitant T2DM (Group 2), a significant increase in TC levels by 44.6% was observed compared to the control group (p<0.001). Compared to patients with isolated CAD and the control group, the indicators changed as follows: TG increased by 25.7% and 38.2% (p<0.05), LDL-C – by 16.6% (p<0.05) and 3.3 times (p<0.001), VLDL-C – by 23.3% (p<0.05) and 2.3 times (p<0.001), and AC – by 78.9% and 4.0 times, respectively, as well as a decrease in HDL-C by 28.3% and 38.1% (p<0.05).
Patients with CHF against the background of CAD and concomitant obesity (Group 3) also showed a significant increase in TG levels by 32.6% and 45.8%, LDL-C – by 25.1% and 3.6 times, VLDL-C – by 30.0% and 2.4 times, and AC – by 88.6% and 4.2 times, as well as a decrease in HDL-C concentration by 29.6% and 39.2% compared to patients with isolated CAD and the control group, respectively (p<0.05).
It should be noted that no lipid profile parameters showed significant changes between patients with CAD and concomitant T2DM and patients with CAD and obesity (p>0.05). These results can be explained by common mechanisms of insulin resistance in both obese patients and patients with T2DM, which is a key mechanism of dyslipidaemia. Systemic inflammation also has a significant impact, affecting lipid metabolism and contributing to the progression of atherosclerosis.
Analysis of serum GAS6 protein levels revealed the greatest increase in patients with combined cardiometabolic pathology (Group 1), where its concentration exceeded that in Groups 2, 3, and 4 by 26.8%, 17.3%, 32.5% (p<0.05) and 66.3% (p<0.001), respectively, compared to Groups 2, 3, 4 and the control group, respectively. The content of this protein in patients with CAD and obesity was significantly higher compared to patients with isolated CAD without metabolic pathology by 13.0% (p<0.05) and the control group by 41.8% (p<0.001). At the same time, no significant differences in GAS6 levels were found between Group 2 and Group 4, as well as between Group 2 and Group 3 (p>0.05). However, the GAS6 level in Group 2 was significantly higher than that in the control group by 31.1% (p=0.003). The data obtained indicate the cumulative effect of combined metabolic conditions on the activation of GAS6 protein, which is a mediator of inflammation and fibrosis.
We examined the correlations between serum GAS6 levels, lipid profile parameters, and BMI in patients with CAD comorbid with T2DM and obesity. For this analysis, the critical value of the Spearman rank correlation coefficient was established at rcrit =0.39 (p<0.05). The resulting correlation matrix is illustrated in Figure 1.
Strong positive correlations were found with BMI (r=0.68; p<0.05), LDL-C (r=0.54; p<0.05) and VLDL-C (r=0.51; p<0.05) and moderate direct correlations with TG (r=0.47; p<0.05), indicating that as serum GAS6 levels increase in this cohort of patients, the most atherogenic lipid metabolism fractions increase proportionally. We also found weak direct correlations with TC (r=0.31; p>0.05), HDL-C (r=-0.26; p>0.05), and AC (r=0.11; p>0.05), which did not reach the level of significance.
When analyzing the data obtained in a group of patients with CAD against the background of concomitant T2DM (Fig. 2), moderate positive correlations were found with LDL-C (r=0.48; p<0.05) and VLDL-C (r=0.52; p<0.05). We also found weak direct correlations with BMI (r=0.31; p>0.05), total cholesterol (r=0.19; p>0.05), HDL cholesterol (r=-0.09; p>0.05), and CA (r=0.24; p>0.05), which did not reach the level of significance.
When analyzing the data obtained in the group of patients with ischemic heart failure against the background of concomitant obesity, reliable positive correlations of moderate strength with BMI (r=0.54; p<0.05), LDL-C (r=0.53; p<0.05) and VLDL-C (r=0.54; p<0.05) and weak correlations with TC (r=0.38; p>0.05), HDL-C (r=-0.24; p>0.05), CA (r=0.31; p>0.05), which did not reach the level of significance. The data are presented in Figure 3.
In the group of patients with CHF and CAD without concomitant metabolic pathology (Fig. 4), significant direct correlations of moderate strength were found with LDL-C (r=0.42; p<0.05) and VLDL-C (r=0.46; p<0.05). Weak direct correlations were also found with BMI (r=0.31; p>0.05), TC (r=0.28; p>0.05), HDL-C (r=-0.14; p>0.05), CA (r=0.24; p>0.05), which did not reach the level of significance.
Thus, the established relationship between elevated GAS6 levels in blood serum and the severity of atherogenic dyslipidaemia confirms that this protein may act as an important biochemical mediator that reflects the degree of metabolic disorders and, presumably, exacerbates the processes of atherosclerosis progression and myocardial remodelling, while the link with BMI indicates that GAS6 protein activation is closely associated with excess body weight and obesity and reflects the severity of metabolic dysfunction directly related to the volume of adipose tissue.
GAS6 protein demonstrated high independent prognostic performance, with a sensitivity of 91.1% and a specificity of 86.4% (data are presented in Fig. 5). This indicator was found to have significant prognostic value on its own and was subsequently included in a mathematical model for predicting the worsening of the functional class of CHF in patients with concomitant metabolic pathology. GAS6 serves as a robust biomarker reflecting the processes of systemic inflammation and myocardial remodeling, providing an optimal balance between the identification of high-risk patients and the minimization of false-positive results.
The results obtained, demonstrating the cumulative effect of comorbid cardiometabolic pathology on the activation of GAS6 protein and its close relationship with atherogenic dyslipidaemia, are consistent with current global trends in the study of the cardiometabolic continuum and the role of vitamin K-dependent proteins in its progression.
Global literature data position GAS6 as a key ligand of the TAM (Tyro3, Axl, MerTK) receptor family, which is a critical mediator in response to inflammation, fibrosis, and cellular homeostasis disorders in the cardiovascular system. In particular, studies by Chen J. et al. [11] and McShane L. et al. [12] confirm that increased expression of the GAS6-Axl signalling pathway plays a central role in myocardial fibrosis and vascular remodelling, especially against the background of metabolic dysfunction. The dominant activation of GAS6 in patients with CAD and concomitant metabolic pathology, as well as a significant increase in its content in the group of patients with only concomitant T2DM or obesity, emphasises that each of these comorbid conditions is an independent and significant stimulus for the activation of GAS6, and their combination leads to the maximum effect. This hypothesis is confirmed by the strong positive correlation between GAS6 and BMI in patients with combined pathology, which directly associates protein activation with the volume of dysfunctional adipose tissue and chronic systemic inflammation characteristic of obesity, as shown in earlier works by Wu K-S et al. [13] and recent studies by Su S-C. et al. [14]. Moreover, the established reliable correlations between GAS6 and proatherogenic fractions of lipid metabolism indicate that GAS6 is not just a marker, but an important signalling protein that reflects the degree of dyslipidaemia and is actively involved in the progression of atherosclerosis. This involvement of GAS6 in the progression of atherosclerosis and plaque instability through its effect on endothelial cells and macrophages is widely covered in the works of Prouse T. et al. [15] and Lutgens E. et al. [16]. Thus, the data obtained allow us to consider GAS6 as an integral prognostic biomarker that reflects the degree of convergence of metabolic and cardiac damage and can be used for more accurate risk stratification in patients with ischemic heart failure against the background of comorbid metabolic conditions.
Prospects for further research. A promising area of current research is the assessment of the prognostic effectiveness of GAS6 in dynamics, namely its ability to predict the development of major cardiovascular events and the progression of chronic heart failure.
CONCLUSIONS
1. Serum GAS6 protein levels exhibit a cumulative growth pattern proportional to the severity of comorbid metabolic disorders, reaching a maximum in patients with combined coronary artery disease, type 2 diabetes mellitus, and obesity (66.3% higher than control; p<0.001). This identifies GAS6 as a key molecular marker of exacerbated inflammation and myocardial remodeling in conditions of triple comorbidity.
2. Significant positive correlations with body mass index (r=0.68; p<0.05), triglyceride levels (r=0.54; p<0.05), and low-density lipoprotein cholesterol (r=0.58; p<0.05) prove that GAS6 activation is a direct reflection of metabolic dysfunction and dyslipidemia severity. This confirms its role in the accelerated progression of atherosclerosis in patients with excess body weight.
3. The presence of either type 2 diabetes mellitus or obesity alone significantly increases GAS6 levels (by 31.1% and 41.8% respectively vs control; p<0.05), characterizing GAS6 as a sensitive diagnostic and prognostic marker for early stratification of cardiac risk in patients with ischaemic-origin chronic heart failure and metabolic disorders.
Contributors:
Borovyk K.M. – methodology, resources, investigation, data curation, writing – original draft;
Kravchun P.G. – conceptualization, writing – review & editing;
Kadykova O.I. – methodology, writing – review & editing;
Babadzhan V.D. – data curation, visualization.
Funding. This research received no external funding.
Conflict of interests. The authors declare no conflict of interest.
REFERENCES
1. Savarese G, Becher PM, Lund LH, Seferovic P, Rosano GMC, Coats AJS. Global burden of heart failure: a comprehensive and updated review of epidemiology. Cardiovasc Res. 2023;118(17):3272-3287. doi: https://doi.org/10.1093/cvr/cvac013
2. Al-Tamimi MA, Gillani SW, Abd Alhakam ME, Sam KG. Factors Associated With Hospital Readmission of Heart Failure Patients. Front Pharmacol. 2021;12:732760. doi: https://doi.org/10.3389/fphar.2021.732760
3. Yao YS, Li TD, Zeng ZH. Mechanisms underlying direct actions of hyperlipidaemia on myocardium: an updated review. Lipids Health Dis. 2020;19(1):23. doi: https://doi.org/10.1186/s12944-019-1171-8
4. Manfioletti G, Brancolini C, Avanzi G, Schneider C. The protein encoded by a growth arrest-specific gene (Gas6) is a new member of the vitamin K-dependent proteins related to protein S, a negative coregulator in the blood coagulation cascade. Mol Cell Biol. 1993;13(8):4976-85. doi: https://doi.org/10.1128/mcb.13.8.4976
5. Rothlin CV, Carrera-Silva EA, Bosurgi L, Ghosh S. TAM receptor signalling in immune homeostasis. Annu Rev Immunol. 2015;33:355-91. doi: https://doi.org/10.1146/annurev-immunol-032414-112103
6. Bellan M, Quaglia M, Nerviani A, et al. Increased plasma levels of Gas6 and its soluble tyrosine kinase receptors Mer and Axl are associated with immunological activity and severity of lupus nephritis. Clin Exp Rheumatol. 2021;39(1):132-38. doi: https://doi.org/10.55563/clinexprheumatol/xyylza
7. Pagani S, Bellan M, Mauro D, et al. New insights into the role of Tyro3, Axl, and Mer receptors in rheumatoid arthritis. Dis Markers. 2020;2020:1614627. doi: https://doi.org/10.1155/2020/1614627
8. Yin Z, Nie X, Li T, et al. Detection of Gas6/AXL complex and its expression changes in patients with ST-segment elevation myocardial infarction. Front Med (Lausanne). 2025;12:1653708. doi: https://doi.org/10.3389/fmed.2025.1653708
9. Shan S, Liu Z, Guo T, et al. Growth arrest-specific gene 6 transfer promotes mesenchymal stem cell survival and cardiac repair under hypoxia and ischaemia via enhanced autocrine signalling and paracrine action. Arch Biochem Biophys. 2018;660:108-20. doi: https://doi.org/10.1016/j.abb.2018.10.016
10. Ivanchuk MA. [Statistical analysis in medical research]. [Internet]. Chernivtsi: Bukovynskyi derzhavnyi medychnyi universytet; 2022 [cited 2025 Mar 20]. 121 p. Ukrainian. Available from: https://dspace.bsmu.edu.ua/bitstream/123456789/19936/1 /456_Ivanchuk.pdf
11. Chen J, Wang Y, Li X, Guo X, Tian J, Zheng X, et al. IDHP Mitigates LPS-Induced Cardiomyocyte Injury via the GAS6/Axl-AMPK Axis: A Multi-Target Strategy Counteracting Inflammation, Oxidative Stress, and Apoptosis. Pharmaceuticals. 2025;18(8):1188. doi: https://doi.org/10.3390/ph18081188
12. McShane L, Tabas I, Lemke G, Kurowska-Stolarska M, Maffia P. TAM receptors in cardiovascular disease. Cardiovasc Res. 2019;115(8):1286-95. doi: https://doi.org/10.1093/cvr/cvz100
13. Wu K-S, Hung Y-J, Lee C-H, Hsiao F-C, Hsieh P-S. The Involvement of GAS6 Signaling in the Development of Obesity and Associated Inflammation. Int J Endocrinol. 2015:2015:202513. doi: https://doi.org/10.1155/2015/202513
14. Su S-C, Chiang C-F, Hsieh C-H, Lu G-H, Liu J-S, Shieh Y-S, et al. Growth arrest-specific 6 modulates adiponectin expression and insulin resistance in adipose tissue. J Diabetes Investig. 2021 Apr;12(4):485-92. doi: https://doi.org/10.1111/jdi.13412
15. Prouse T, Majumder S, Majumder R. Functions of TAM Receptors and Ligands Protein S and Gas6 in Atherosclerosis and Cardiovascular Disease. Int J Mol Sci. 2024;25(23):12736. doi: https://doi.org/10.3390/ijms252312736
16. Lutgens E, Tjwa M, Garcia de Frutos P, Wijnands E, Beckers L, Dahlbäck B, et al. Genetic loss of Gas6 induces plaque stability in experimental atherosclerosis. J Pathol. 2008 Sep;216(1):55-63. doi: https://doi.org/10.1002/path.2381
Key words: dyslipidemia, insulin resistance, coronary artery disease, prostate cancer survivors, statin-intolerance, ursodeoxycholic acid
Ключові слова: дисліпідемія, інсулінорезистентність, ішемічна хвороба серця, пацієнти, що вижили після раку передміхурової залози, непереносимість статинів, урсодезоксихолева кислота
Abstract
Numerous studies suggest an increased frequency of dyslipidemia and metabolic disorders in patients with prostate adenocarcinoma. The aim was to evaluate lipid profile, insulin resistance level in men with coronary artery disease and concomitant prostate cancer and impact of ursodeoxycholic acid on these indicators in complex therapy. Study included 48 men with coronary artery disease and prostate adenocarcinoma. The lipid profile, insulin resistance, testosterone level were determined in all of patients. The level of insulin, C-reactive protein were determined by immune-enzyme analysis. 1st group (n=22) was made up by statin-intolerant patients treated with ursodeoxycholic acid during 60 days in addition to standard therapy; 2nd group (n=26) – by statin-intolerant patients treated with standard regimen. The levels of triglycerides, low density lipoprotein-cholesterol and apolipoprotein-B in men with coronary artery disease and prostate adenocarcinoma were significantly higher than those in control group (p<0.001). The complex therapy with ursodeoxycholic acid resulted in significant decrease in the level of total cholesterol by 17.6% (p<0.001), triglycerides by 21.6% (p<0.001), low density lipoprotein-cholesterol by 25.2% (p<0.001), apolipoprotein-B by 12.9% (p<0.001), HOMA index level by 19.4% (p=0.001), median insulin level by 22.9% (p=0.002). Men with coronary artery disease and concomitant prostate cancer are characterized by increased levels of triglycerides, low density lipoprotein-cholesterol, insulin resistance and decreased apolipoprotein-B associated with low testosterone level. Complex treatment with ursodeoxycholic acid in these patients contributed to significant lipid level improvement and additional decrease of insulin resistance.
Реферат
Метаболічні зміни в чоловіків з ішемічною хворобою серця і супутнім раком передміхурової залози та можливості їх корекції в пацієнтів з непереносимістю статинів. Курята О.В., Сіренко О.Ю. Численні дослідження свідчать про підвищену частоту дисліпідемії та метаболічних порушень у пацієнтів з аденокарциномою простати. Метою дослідження було оцінити ліпідний профіль, рівень інсулінорезистентності в чоловіків з ішемічною хворобою серця та аденокарциномою простати та вплив урсодезоксихолевої кислоти на ці показники в комплексній терапії. У дослідженні взяли участь 48 чоловіків з ішемічною хворобою серця та аденокарциномою простати. У всіх пацієнтів визначали ліпідний профіль, інсулінорезистентність, рівень тестостерону. Рівень інсуліну, С-реактивного білка визначався за допомогою імуноферментного аналізу. 1-шу групу (n=22) склали пацієнти з непереносимістю статинів, які отримували урсодезоксихолеву кислоту протягом 60 днів як доповнення до стандартної терапії; 2-гу групу (n=26) – пацієнти з непереносимістю статинів, які отримували стандартний режим лікування. Рівні тригліцеридів, холестерину ліпопротеїнів низької щільності та аполіпопротеїну-B у чоловіків з ішемічною хворобою серця та аденокарциномою передміхурової залози були достовірно вищими, ніж у контрольній групі (p<0,001). Комплексна терапія із включенням урсодезоксихолевої кислоти привела до достовірного зниження рівня загального холестерину на 17,6% (p<0,001), тригліцеридів на 21,6% (p<0,001), холестерину ліпопротеїнів низької щільності на 25,2% (p<0,001), аполіпопротеїну-B на 12,9% (p<0,001), рівня індексу HOMA на 19,4% (p=0,001), інсуліну на 22,9% (p=0,002). Чоловіки з ішемічною хворобою серця та аденокарциномою простати характеризуються підвищеним рівнем тригліцеридів, холестерину ліпопротеїнів низької щільності, інсулінорезистентністю та дефіцитом аполіпопротеїну-B, що асоціюється з низьким рівнем тестостерону. Комплексне лікування із включенням урсодезоксихолевої кислоти в цих пацієнтів сприяло достовірному поліпшенню показників ліпідного профілю та додатковому зменшенню рівня інсулінорезистентності.
Cardiovascular diseases (CVD) and oncological diseases continue to be the main causes of mortality worldwide. Improvements in cancer survival have led to greater number of successfully treated patients with an increased mortality from cardiovascular diseases and their complications [1].
Prostate cancer (PC) is associated with increasing incidence rates worldwide and it is the second most common cancer in men [3]. Coronary Artery Disease (CAD) is prevalent and one of the leading cause of mortality in men with prostate cancer [2]. Increasing evidence of overlapping risk factors for cancer and cardiovascular disease in patients with PC represents a relevance of the cardio-oncological subspecialty for optimization of survivorship outcomes [4].
Numerous studies suggest an increased frequency of cardiovascular diseases and metabolic disorders in patients with prostate adenocarcinoma [5, 6], therefore, correction of risk factors is relevant, especially of dyslipidemia and insulin resistance (IR) [7, 11]. As known, the main pharmacological agents for treatment of dyslipidemia are statins [8, 21]. However, treatment with statins not always leads to achievement of lipid level targets, especially triglycerides [12]. According to literary data, up to 29% of patients report adverse musculoskeletal effects that limit using statins or their guideline-recommended doses [25]. Limitations of using statins for patients with cancer demonstrate conflicting results, increased muscle loss in some models, increased risk of muscle pain in elderly patients and drug interactions [22]. Therefore, in recent years, there has been active interest in other groups of lipid-lowering drugs. Thus, latest trials have shown bempedoic acid efficacy in lowering LDL cholesterol and its ability to reduce cardiovascular events in statin-intolerant patients [23], but has limited data for cancer patients, though ongoing research [26].
In recent literature, increasing attention is being paid to the possibilities of using ursodeoxycholic acid (UDCA) in patients with cancer [9]. It was found, that UDCA can protect epithelial cells from damage and apoptosis, while suppressing the proliferation and induction of apoptosis of cancer cells, including in prostate adenocarcinoma. Therefore, there is evidence that UDCA has a positive effect on the treatment of cancer patients, in particular, with hepatotoxicity caused by chemotherapy [13]. Interestingly, that UDCA has some hypocholesterolemic effect, reduces cholesterol synthesis by decreasing bile secretion and inhibiting the absorption of cholesterol in the intestine [10].
Thus, the purpose of the present study was to evaluate lipid profile, insulin resistance level in men with coronary artery disease after prostate cancer treatment and impact of UDCA on these indicators in complex therapy.
MATERIALS AND METHODS OF RESEARCH
The present study was conducted according to the Helsinki declaration principles and was approved by the Biomedical Ethics Commission of the Dnipro State Medical University (protocol No. 24 dated 01/15/25). All participants of research gave informed written consent. Dynamic observation and treatment was performed in 48 men with CAD with concomitant prostate adenocarcinoma (stages I-IIІ) at the age of 45 to 75 years (the main group). The baseline characteristics of patients have been demonstrated in the Table 1.
All patients had verified CAD according to the guidelines of the European Society of Cardiology, the diagnosis of prostate cancer was confirmed by a biopsy. Аll patients received standard treatment of CAD but stopped taking statins due to side effects or refused to take them. The inclusion criteria were: men aged 45-75 years, verified diagnosis of CAD and prostate cancer (stages I-IIІ), completed course of anticancer therapy by the doctor's decision (due to unacceptable toxicity) or the patient's refusal more than 6 months ago, consistently selected cardiologic treatment for the last 3 months, voluntary informed consent to participate in the study.
The presence of CAD was assessed based on documented cardiovascular disease, such as a history of myocardial infarction, angiographically confirmed coronary artery stenosis, and a history of coronary artery revascularization procedures.
According to magnetic resonance imaging (MRI) data, 40 (83,3%) of patients had tumors localized to the prostate gland without extracapsular extension (T1c-T2b), while 8 (16,7%) had tumors of a higher grade (T3a-T3b).
Exclusion criteria from the study were: age over 75 years; previous therapy with statins within the last 3 months, arrhythmias that cause hemodynamic disturbances and require correction with antiarrhythmic agents (including high gradations of ventricular arrhythmias, atrial flutter, paroxysmal tachycardias, sinus node weakness syndrome, atria-ventricular block 2-3 degrees), acute myocardial infarction, acute cerebrovascular accident, diabetes, hyper- and hypothyroidism with thyroid stimulating hormone (TSH) levels >4 mU/l, chronic kidney insufficiency (glomerular filtration rate (GFR) <30 ml/min/1.73 m2), acute heart failure, obesity with grade 4, cachexia.
Characteristic Men with coronary artery disease after prostate cancer (n=48) Control group (n=31) p Median of age, years 67 [56.8; 72.7] 65.4 [57.4; 74.2] 0.651 Median duration of CAD, years 9.8 [7.6; 10.4] 9.5 [7.5; 9.7] 0.143 Glomerular filtration rate (GFR), ml / (min · 1.73 m2) 76 [63; 79] 78 [63.8; 81.2] 0.177 Patients with stable angina, % 64.6 54.8 0.461 Patients with previous MI, % 29.2 29.0 0.214 Patients with hypertension, % 85.4 80.6 0.614 Median of ejection fraction, % 62.8 [51.4; 68.4] 65.1 [52.6; 69.6] 0.158 Patients, received cardiology treatment (%): ACE inhibitors/ACE receptors blockers 79.2 77.4 0.122 aldosterone antagonists 75.0 67.7 0.092 β-blockers 79.2 80.6 0.266 calcium antagonists 72.9 61.3 0.347 antiplatelet agents 68.8 67.7 0.284 diuretics 54.2 48.4 0.521
Patients were blindly divided into two groups: I group (n=22) – patients with CAD and prostate cancer treated with UDCA (Ursofalk, Dr. Falk Pharma GmbH, Germany) during 60 days in addition to standard therapy. The dose was calculated individually – 15 mg/kg. Group II (n=26) – patients who were treated with standard regimen without agreement on UDCA therapy. The control group consisted of 31 men with CAD without prostate cancer, comparable in age, cardiovascular risk profile, obtained by treatment of CAD.
At the initial state, the patients of both groups were comparable in terms of the main disease, indicators of age, duration of the disease, level of GFR, low-density lipoprotein cholesterol (LDL-C), high-density lipoprotein cholesterol (HDL-C), triglycerides (TG), systolic and diastolic blood pressure, heart rate.
All the patients were examined by physician, laboratory and instrumental methods at the beginning and to the end of the study were used. The patients were observed in outpatient department. The standard clinical and biochemical laboratory tests, blood tests for detection of total cholesterol (TC), TG, LDL-C, HDL-C, apolipoprotein А (Аpо-А1), apolipoprotein В (Аpо-В) [28], serum insulin [29] were performed. Tolerability of the drug was determined on the basis of an assessment of laboratory parameters (the level of ALT, AST in the serum), the level of GFR, the incidence of adverse reactions. GFR was determined by the formula CKD-EPI [30], IR – by the formula HOMA [14].
In order to evaluate the state of androgen deficiency the testosterone level was determined by the method of immunoenzymatic analysis with the reagent test kit “AccuBind ELISA”, androgen deficiency were established in case of total testosterone level below 2.5 ng/ml.
Statistical processing of the obtained results was performed using the licensed program STATISTICS 12.0 (StatSoft Inc, USA, trial version). Non-parametric statistics were used [27]. The data was presented in the form of a median (Me) and the interquartile segment [25%; 75%]. Categorical data were presented as n (%) and were compared using Chi-squared test. For comparison of indicators in two independent groups, the Mann-Whitney U-test, the two-sided Fisher exact test, and the Wilcoxon test (W) were used to compare two dependent groups. Statistically significant differences in research results were determined at a level of p<0.05.
RESULTS AND DISCUSSION
The incidence of dyslipidemia was significantly higher in main group compared to control group (p< 0.001). The levels of TG, LDL-C and Apo-B in men with CAD and concomitant prostate cancer were significantly higher than those in control group (Table 2) (p< 0.001). Significant correlation relations between the testosterone level with TG, HDL-C, LDL-C, Apo-B were determined in men with CAD and concomitant prostate cancer – R= -0.58 (p<0.001), R=0.60 (p<0.05), R= -0.74 (p<0.001), R= -0.79 (p<0.001) respectively.
Parameter Men with CAD and prostate adenocarcinoma (n = 48) Men with CAD (n = 31) median [25%;75] (mmol/l) abnormal (n, %) median [25%;75] (mmol/l) abnormal (n, %) TC 6.12 [4.98;6.64] 34(70.80)* 5.78 [4.36;6.15] 16(51.6) TG 3.26 [2.68;3.89]** 38(79.17)* 1.56 [1.18;2.04] 12(38.71) HDL-C 1.43[1.15;1.79] 5(10.42) 1.50[1.10;1.68] 2(6.45) LDL-C 4.53[3.74;4.86]** 39(91.25)* 3.43[3.01;3.95] 20(64.52) Apo-A1 1.4[1.14;1.58] 8(16.67) 1.31[1.20;1.47] 5(16.13) Apo-B 1.88[1.62;2.09]** 25(52.08)* 1.22[1.03;1.54]* 7(22.58) Dyslipidemia, % – 42(87.50) * – 18(58.06) Notes: * – p<0.05; ** – p<0.001 comparison of lipid levels and dyslipidemia incidence between cancer patients and control group; TC: total-cholesterol; TG: triglyceride; HDL-C: high density lipoprotein-cholesterol; LDL-C: low density lipoprotein-cholesterol; Apo-A1: apolipoprotein-A1, Apo-B: apolipoprotein-B.
The level of insulin in patients with CAD and concomitant prostate cancer ranged from 10.7 to 25.9 MO/ml baseline, the median insulin level was 18.9 [11.3; 23.7] MO/ml, in the control group – ranged from 5.4 to 17.5 MO/ml baseline, the median insulin level was 10.8 [5.5; 13.4] MO/ml respectively (p<0.001). IR was established in 29 (60.42%) patients of main group and 13 (41.94%) of controls (p<0.05). Men with CAD and concomitant prostate cancer had significantly higher level of insulin, HOMA index compared with the control group (p<0.001). Correlation relations between the HOMA index with PSA, testosterone level, TG, LDL-C were determined in men with CAD after prostate adenocarcinoma treatment – R=0.65 (p<0.001), R= -0.68 (p<0.001), R=0.58 (p<0.05), R=0.63 (p<0.05) respectively.
The complex therapy with UDCA for patients with CAD and co-existent prostate adenocarcinoma resulted in a more significant reduction of the level of the pro-atherogenic fractions of blood lipids (р<0.01) (Table 3). Thus prescribing only standard therapy contributed to a significant decrease in the level of TC by 12.2% (p<0.001), TG by 18% (p<0.001), LDL-C by 20% (p<0.001), number of dyslipidaemia pts by 23.08% (p<0.001). On the other hand the complex therapy with UDCA resulted in a greater reduction of pro-atherogenic fractions of blood lipids: significant decrease in the level of TC by 17.6% (p<0.001), TG by 21.6% (p<0.001), LDL-C by 25.2% (p<0.001), number of dyslipidaemia pts by 31.82% (p<0.001) and additional significant decrease in the level of Apo B by 12.9% (p<0.001). The significant differences between Group I and II after observation were identified by LDL-C level (p<0.001). There were no significant differences between the levels of liver transaminases before and after observation period in all groups of pts (Table 3).
Lipid profile indicators Before treatment After treatment men with coronary artery disease after prostate cancer treatment (n=22) men with coronary artery disease after prostate cancer treatment -UDCA (n=26) men with coronary artery disease after prostate cancer treatment +UDCA (n=22) men with coronary artery disease after prostate cancer treatment -UDCA (n=26) TC, mmol/l 6.18 [4.88;6.52] 5.98 [4.76;6.45] 5.09 [4.18; 5.32]* 5.25 [4.18;5.54]* HDL-C, mmol/l 1.40[1.11;1.83] 1.46 [1.18;1.96] 1.48[1.15;1.89] 1.52 [1.25;2.10] LDL-C, mmol/l 4.56[3.74;4.88] 4.50[3.10;4.68] 3.41[3.14;3.65]* 3.60[2.60;4.15]** TG, mmol/l 3.24 [2.65;3.88] 3.33[3.01;3.95] 2.54 [1.48;3.09]* 2.73[2.31;3.34]* Apo-A1 1.42[1.16;1.59] 1.31[1.20;1.47] 1.42[1.15;1.60] 1.35[1.21;1.49] Apo-B 1.86[1.60;2.03] 1.79[1.53;2.14] 1.62[1.51;1.96]* 1.72[1.44;2.00] Dyslipidemia, % 22(100) 26(100) 15(68.18) * 20(76.92)* ALT, U/l 21 [14.78; 28.78] 19 [12.32; 26.75] 24.63 [15.36; 29.79] 22.61 [14.33; 27.77] AST, U/l 26.14 [16.29; 31.66] 24.54 [13.32; 29.71] 27.52 [17.31; 30.63] 25.51 [14.35; 28.69] Notes: * – p<0.05; ** – p<0.001 comparison of the status of lipidemia between groups; TC: total-cholesterol; TG: triglyceride; HDL-C: high density lipoprotein-cholesterol; LDL-C: low density lipoprotein-cholesterol; Apo-A1: apolipoprotein-A1; Apo-B: apolipoprotein-B; UDCA: ursodeoxycholic acid.
+UDCA
Analysis of the dynamics of the insulin level and insulin resistance on the background of treatment revealed significant differences in these indicators in patients of Group I and II (Fig. 1, 2). In the group of patients UDCA was included in the composition of complex therapy, the median insulin level and HOMA index decreased by 19.4% (p=0.001) and 22.9% (p=0.002), respectively, in the standard treatment group dynamics of these indicator were not significantly different. The inclusion of UDCA in the complex therapy contributed to a more pronounced decrease in insulin level and IR in men with androgen deficiency (Fig. 1, 2). There were no significant side effects with the inclusion of UDCA in the standard therapy in the dynamics of observation, and there was no need to change the daily dose or discontinue treatment. Thus, the results of the study indicate the effectiveness and safety of UDCA in complex treatment in men with CAD with concomitant prostate cancer.
Cancer and CVD are linked by multiple pathways and common risk factors. Thus, their combined treatment is a complex task and requires a multidisciplinary approach with the involvement both of cardiologists and oncologists [15].
Evidence for an association between TC, LDL-C, HDL-C, triglycerides with prostate cancer is conflicting. The retrospective cohort analysis of 843 patients with radical prostatectomy demonstrated association between elevated serum triglycerides with increased risk of prostate cancer recurrence [16]. Cholesterol of LDL-C, HDL-C were not associated with prostate cancer recurrence risk among all of analyzed population. At the same time, among men with prostate cancer and dyslipidemia, elevated total cholesterol and HDL-C levels were associated with increased and decreased risk of cancer recurrence, respectively [16]. Our results demonstrate that the presence of concomitant prostate adenocarcinoma in men with CAD was associated with significantly higher levels of TG, LDL-C and lower Apo-B and were correlated with androgen deficiency.
Thus in recent years a large number of studies suggest the role of lipid and glucose metabolism in the development of prostate cancer [17]. A recent meta-analysis showed a strong positive association between obesity and the risk of advanced prostate cancer. However, epidemiological data on the relationship between lifestyle risk factors (dyslipidemia, diabetes and IR) and the development and progression of prostate cancer remains inconclusive [17].
We provided evidence supporting a relationship of dyslipidemia, IR, and androgen deficiency in men with prostate cancer. Our findings showed a negative correlation between serum testosterone and TG, LDL‑C, serum insulin, and IR. Conversely, we found that HDL‑C, Apo-B was directly correlated with serum testosterone. It was concluded that low serum testosterone is associated with dyslipidemia and IR in men with CAD and prostate cancer. This could be explained by the sex hormone pathway in obesity [18].
Given that standard pharmacologic treatment may not be sufficient to achieve the recommended lipid target, an alternative treatment may be needed. The recent meta-analysis of randomized placebo-controlled trials demonstrated that ursodeoxycholic acid treatment might be an effective lipid-lowering agent with significant reduction in total cholesterol levels [19]. Thus, it was suggested that ursodeoxycholic acid can reduce cholesterol biosynthesis by reducing the activity of hydroxymethylglutaryl-coenzyme A-reductase and decreasing the intestinal absorption of cholesterol [19]. Ursodeoxycholic acid can also affect adipose tissue by lowering triglyceride levels and increasing esterification and desaturation of fatty acids [20].
Our findings suggest that UDCA in complex treatment men with CAD and concomitant prostate cancer decreases pro-atherogenic lipids and IR level. Further investigation is required to elucidate if observed lipid and IR lowering effects of ursodeoxycholic acid in this patients can contribute to the prevention of cardiovascular events.
Limitations.
However, this study should be interpreted with several limitations. Therefore, only patients with CAD with prostate cancer were chosen for this study, and consequently the results can only be applied to this population. It could be perspectival to evaluate the hard end point with prolongation of this therapy.
CONCLUSIONS
1. The present study have demonstrated that men with coronary artery disease and concomitant prostate cancer are characterized by increased levels of triglycerides, low-density lipoprotein cholesterol, IR and decreased apolipoprotein В associated with low testosterone level.
2. Complex treatment with ursodeoxycholic acid in these patients contributed to significant lipid level improvement and additional decrease of insulin resistance.
Contributors:
Kuryata O.V. – conceptualization, methodology, writing – review & editing, project administration;
Sіrenko O.Yu. – methodology, formal analysis, resources, data curation, writing – original draft, investigation.
Funding. This research received no external funding.
Conflict of interests. The authors declare no conflict of interest.
REFERENCES
1. Estruch R, Ruilope LM, Cosentino F. The year in cardiovascular medicine 2020: epidemiology and prevention. European Heart Journal. 2021;42(8):813-21. https://doi.org/10.1093/eurheartj/ehaa1062">doi: https://doi.org/10.1093/eurheartj/ehaa1062
2. Ralapanawa U, Sivakanesan R. Epidemiology and the Magnitude of Coronary Artery Disease and Acute Coronary Syndrome: A Narrative Review. J Epidemiol Glob Health. 2021;11(2):169-77. doi: https://doi.org/10.2991/jegh.k.201217.001
3. Vieira Lima Aguiar Melão B, Pekala K, Matsoukas K, et al. SIU-ICUD: Epidemiology of Prostate Cancer. Soc Int Urol J. 2025;6(44). doi: https://doi.org/10.3390/siuj6030044
4. Sun L, Parikh RB, Hubbard RA, et al. Assessment and Management of Cardiovascular Risk Factors Among US Veterans With Prostate Cancer. JAMA Netw Open. 2021;4(2):e210070. doi: https://doi.org/10.1001/jamanetworkopen.2021.0070
5. Kuryata O, Sirenko O. The Influence of L-Carnitine in the Complex Treatment of Patients With Renal Dysfunction Who Have Synchronous Chronic Coronary Artery Disease and Prostate Adenocarcinoma. Turkiye Klinikleri J Med Sci. 2019;39(4):381-8. doi: https://doi.org/10.5336/medsci.2019-65452
6. Kuryata OV, Sirenko O, Tykhomyrov A, et al. Plasminogen activator inhibitor-1 and circulating ceruloplasmin levels in men with iron-deficiency anemia and heart failure with concomitant prostate cancer and their dynamics after treatment. Journal of Medical Sciences. 2022;42:72-80. doi: https://doi.org/10.4103/jmedsci.jmedsci_427_20
7. Kim TH, Lim DG, Chung HS, Chang Hwang E, Kang TW, Kwon DD, et al. The prevalence of dyslipidemia in patients with prostate cancer. Prostate Int. 2025;13(3):174-8. doi: https://doi.org/10.1016/j.prnil.2025.03.005
8. Mach F, Koskinas KC, Roeters van Lennep JE, Tokgözoğlu L, Badimon L, Baigent C, et al. 2025 Focused Update of the 2019 ESC/EAS Guidelines for the management of dyslipidaemias: Developed by the task force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and the European Atherosclerosis Society (EAS). European Heart Journal. 2025;46(42):4359-78. doi: https://doi.org/10.1093/eurheartj/ehaf190
9. Zhang H, Xu H, Zhang C, et al. Ursodeoxycholic acid suppresses the malignant progression of colorectal cancer through TGR5-YAP axis. Cell Death Discov. 2021;7(1):207. doi: https://doi.org/10.1038/s41420-021-00589-8
10. Lakić B, Škrbić R, Uletilović S, et al. Beneficial Effects of Ursodeoxycholic Acid on Metabolic Parameters and Oxidative Stress in Patients with Type 2 Diabetes Mellitus: A Randomized Double-Blind, Placebo-Controlled Clinical Study. J Diabetes Res. 2024 Feb 29;2024:4187796. doi: https://doi.org/10.1155/2024/4187796
11. Daniels JP, Hernández-Tirado A, Mirocha J, et al. Association between insulin resistance and prostate volume: A 4-year analysis from the Reduction by Dutasteride of Prostate Cancer (REDUCE) Trial. BJUI Compass. 2025;6(9):e70085. doi: https://doi.org/10.1002/bco2.70085
12. Morieri ML, Perrone V, Veronesi C, et al. Improving statin treatment strategies to reduce LDL-cholesterol: factors associated with targets’ attainment in subjects with and without type 2 diabetes. Cardiovasc Diabetol. 2021 Jul 16;20(1):144. doi: https://doi.org/10.1186/s12933-021-01338-y
13. Zeng H, Safratowich BD, Cheng W-H, et al. Ursodeoxycholic Acid Exhibits Greater Inhibitory Effects on Cancerous HCT116 Colon Cells than on Noncancerous NCM460 Colon Cells. Nutrients. 2025;17:1072. doi: https://doi.org/10.3390/nu17061072
14. Levey AS, Stevens LA. Estimating GFR using the CKD Epidemiology Collaboration (CKD-EPI) creatinine equation: more accurate GFR estimates, lower CKD prevalence estimates, and better risk predictions. Am J Kidney Dis. 2010;55(4):622-7. doi: https://doi.org/10.1053/j.ajkd.2010.02.337
15. Martín García A, Mitroi C, Mazón Ramos P, et al. Stratification and management of cardiovascular risk in cancer patients. A consensus document of the SEC, FEC, SEOM, SEOR, SEHH, SEMG, AEEMT, AEEC, and AECC. Rev Esp Cardiol (Engl Ed). 2021;74(5):438-48. doi: https://doi.org/10.1016/j.rec.2020.11.020
16. Khan A, Sarkar E, Chandra A, et al. Serum Insulin, Insulin-Like Growth Factor-1, Testosterone and Lipid Profile Levels in Benign Prostatic Hyperplasia and Prostate Cancer at Diagnosis. Cureus. 2024;16(12):e75342. doi: https://doi.org/10.7759/cureus.75342
17. Zhou Z, Huang Z, Zhao Y, et al. Association between low density lipoprotein cholesterol levels and prostate cancer risk in non-hypertensive middle-aged and older American men. Sci Rep. 2024;14:29096. doi: https://doi.org/10.1038/s41598-024-80190-y
18. Wittert G, Grossmann M. Obesity, type 2 diabetes, and testosterone in ageing men. Rev Endocr Metab Disord. 2022;23(6):1233-42.
doi: https://doi.org/10.1007/s11154-022-09746-5
19. Seo SH, Lee DH, Lee YS, Cho KJ, Park HJ, Lee HW, et al. Co-administration of ursodeoxycholic acid with rosuvastatin/ezetimibe in a non-alcoholic fatty liver disease model. Gastroenterology Report. 2022;10:goac037. doi: https://doi.org/10.1093/gastro/goac037
20. Oostveen RF, Kaiser Y, Hartgers ML, et al. Ursodeoxycholic Acid for Trans Intestinal Cholesterol Excretion Stimulation: A Randomized Placebo Controlled Crossover Study. J Am Heart Assoc. 2024;13(20):e035259. doi: https://doi.org/10.1161/JAHA.124.035259
21. Reiss AB, Vasalani S, Albert J, et al. The Effect of Androgen Deprivation Therapy on the Cardiovascular System in Advanced Prostate Cancer. Medicina. 2024;60:1727. doi: https://doi.org/10.3390/medicina60111727
22. Chou E, Legasto CS, Chin AK, et al. Statin Use in Patients With Cancer: Drug Interaction and Statin Usage. JACC Adv. 2025;4(11 Pt 1):102259. doi: https://doi.org/10.1016/j.jacadv.2025.102259
23. Xia X, Niu H, Xu C, Liu X, Zhang G, Ling J. Revisiting the metabolic crosstalk between type 2 diabetes and hyperuricemia: Pathophysiological insights and therapeutic perspectives. Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 2026;1872(2):168102. doi: https://doi.org/10.1016/j.bbadis.2025.168102
24. de Jesus M, Mohammed T, Singh M, et al. Etiology and Management of Dyslipidemia in Patients With Cancer. Front Cardiovasc Med. 2022;25(9):892335. doi: https://doi.org/10.3389/fcvm.2022.892335
25. Nissen SE, Lincoff AM, Brennan D, et al. Bempedoic Acid and Cardiovascular Outcomes in Statin-Intolerant Patients. N Engl J Med. 2023;388(15):1353-64. doi: https://doi.org/10.1056/NEJMoa2215024
26. Velez BC, Petrella CP, DiSalvo KH, et al. Combined inhibition of ACLY and CDK4/6 reduces cancer cell growth and invasion. Oncol Rep. 2023;49(2):32. doi: https://doi.org/10.3892/or.2022.8469
27. Makhanets L, Vinnychuk O, Hryhorkiv M. [Statistics: Laboratory Workshop in STATISTICA 12: Tutorial]. Chernivtsi: Chernivets nats un-t im. Yu. Fedkovycha; 2023. 161 р. Ukrainian.
28. Pancholia AK, Kabra NK, Gupta R. Laboratory evaluation of lipid parameters in clinical practice. Indian Heart J. 2024;76(Suppl 1):S29-S32. doi: https://doi.org/10.1016/j.ihj.2024.02.002
29. Gastaldelli A. Measuring and estimating insulin resistance in clinical and research settings. Obesity (Silver Spring). 2022;30(8):1549-63. doi: https://doi.org/10.1002/oby.23503
30. Kwok R, Kishore K, Zafari T, et al. Comparative performance of CKD-EPI equations in people with diabetes: An international pooled analysis of individual participant data. Diabetes Res Clin Pract. 2025;223:112104. doi: https://doi.org/10.1016/j.diabres.2025.112104
Ключові слова: Фламідез, диклофенак, люмбаго, люмбоішіалгія, ефективність, безпека, обсерваційне дослідження
Key words: Flamidase, diclofenac, lumbago, lumbosciatica, efficacy, safety, observational study
Реферат
Біль у поперековій ділянці (люмбалгія) посідає одне з провідних місць серед причин тимчасової непрацездатності в економічно активного населення в усьому світі, включаючи Україну. Нестероїдні протизапальні препарати на сьогодні залишаються препаратами першої лінії при лікуванні вертеброгенних больових синдромів, забезпечуючи анальгетичну та протизапальну дію, проте їх призначення обмежено гастропатіями. Фламідез – комбінований препарат на основі диклофенаку калію та парацетамолу, що містить також ензим серратіопептидазу. Така комбінація дозволяє досягати синергічного ефекту: парацетамол посилює анальгезивну дію диклофенаку калію, зменшуючи потребу в підвищенні дози нестероїдного протизапального препарату, а серратіопептидаза додатково чинить протизапальний та протинабряковий ефект. Метою роботи було оцінити ефективність та безпеку комбінованого лікарського засобу Фламідез (диклофенак калію, парацетамол, серратіопептидаза) порівняно з диклофенаком натрію при лікуванні гострого болю в нижній частині спини (люмбаго, люмбоішіалгія). Проведено порівняльне проспективне багатоцентрове обсерваційне дослідження за участі 157 пацієнтів з 15 регіонів України. Учасників було розподілено на 4 групи залежно від нозології та застосованого препарату: люмбаго-диклофенак (n=29), люмбоішіалгія-диклофенак (n=49), люмбаго-Фламідез (n=25), люмбоішіалгія-Фламідез (n=54). Ефективність оцінювали за динамікою больового синдрому з 1 до 7 дня лікування, безпеку – за активністю ферментів-трансаміназ (АЛТ, АСТ) у плазмі крові, а також суб’єктивними проявами побічних реакцій (нудота, біль у животі тощо). Як диклофенак натрію, так і Фламідез демонструють ефективність у зниженні інтенсивності болю в попереку, при цьому Фламідез значуще перевершує диклофенак за вираженістю та швидкістю розвитку анальгезивного ефекту (особливо при ноцицептивному компоненті). Середнє зменшення інтенсивності болю (ΔВАШ) за 7 днів лікування становило 5,76 бала в групі Фламідезу проти 4,12 бала в групі диклофенаку натрію, що є статистично значущим (p<0,05). У пацієнтів з люмбаго ΔВАШ становив 6,12 бала (Фламідез) проти 4,48 бала (диклофенак). У пацієнтів з люмбоішіалгією – 5,39 бала (Фламідез) проти 3,76 бала (диклофенак). Медіана ВАШ на 7-й день лікування: 0 балів у групі Фламідезу проти 2 балів у групі диклофенаку. У плані безпеки диклофенак натрію також дещо поступається Фламідезу, вірогідно (проте клінічно незначуще) збільшуючи активність АЛТ та АСТ, при цьому не було верифіковано статистично значущої різниці між препаратами за впливом на шлунок: побічні реакції з боку ШКТ спостерігались у 15% пацієнтів, які приймали диклофенак, і в 11%, які приймали Фламідез. Фламідез демонструє кращу за диклофенак натрію ефективність і безпеку при лікуванні гострого поперекового болю, особливо за наявності ноцицептивного компонента. Комбінована дія диклофенаку калію, парацетамолу та серратіопептидази забезпечує виражену анальгезивну дію, не створюючи при цьому додаткових гастральних та гепатобіліарних ризиків для пацієнта. Отримані результати свідчать, що комбінований препарат Фламідез може бути ефективним варіантом фармакотерапії гострого поперекового болю. Подальші рандомізовані контрольовані дослідження з більшим періодом спостереження необхідні для підтвердження цих результатів.
Abstract
Clinical efficacy and safety of Flamidase in the treatment of lumbar pain: results of a multicenter observational comparative study in Ukraine. Kononenko N.M., Tsyvunin V.V., Briukhanova T.O., co-authors (20)4. Pain in the lumbar region (lumbalgia) is one of the leading causes of temporary disability among the economically active population worldwide, including Ukraine. Nonsteroidal anti-inflammatory drugs remain the first-line treatment for vertebrogenic pain syndromes, providing analgesic and anti-inflammatory effects, but their use is limited by gastrointestinal disorders. Flamidase is a combination drug based on potassium diclofenac and paracetamol, which also contains the enzyme serratiopeptidase. This combination achieves a synergistic effect: paracetamol enhances the analgesic effect of potassium diclofenac, reducing the need to increase the dose of the nonsteroidal anti-inflammatory drug, while serratiopeptidase provides additional anti-inflammatory and anti-edema effects. The aim of the study was to evaluate the efficacy and safety of the combination drug Flamidase (potassium diclofenac, paracetamol, serratiopeptidase) compared to sodium diclofenac in the treatment of acute lower back pain (lumbago, lumbosciatica). A comparative prospective multicenter observational study was conducted involving 157 patients from 15 regions of Ukraine. Participants were divided into 4 groups depending on the nosology and the drug used: lumbago-Diclofenac (n=29), lumbosciatica-Diclofenac (n=49), lumbago-Flamidase (n=25), lumbosciatica-Flamidase (n=54). Efficacy was assessed based on the dynamics of pain syndrome from days 1 to 7 of treatment, safety was assessed based on the activity of transaminase enzymes (ALT, AST) in blood plasma, as well as subjective manifestations of side effects (nausea, abdominal pain, etc.). Both diclofenac sodium and Flamidase are effective in reducing the intensity of low back pain, with Flamidase significantly superior to diclofenac in terms of the severity and speed of the analgesic effect (especially in the nociceptive component). The average reduction in pain intensity (ΔVAS) over 7 days of treatment was 5.76 points in the Flamidase group versus 4.12 points in the diclofenac sodium group, which is statistically significant (p<0.05). In patients with lumbago, ΔVAS was 6.12 points (Flamidase) versus 4,48 points (diclofenac). In patients with lumbosciatica, it was 5.39 points (Flamidase) versus 3.76 points (diclofenac). The median VAS on the 7th day of treatment was 0 points in the Flamidase group versus 2 points in the diclofenac group. In terms of safety, diclofenac sodium is also slightly inferior to Flamidase, reliably (but clinically insignificantly) increasing ALT and AST activity, while no statistically significant difference between the drugs in terms of their effect on the stomach was verified: gastrointestinal side effects were observed in 15% of patients on diclofenac and 11% on Flamidase. Flamidase demonstrates better efficacy and safety compared to diclofenac sodium in the treatment of acute low back pain, especially in the presence of a nociceptive component. The combined action of potassium diclofenac, paracetamol, and seratopeptidase provides a pronounced analgesic effect without creating additional gastric and hepatobiliary risks for the patient. The results obtained indicate that the combination drug Flamidase may be an effective option for pharmacotherapy of acute low back pain. Further randomized controlled trials with a longer follow-up period are needed to confirm these results.
Біль у поперековій ділянці (люмбалгія) посідає одне з провідних місць серед причин тимчасової непрацездатності в економічно активного населення в усьому світі, включаючи Україну [1]. За даними Всесвітньої організації охорони здоров’я, до 80% людей хоча б раз у житті переживають епізод вираженого болю в попереку, що може мати як механічну, так і нейропатичну природу. Часті рецидиви, хронізація болю та пов’язане з цим зниження якості життя роблять проблему медико-соціальною та економічно значущою.
Найбільш поширеними клінічними формами гострого вертеброгенного болю є люмбаго (раптовий, гострий м’язово-зв’язковий біль у попереку, без іррадіації) та люмбоішіалгія (компресійно-нейропатичний біль з іррадіацією по ходу сідничного нерва), які часто асоціюються з міофасціальним синдромом, дегенеративно-дистрофічними змінами хребта, міжхребцевими грижами, фасетковим синдромом, спондилоартропатією та компресією корінців.
За даними Міністерства охорони здоров’я України та профільних інститутів, вертеброгенні больові синдроми посідають друге місце серед причин звернень до лікарів-неврологів, поступаючись лише судинним захворюванням мозку. Щороку понад 1,5 млн пацієнтів звертаються до медичних закладів із симптомами люмбалгії чи люмбоішіалгії [2].
Серед дорослого населення працездатного віку понад 40% осіб віком від 30 до 60 років повідомляють про епізоди болю в поперековій ділянці тривалістю понад 7 днів, а в 15-20% випадків цей біль рецидивує або хронізується [3]. Особливо тривожною є тенденція до зростання частоти первинної інвалідизації, спричиненої саме вертеброгенними ураженнями – до 5-6% щорічно.
За інформацією Національної служби здоров’я України (НСЗУ), у 2022 році понад 200 тисяч випадків було зареєстровано за кодами М54.3 (ішіас) та М54.5 (люмбалгія) згідно з МКХ-10. Ці показники значно зросли після пандемії COVID-19, що пов’язується з гіподинамією, порушенням постави при дистанційній роботі, зниженням фізичної активності населення.
Ураховуючи поліморфізм патогенезу, терапія потребує ретельного підбору фармакологічних засобів з урахуванням типу болю, тривалості та індивідуальних факторів ризику. У гострому періоді лікування основними завданнями є швидке та ефективне гальмування болю, зменшення запального процесу, нормалізація функціонального стану хребта, а також мінімізація ризику розвитку побічних реакцій фармакотерапії [4].
Нестероїдні протизапальні препарати (НПЗП) на сьогодні залишаються препаратами першої лінії при лікуванні вертеброгенних больових синдромів, забезпечуючи анальгетичну та протизапальну дію [5]. Диклофенак натрію залишається одним з найбільш поширених засобів цього фармакологічного класу завдяки доведеній ефективності в зменшенні інтенсивності болю та набряку [6]. Проте його призначення обмежене побічними діями, зокрема гастропатіями й гепатоксичністю [7, 8, 9, 10].
Останніми роками значну увагу привертають комбіновані препарати, зокрема Фламідез – комбінований препарат на основі диклофенаку калію та парацетамолу, що містить також ензим серратіопептидазу. Така комбінація дозволяє досягати синергічного ефекту: парацетамол посилює анальгезивну дію диклофенаку калію, зменшуючи потребу в підвищенні дози НПЗП, а серратіопептидаза додатково чинить протизапальний та протинабряковий ефект. Також диклофенак калію, що входить до складу Фламідезу, має доведені переваги над натрієвою сіллю диклофенаку у швидкості та вираженості ефекту. Існують також окремі дані щодо кращого профілю безпеки калієвої солі диклофенаку порівняно з натрієвою [11]. Серратіопептидаза при цьому є цінним ад’ювантом, що не лише вірогідно посилює знеболювальні та протизапальні властивості НПЗП, але й має потенціал до корекції можливих побічних ефектів диклофенаку [12, 13].
Фламідез продемонстрував високу клінічну ефективність при болю в спині, остеоартриті, міозитах, а також у лікуванні післяопераційного болю. За даними окремих досліджень, у пацієнтів, які отримували Фламідез, спостерігали не лише швидший знеболювальний ефект, але й також рідшу частоту виникнення побічних реакцій (у першу чергу диспептичних) [14].
Таким чином, комбіновані засоби на основі диклофенаку калію, такі як Фламідез, можуть становити альтернативу монотерапії класичними НПЗП, дозволяючи зменшити медикаментозне навантаження, особливо в пацієнтів із супутніми факторами ризику ураження шлунка та печінки.
Проте, незважаючи на широке застосування в клінічній практиці як монопрепаратів диклофенаку натрію, так і Фламідезу, порівняльна оцінка їхньої ефективності та безпеки для пацієнтів з гострим поперековим болем – як у контексті гастроінтестинальних ризиків, так і з урахуванням негативних впливів на функції печінки за змінами біохімічних маркерів аланінамінотрансферази (АЛТ) й аспартатамінотрансферази (АСТ) – залишається недостатньо дослідженою в українській популяції. Більшість наявних даних зосереджені на загальній ефективності знеболювання, тоді як фармакобезпека вивчена переважно на обмежених вибірках.
Зважаючи на вищезазначене, проведення багатоцентрового дослідження, спрямованого на порівняння ефективності та безпеки лікування Фламідезом та монотерапії диклофенаком натрію в пацієнтів з люмбаго та люмбоішіалгією, є актуальною, науково обґрунтованою та практично значущою задачею, що має важливе значення для оптимізації терапевтичних підходів у лікуванні вертеброгенних уражень та дозволить сформувати сучасні протоколи ефективної та безпечної терапії.
Сьогодні поняття «якість життя» є невід’ємною частиною системи охорони здоров’я, а також клінічних та медико-соціальних досліджень. У 1982 році Kaplan і Bush запровадили термін health-related quality of life (HRQoL – «якість життя, пов’язана зі здоров’ям»), що дозволило виділити параметри, які описують стан здоров’я, турботу про нього та якість медичної допомоги відповідно до загальної концепції якості життя [15].
Простота й легкість визначення методів візуально-аналогової шкали болю (ВАШ) дозволяє широко їх використовувати в багатьох різних ситуаціях. Надійність, валідність і можливість використання методів прямого рейтингу були продемонстровані в літературі [16]. Переваги ВАШ включають швидку адаптацію як у дослідницьких, так і в клінічних умовах. Також можна включити визначення балів за шкалою ВАШ для кожної з основних областей здоров’я, включаючи фізичне, соціальне та психічне здоров’я. Було встановлено, що лінія довжиною 10 см (100 мм) має найменшу похибку оцінювання порівняно з довжиною лінії 5 і 20 см. З точки зору психофізичного вимірювання, ВАШ вважається методом прямого оцінювання шкали та формою кросмодальності, у якій довжина лінії регулюється відповідно до інтенсивності болю [17].
Мета – оцінити ефективність та безпеку комбінованого лікарського засобу Фламідез (диклофенак калію, парацетамол, серратіопептидаза) порівняно з диклофенаком натрію при лікуванні гострого болю в нижній частині спини (люмбаго, люмбоішіалгія).
МАТЕРІАЛИ ТА МЕТОДИ ДОСЛІДЖЕНЬ
Дослідження мало дизайн проспективного обсерваційного багатоцентрового порівняльного дослідження, спрямованого на оцінювання ефективності та безпеки комбінованого лікарського засобу Фламідез порівняно з диклофенаком натрію в пацієнтів з гострим поперековим больовим синдромом.
Дослідження проводилося в період з березня до липня 2025 року за участю лікарів первинної ланки (сімейних лікарів та терапевтів), а також лікарів-неврологів з 15 регіонів України. У дослідження було включено 157 пацієнтів з клінічними діагнозами «люмбаго» або «люмбоішіалгія».
Пацієнти розподілялися на групи лікування відповідно до призначеної терапії в межах рутинної клінічної практики. Було сформовано чотири підгрупи залежно від клінічного діагнозу та застосованого препарату: люмбаго – диклофенак натрію (n=29), люмбоішіалгія – диклофенак натрію (n=49), люмбаго – Фламідез (n=25), люмбоішіалгія – Фламідез (n=54).
Фламідез призначали у формі таблеток у стандартній дозі 2 таблетки на добу (еквівалентно 100 мг диклофенаку калію). Диклофенак натрію (Ортофен-Форте) застосовували в дозі 100 мг на добу відповідно до інструкції для медичного застосування.
Критерії включення
До дослідження включали пацієнтів за наявності таких критеріїв:
1. Вік ≥18 років.
2. Наявність гострого поперекового болю тривалістю до 14 днів.
3. Клінічно встановлений діагноз люмбаго або люмбоішіалгія.
4. Підписана інформована згода на участь у дослідженні.
Критерії невключення
Пацієнти не включалися до дослідження за наявності:
Пацієнтам дозволялося застосування базової терапії, включаючи місцеві форми нестероїдних протизапальних препаратів. Такий підхід відповідав умовам реальної клінічної практики, проте потенційно міг впливати на інтенсивність больового синдрому та швидкість його регресу, що враховувалося під час інтерпретації результатів дослідження.
Тривалість спостереження становила 7 днів для кожного пацієнта, що відповідає типовій тривалості лікування гострого поперекового болю.
Передбачалося два візити:
Початковий візит (1-й день) включав:
Пацієнтам видавали індивідуальну картку для щоденного самостійного оцінювання інтенсивності болю за шкалою ВАШ у період з 2-го до 6-го дня лікування.
Заключний візит (7-й день) включав:
Кінцеві точки дослідження
Первинною кінцевою точкою була зміна інтенсивності болю за візуально-аналоговою шкалою (ΔВАШ) між 1-м і 7-м днем лікування.
Вторинні кінцеві точки включали:
Для оцінювання клінічної значущості змін використовували мінімально клінічно важливу різницю (MCID) для шкали ВАШ, що становить приблизно 1,5-2 бали.
Дослідження проводилося відповідно до принципів Гельсінської декларації Всесвітньої медичної асоціації. Усі учасники перед включенням підписали письмову інформовану згоду на участь у дослідженні. Протокол дослідження був схвалений комісією з питань біоетики Національного фармацевтичного університету (протокол № 5 від 25.03.2025 р.).
Статистичну обробку даних проводили за допомогою програмного забезпечення Statistica (версія 12), серійний номер ААА 12334567. Кількісні змінні наведено у вигляді медіани та міжквартильного розмаху (Me [Q1; Q3]). Категоріальні змінні наведені як абсолютна кількість та відсоток. Нормальність розподілу перевіряли за допомогою критерію Шапіро-Вілка. Для порівняння показників до та після лікування використовували парний t-критерій Стьюдента або критерій Вілкоксона залежно від характеру розподілу. Для міжгрупових порівнянь застосовували однофакторний дисперсійний аналіз (ANOVA) або критерій Краскела-Уолліса з відповідними post-hoc тестами (Тьюкі або Данна). Результати представлені з розрахунком 95% довірчих інтервалів (95% CI). Аналіз проводили за принципом per-protocol, оскільки всі включені пацієнти завершили період спостереження. Через відсутність втрат пацієнтів під час спостереження аналіз intention-to-treat не проводився. Статистично значущими вважали відмінності при p<0,05.
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
Демографічна характеристика учасників дослідження
За період проведення дослідження було залучено 157 пацієнтів з різних регіонів України, що забезпечило репрезентативність вибірки та можливість екстраполяції отриманих результатів на всю популяцію країни. Географічне охоплення було досить широким і включало 15 областей України: Дніпропетровську (n=19), Одеську (n=34), Полтавську (n=12), Київську (n=12), Тернопільську (n=9), Хмельницьку (n=10), Черкаську (n=9), Львівську (n=13), Харківську (n=9), Запорізьку (n=7), Миколаївську (n=6), Чернігівську (n=5), Вінницьку (n=4), Сумську (n=4) та Волинську (n=4).
Середній вік пацієнтів становив 51,4±14,2 року, що відповідає активній працездатній групі населення, для якої особливо важливим є швидке усунення больового синдрому. Розподіл пацієнтів за віковими групами показав, що найбільшу частку становили особи віком 43-59 років, що є типовим для захворювань опорно-рухового апарату.
Оцінка ефективності терапії
Динаміка больового синдрому в пацієнтів з різними формами болю в нижній частині спини наведена в таблиці 1.
Аналізуючи дані всіх пацієнтів, встановлено, що в початковий день лікування (1-й день) інтенсивність больового синдрому за ВАШ була високою та приблизно однаковою в обох групах (медіана 7 балів).
Препарат, кількість пацієнтів (n) ВАШ, бали 1-й день 2-й день 3-й день 4-й день 5-й день 6-й день 7-й день Усі пацієнти Диклофенак (n=78) 7 (5; 8) 6 (5; 8) 5 (4; 7) # 5 (3; 6) # 4 (3; 6) # 3 (2; 5) # 2 (1; 4) # Фламідез (n=79) 7 (6; 8) 6 (4; 7) # 4 (3; 6) #* 3 (2; 5) #* 2 (1; 4) #* 1 (1; 3) #* 0 (0; 1) #* Пацієнти з люмбаго Диклофенак (n=29) 6 (5; 8) 6 (5; 7) 5 (5; 7) 5 (4; 6) # 4 (3; 5) # 3 (2; 4) # 2 (1; 3) # Фламідез (n=25) 6 (6; 9) 5 (4; 7) # 4 (4; 5) #* 3 (2; 4) #* 2 (1; 3) #* 1 (0; 2) #* 0 (0; 1) #* Пацієнти з люмбоішіалгією Диклофенак (n=49) 7 (5; 8) 7 (4; 8) 6 (4; 7) # 5 (3; 7) # 4 (2; 6) # 3 (2; 5) # 2 (1; 4) # Фламідез (n=54) 7 (5; 8) 6 (4; 7) # 4 (3; 6) #* 3 (2; 5) #* 2 (2; 4) #* 1 (1; 3) #* 0 (0; 2) #* Примітки: n – кількість пацієнтів; # – достовірні відмінності порівняно з показником на 1-й день, р<0,05; * – достовірні відмінності порівняно з групою диклофенаку, р<0,05.
Протягом 7-денного курсу терапії в обох групах відзначалося поступове зниження болю, однак швидкість і вираженість цього зниження були різними для диклофенаку та Фламідезу. У групі диклофенаку зменшення вираженості болю набуло статистичної значущості порівняно з початковим рівнем лише на 3-й день, коли медіана ВАШ у цій групі знизилася до 5 балів (з 7 на початку; p<0,05 проти 1-го дня). Надалі показники болю в групі диклофенаку продовжували зменшуватися: медіана ВАШ становила 5 балів на 4-й день, 4 бали на 5-й день, 3 бали на 6-й день і 2 бали на 7-й день. Усі ці зміни були достовірними порівняно з початковим рівнем (p<0,05). Таким чином, за тиждень терапії диклофенаком інтенсивність болю зменшилася в середньому приблизно на 5 балів, до 2 балів на 7-й день, що вказує на суттєве полегшення больового синдрому, хоча в частини пацієнтів все ж зберігався помірний біль.
У цьому дослідженні комбінована терапія асоціювалася з більш швидким зниженням інтенсивності болю. Уже на 2-й день лікування інтенсивність болю достовірно знизилася порівняно з 1-м днем (p<0,05), тоді як у групі диклофенаку подібного достовірного поліпшення на 2-й день не спостерігалось. На 3-й день медіана болю в пацієнтів, які отримували Фламідез, становила 4 бали, що достовірно менше як вихідного рівня (p<0,05), так і показника групи диклофенаку на той самий день (p<0,05 між групами). З 3-го дня і до кінця спостереження різниця між групами зберігалася: показники ВАШ у групі Фламідезу були статистично нижчими, ніж у групі диклофенаку на кожному вимірюванні (p<0,05). Динаміка інтенсивності болю показувала щоденний регрес: на 4-й день медіана становила 3 бали, на 5-й – 2 бали, на 6-й – 1 бал. До кінця 7-го дня лікування в групі Фламідезу досягнуто майже повного регресу болю – медіана ВАШ становила 0 балів. Отже, за тиждень терапії комбінованим препаратом Фламідез інтенсивність болю знизилася приблизно на 7 балів (з 7 до 0), що свідчить про майже повне купірування больового синдрому в більшості пацієнтів.
Аналіз підгруп показав аналогічну тенденцію. Так, у пацієнтів з ізольованим люмбаго (поперековий біль без ішіасу, n=54) медіана початкового рівня болю становила 6 балів. У підгрупі диклофенаку достовірне зменшення болю настало лише на 4-й день лікування (p<0,05 проти початкового рівня); раніше (дні 2-3) різниця з базовим рівнем не досягала значущості. Натомість у підгрупі Фламідезу зниження болю при люмбаго досягло статистичної значущості вже на 2-й день (p<0,05). На 3-й день у цій підгрупі медіана ВАШ становила 4 бали, що достовірно нижче, ніж у групі диклофенаку (p<0,05 між групами). До 7-го дня лікування пацієнти з люмбаго, які отримували Фламідез, мали мінімальний залишковий біль (медіана 0 балів), тоді як у групі диклофенаку медіана становила 2 бали (p<0,05 між групами). Схожа картина спостерігалась і в пацієнтів з люмбаго, ускладненим ішіасом (n=103). У цій підгрупі диклофенак забезпечив достовірне полегшення болю з 3-го дня (p<0,05 проти 1-го дня), тоді як Фламідез знову ж таки спрацював швидше – вже на 2-й день відзначалось значуще зниження болю (p<0,05). Надалі різниця між препаратами виявилась ще більш вираженою: на 3-й день при застосуванні Фламідезу медіана ВАШ становила 4 бали проти 6 балів у групі диклофенаку (p<0,05), на 5-й день – 2 бали проти 4 балів відповідно (p<0,05). До кінця 7-го дня в підгрупі люмбоішіалгії медіана болю на фоні Фламідезу знизилась до 0 (міжквартильний розмах 0-2), що вказує на практично повне усунення болю, тоді як при лікуванні диклофенаком медіана становила 2 бали (міжквартильний розмах 1-4; p<0,05 між групами). Отже, в обох клінічних підгрупах комбінований препарат продемонстрував більш швидке настання анальгетичного ефекту та більш повне купірування болю порівняно з монотерапією диклофенаком натрію.
Середній показник зменшення болю Δ ВАШ (рис.), що його розраховували за різницею балів на початку та наприкінці лікування, становив 5,76 бала в групі Фламідезу проти 4,12 бала в групі диклофенаку (p<0,05) – для усіх пацієнтів. Аналогічно, у підгрупі пацієнтів з люмбаго зниження болю було більш вираженим при застосуванні Фламідезу (Δ ВАШ 6,12 бала проти 4,48 бала на тлі диклофенаку, p<0,05). У пацієнтів з люмбоішіалгією комбінована терапія також забезпечила кращий анальгезивний ефект: середній показник Δ ВАШ досягав 5,39 бала порівняно з 3,76 бала в групі диклофенаку (p<0,05). Таким чином, у всіх аналізованих категоріях пацієнтів комбінований препарат Фламідез забезпечив статистично достовірно більш виражену редукцію болю, аніж традиційна НПЗП-терапія диклофенаком натрію.
Важливо, що перевага Фламідезу спостерігалася як при ізольованому поперековому болю (люмбаго), так і при люмбоішіалгії, яка характеризується залученням корінцевого компонента болю. У хворих з люмбоішіалгією монотерапія диклофенаком виявилася менш ефективною (середнє зниження ВАШ становило 3,76 бала), ймовірно через більш інтенсивний запальний набряк та нейропатичний компонент болю. Застосування ж Фламідезу в якості фармакотерапевтичного агента дозволило суттєво посилити знеболювання в цій підгрупі пацієнтів (Δ ВАШ 5,39 бала), практично зрівнявши ступінь полегшення болю з таким у пацієнтів з люмбаго. Це свідчить, що комбінована дія диклофенаку калію, парацетамолу та серратіопептидази ефективно усуває як ноцицептивний, так і запально-компресійний (корінцевий) біль. Для пацієнтів з люмбаго ж отримані результати (Δ ВАШ 6,12 проти 4,48) вказують, що навіть при суто м’язово-скелетному болю в попереку мультимодальна анальгезія перевершує монотерапію: комбінований препарат зменшує біль майже на 40% ефективніше, ніж диклофенак натрію.
З погляду клінічної значущості, виявлені розбіжності між препаратами мають важливе практичне значення. Різниця приблизно в 1,6 бала за шкалою ВАШ на користь Фламідезу означає помітніше полегшення болю для пацієнта. Додаткова анальгезія, досягнута з Фламідезом, наближається до цього порогу або навіть перевищує його. Фактично пацієнти, які отримували Фламідез, у середньому відчули більше ніж на третину вираженіше полегшення болю порівняно з тими, хто отримував лише диклофенак. Така додана ефективність може означати перехід від помірного болю до легкого, що суттєво покращує здатність хворих до повсякденної активності та підвищує якість життя. У підгрупі з люмбоішіалгією, де початковий біль часто інтенсивніший і складніший для лікування, перевага комбінованої терапії (43% додаткового зниження болю на тлі Фламідезу проти диклофенаку) особливо підкреслює її клінічну цінність. Це вказує на те, що застосування мультимодального підходу дозволяє більш ефективно контролювати больовий синдром навіть за наявності корінцевого ураження.
Аналіз активності печінкових трансаміназ у пацієнтів
З метою оціювання безпечності терапії було проаналізовано зміни рівнів печінкових ферментів АЛТ та АСТ з 1-го до 7-го дня лікування (табл. 2).
Загалом по групах помітна різниця у впливі препаратів на ці показники. Аналізуючи дані всіх пацієнтів, визначено, що на тлі диклофенаку спостерігалося помірне підвищення рівнів АЛТ і АСТ за тиждень терапії, яке було статистично достовірним. Медіана АЛТ зросла з 26 Од/л (міжквартильний розмах 20,5-35) на 1-й день до 32 Од/л (25-41,5) на 7-й день (p<0,05 порівняно з початковим рівнем). Аналогічно, медіана АСТ підвищилася з 25 Од/л (20-32) до 30 Од/л (24-39) (p<0,05). Таким чином, монотерапія диклофенаком натрію була пов’язана з клінічно незначущою, але статистично вірогідною ескалацією рівня печінкових трансаміназ, що може вказувати на підвищене навантаження на печінку протягом лікування.
У групі Фламідезу змін показників печінкових ферментів майже не відбулося. Рівні АЛТ та АСТ залишалися близькими до початкових значень, і статистично значущого зростання не відзначено. Медіана АЛТ у групі Фламідезу становила 24 Од/л (19-34) на початку та 27 Од/л (21-34) на 7-й день, різниця статистично невірогідна (p>0,05). Медіана АСТ змінилася з 25 Од/л (18-31) до 27 Од/л (20-32) відповідно – різниця також статистично невірогідна. Важливо, що порівняння між групами в кінці дослідження продемонструвало достовірно нижчі значення трансаміназ у пацієнтів, які отримували Фламідез: на 7-й день рівні АЛТ та АСТ були вірогідно меншими в групі Фламідезу, ніж у групі диклофенаку (p<0,05). Іншими словами, диклофенак натрію спричиняв більш виражений вплив на печінкові показники, аніж комбінований препарат з калієвою сіллю диклофенаку.
Понял, добавил жирность текста (font-weight: bold;) ко всем ячейкам этого блока. Теперь и границы, и текст будут отображаться максимально «строго» и заметно. Вот готовый код: HTML Препарат, кількість пацієнтів (n) АЛТ, Од/л АСТ, Од/л 1-й день 7-й день 1-й день 7-й день Усі пацієнти Диклофенак (n=78) 26 (20,5; 35) 32 (25; 41,5) # 25 (20; 32) 30 (24; 39) # Фламідез (n=79) 24 (19; 34) 27 (21; 34) * 25 (18; 31) 27 (20; 32) * Пацієнти з люмбаго Диклофенак (n=29) 25 (21; 39) 31 (25; 41) # 25 (20; 31) 30 (23; 37) # Фламідез (n=25) 22,5 (19; 39) 26 (21; 36) * 25 (18; 29) 24,5 (20; 30) * Пацієнти з люмбоішіалгією Диклофенак (n=49) 26,5 (21; 31) 33,5 (25; 42) # 25 (17; 32) 32 (25; 39) # Фламідез (n=54) 25,5 (19; 33) 27 (20; 33) * 24,5 (19,5; 31) 27,5 (21; 32) * Примітки: n – кількість пацієнтів; # – достовірні відмінності порівняно з показником на 1-й день, р<0,05; * – достовірні відмінності порівняно з групою диклофенаку, р<0,05.
Подібні відмінності зафіксовано і при роздільному аналізі підгруп. У пацієнтів з люмбаго монотерапія диклофенаком натрію супроводжувалась зростанням АЛТ з медіани 25 до 31 Од/л за 7 днів (p<0,05) та АСТ з 25 до 30 Од/л (p<0,05). Натомість у підгрупі Фламідезу при люмбаго зміни АЛТ/АСТ були мінімальні та недостовірні (медіани АЛТ 22,5 → 26 Од/л; АСТ 25 → 24,5 Од/л; p>0,05), причому кінцеві рівні знову були нижчими, ніж на тлі диклофенаку (p<0,05 між групами). У пацієнтів з люмбоішіалгією спостерігали аналогічну ситуацію: у групі диклофенаку АЛТ зріс з 26,5 до 33,5 Од/л (p<0,05), АСТ – з 25 до 32 Од/л (p<0,05); тоді як при застосуванні Фламідезу зміни були несуттєвими (АЛТ 25,5 → 27 Од/л, АСТ 24,5 → 27,5 Од/л; p>0,05), причому медіанні рівні ферментів на 7-й день виявились достовірно нижчими, аніж у групі диклофенаку (p<0,05).
Отже, комбінований препарат Фламідез продемонстрував більш сприятливу динаміку показників печінкових трансаміназ протягом періоду спостереження. Водночас ці результати слід інтерпретувати обережно, оскільки спостереження тривало лише 7 днів і відображає переважно короткострокову реакцію організму на терапію. Для більш повної оцінки можливого впливу лікування на функціональний стан печінки необхідні дослідження з тривалішим періодом спостереження.
Оцінка частоти побічних реакцій з боку ШКТ
Оцінювання побічних ефектів з боку шлунково-кишкового тракту (ШКТ) виявило, що обидва препарати загалом добре переносились, проте частота шлунково-кишкових розладів була трохи вищою в групі диклофенаку натрію (табл. 3). За час спостереження мінімум одну побічну реакцію з боку ШКТ відзначили 12 із 78 пацієнтів, які отримували диклофенак (15%), у той час як у групі Фламідезу таких пацієнтів було 9 із 79 (11%). Різниця в загальній частоті шлунково-кишкових побічних явищ між групами не досягла статистичної значущості (p>0,05), але демонструвала тенденцію до кращої переносимості Фламідезу. Подібна картина спостерігалася і в підгрупах: при люмбаго частота гастроінтестинальних побічних реакцій становила 14% (4/29) у групі диклофенаку проти 12% (3/25) на тлі Фламідезу; при люмбоішіалгії – 16% (8/49) проти 11% (6/54) відповідно. Таким чином, у всіх аналізованих категоріях комбінований препарат мав номінально дещо нижчу частоту шлунково-кишкових ускладнень, хоча різниця не була статистично значущою.
Група Препарат Кількість пацієнтів, що мали мінімум одну побічну реакцію Усі пацієнти Диклофенак 12/78 (15%) Фламідез 9/79 (11%) Пацієнти з люмбаго Диклофенак 4/29 (14%) Фламідез 3/25 (12%) Пацієнти з люмбоішіалгією Диклофенак 8/49 (16%) Фламідез 6/54 (11%)
Характер побічних реакцій з боку ШКТ був переважно легким та передбачуваним для нестероїдних протизапальних засобів (табл. 4). Найбільш частими симптомами були біль або дискомфорт у животі, нудота та печія. Аналізуючи дані усіх пацієнтів, установлено, що на тлі диклофенаку 11,5% пацієнтів (9/78) скаржились на нудоту, 6% (5/78) – на печію, 14% (11/78) – на біль/дискомфорт у животі. У групі Фламідезу відповідні показники були дещо нижчими: нудота спостерігалась у 9% пацієнтів (7/79), печія – у 4% (3/79), біль або дискомфорт у животі – в 11% (9/79) пацієнтів. Відмінності за окремими реакціями між групами не були статистично значущими, проте відмічається тенденція до меншої частоти й вираженості цих симптомів при застосуванні Фламідезу. Важливо підкреслити, що в більшості випадків один і той самий пацієнт повідомляв про більше ніж один симптом (наприклад, абдомінальний дискомфорт часто поєднувався з нудотою або печією), тому сумарна частота окремих скарг перевищує відсоток пацієнтів із хоча б однією побічною реакцією. Серйозних ускладнень з боку ШКТ (таких як шлунково-кишкові кровотечі або виразки) протягом короткого 7-денного курсу терапії не спостерігалося в жодній групі.
Препарат, кількість пацієнтів (n) Нудота Печія Біль / дискомфорт у животі Усі пацієнти Диклофенак (n=78) 9/78 (11,5%) 5/78 (6%) 11/78 (14%) Фламідез (n=79) 7/79 (9%) 3/79 (4%) 9/79 (11%) Пацієнти з люмбаго Диклофенак (n=29) 3/29 (10%) 1/29 (3%) 3/29 (10%) Фламідез (n=25) 2/25 (8%) 1/25 (4%) 3/25 (12%) Пацієнти з люмбоішіалгією Диклофенак (n=49) 6/49 (12%) 4/49 (8%) 8/49 (16%) Фламідез (n=54) 5/54 (9%) 2/54 (4%) 6/54 (11%) Примітки: у переважній більшості випадків окремі пацієнти відмічали більше ніж одну побічну реакцію (наприклад, біль/дискомфорт у животі супроводжувався нудотою).
Отримані результати демонструють переваги комбінованої терапії з використанням калієвої солі диклофенаку (Фламідез) над монотерапією диклофенаком натрію в аспекті як клінічної ефективності, так і переносимості. З точки зору знеболювальної дії Фламідез забезпечує більш швидке настання та більш виражене полегшення болю в пацієнтів з гострим люмбаго та ішіасом. Уже на другий день лікування біль у групі Фламідезу достовірно зменшується, тоді як диклофенак натрію потребує більше часу для досягнення помітного ефекту. Різниця в показниках ВАШ між групами на користь Фламідезу проявилася з 3-го дня і зберігалася надалі, що свідчить про більш сильний та швидкий анальгетичний ефект комбінованого препарату. До кінця тижневого курсу в більшості пацієнтів, які отримували Фламідез, біль практично зник (медіана 0 балів), тоді як при застосуванні лише диклофенаку натрію в частини пацієнтів залишався помірний больовий синдром. Така динаміка є клінічно значущою, оскільки швидке купірування болю покращує якість життя пацієнтів і може сприяти швидшому відновленню активності.
Переваги Фламідезу можуть пояснюватися, у першу чергу, його складом: комбінація диклофенаку калію з парацетамолом та ферментом серратіопептидазою забезпечує мультифакторний вплив на больовий синдром. Диклофенак калію як НПЗП зменшує запалення і біль через інгібіцію синтезу простагландинів, парацетамол додає центральний анальгетичний ефект, а серратіопептидаза має протинабрякові та протизапальні властивості, що можуть покращувати мікроциркуляцію і зменшувати набряк у місці ураження нервових корінців. Синергічна дія цих компонентів, ймовірно, підсилює знеболювання без необхідності підвищувати дозу НПЗП, що пояснює швидше зниження болю та більшу кінцеву ефективність Фламідезу [19].
Отримані результати узгоджуються з даними інших клінічних досліджень, у яких комбіновані анальгетичні препарати демонстрували більш швидке зменшення больового синдрому порівняно з монотерапією НПЗП. Зокрема, у ряді рандомізованих досліджень показано, що мультимодальна анальгезія із застосуванням НПЗП у комбінації з іншими анальгетиками дозволяє підвищити ефективність контролю болю та зменшити потребу у високих дозах НПЗП.
Окремо варто зазначити можливі переваги калієвої солі диклофенаку. Диклофенак калію є швидкорозчинною формою, що забезпечує швидше всмоктування та, як наслідок, швидший та інтенсивніший анальгезивний ефект. Кокрейнівський метааналіз свідчить, що одноразова доза диклофенаку калію (50 мг) забезпечує значуще полегшення болю в значно більшої кількості пацієнтів, аніж аналогічна доза натрієвої солі диклофенаку [20]. Отже, калієва сіль забезпечує швидший і сильніший анальгетичний ефект при гострому болю, при цьому натрієва сіль діє повільніше й менш ефективна в таких ситуаціях.
Щодо безпечності, комбінований препарат Фламідез також продемонстрував кращий профіль. Незважаючи на те, що обидва досліджувані режими загалом добре переносилися протягом 7 днів, у групі диклофенаку натрію виявлено дещо більшу частоту побічних реакцій з боку ШКТ і помітніші зміни лабораторних показників. Підвищення рівнів АЛТ та АСТ при застосуванні диклофенаку натрію хоч і було відносно невеликим та клінічно незначущим, але статистично підтверджує наявність фармакологічного навантаження на печінку. У половини пацієнтів медіани трансаміназ наблизилися до верхньої межі норми вже за тиждень лікування. Навпаки, на тлі Фламідезу таких змін не спостерігалося, що свідчить про те, що навіть додавання парацетамолу не посилює гепатотоксичної дії, а можливо, дозволяє зменшити ефективну дозу диклофенаку калію в складі комбінації. При цьому варто зазначити можливий захисний вплив третього компонента Фламідезу – серратіопептидази, яка здатна не лише посилювати протизапальний та знеболювальний потенціал НПЗП [21], але й завдяки своїм мультимодальним позитивним властивостям теоретично запобігати негативному впливу на печінку [22], що потребує окремих досліджень.
В аспекті шлунково-кишкової переносимості відмінності між групами були менш виражені, проте загальна тенденція все ж складається на користь Фламідезу, на тлі якого спостерігали дещо меншу частоту розвитку нудоти, печії, абдомінального дискомфорту та взагалі нижчу сумарну кількість пацієнтів з гастроінтестинальними побічними реакціями. Це може бути пов’язано з тим, що комбінована терапія дозволяє досягти знеболювання при нижчому навантаженні на шлунково-кишковий тракт від НПЗП, а також з потенційними цитопротективними ефектами серратіопептидази. У деяких експериментальних і клінічних роботах повідомляється про потенційні протизапальні та протинабрякові властивості серратіопептидази, які можуть посилювати анальгетичний ефект НПЗП. Однак доказова база щодо її гастро- або гепатопротекторних властивостей залишається обмеженою і потребує подальших досліджень [23]. При цьому не можна виключати й можливі переваги калієвої солі диклофенаку. Визначено, що диклофенак калію в значно більшій дозі мав порівняну переносимість з диклофенаком натрію (150 мг/добу проти 100 мг/добу) [24]. Такі властивості калієвої солі можуть бути опосередковано пов’язані з фармакокінетичними особливостями, коли швидше всмоктування диклофенаку калію обмежує час його безпосереднього контакту зі слизовою ШКТ та, як наслідок, подразнювальну дію [25].
Важливо, що побічні реакції, які фіксували пацієнти, мали легкий перебіг та не призводили до відмови від лікування. При цьому жодного випадку серйозного ураження ШКТ (наприклад, виразки чи кровотечі) в обох групах не було, що підкреслює безпечність короткого курсу як
моно-, так і комбінованої терапії.
Таким чином, у цьому дослідженні застосування Фламідезу асоціювалося з більш сприятливим співвідношенням користі та ризику порівняно з диклофенаком натрію при лікуванні больового синдрому в нижній частині спини. Комбінація диклофенаку калію з парацетамолом і серратіопептидазою забезпечила швидше та повніше полегшення болю, не спричиняючи при цьому значного підвищення печінкових ферментів і з тенденційно меншою частотою побічних ефектів з боку ШКТ. Диклофенак як монотерапія, хоча й ефективно знижував біль, поступався комбінованому підходу за швидкістю анальгезії і мав дещо гіршу переносимість. З позицій клінічної фармакології та практичної медицини отримані дані свідчать про можливі клінічні переваги застосування комбінованого препарату Фламідез при гострому люмбаго та люмбоішіалгії, оскільки він дозволяє досягти кращого клінічного результату за коротший час і з меншою імовірністю розвитку побічних реакцій. Це особливо актуально для пацієнтів, яким потрібне швидке відновлення працездатності та мінімізація ризиків при знеболювальній терапії.
Обмеження дослідження.
Незважаючи на отримані клінічно значущі результати, інтерпретація даних цього дослідження повинна враховувати низку методологічних обмежень.
По-перше, дослідження мало відкритий обсерваційний дизайн без рандомізації та засліплення, що потенційно може впливати на порівнянність груп і створювати ризик систематичних похибок. Призначення терапії здійснювалося лікарями в умовах рутинної клінічної практики, тому розподіл пацієнтів між групами не був випадковим.
По-друге, тривалість спостереження становила лише 7 днів, що відповідає типовій тривалості лікування гострого поперекового болю, проте обмежує можливість оцінювання довгострокової ефективності та безпеки терапії. Зокрема, відмінності між групами щодо змін рівнів печінкових трансаміназ (АЛТ та АСТ) відображають переважно короткострокову реакцію організму на лікування і не дозволяють повною мірою оцінити потенційний вплив терапії при більш тривалому застосуванні.
По-третє, у межах дослідження дозволялося застосування супутньої терапії відповідно до стандартної клінічної практики, зокрема місцевих форм нестероїдних протизапальних препаратів. Використання таких засобів могло певною мірою впливати на інтенсивність больового синдрому та швидкість його регресу, що потенційно могло модифікувати кінцеві результати лікування. Водночас подібний підхід відображає реальні умови амбулаторної клінічної практики.
По-четверте, оцінка ефективності терапії ґрунтувалася переважно на суб’єктивному показнику інтенсивності болю за візуально-аналоговою шкалою (ВАШ). Незважаючи на широку валідність і поширене використання цього інструменту в клінічних дослідженнях, результати можуть частково залежати від індивідуального сприйняття болю пацієнтами.
З огляду на зазначені обмеження отримані результати слід розглядати як дані, що відображають ефективність і переносимість терапії в умовах короткострокового застосування в реальній клінічній практиці. Подальші рандомізовані контрольовані дослідження з більшим періодом спостереження та суворішим контролем супутньої терапії є необхідними для підтвердження отриманих результатів та більш повної оцінки довгострокової ефективності й безпеки застосування досліджуваних препаратів.
ВИСНОВКИ
1. У проспективному багатоцентровому обсерваційному дослідженні за участю 157 пацієнтів з гострим поперековим больовим синдромом (люмбаго та люмбоішіалгія) проведено порівняльне оцінювання ефективності та переносимості комбінованого лікарського засобу Фламідез (диклофенак калію, парацетамол, серратіопептидаза) та диклофенаку натрію.
2. Обидві досліджувані схеми терапії асоціювалися зі зменшенням інтенсивності больового синдрому за візуально-аналоговою шкалою протягом 7-денного курсу лікування.
3. У групі пацієнтів, які отримували комбінований препарат Фламідез, спостерігалася тенденція до більш швидкого та вираженого зниження інтенсивності болю порівняно з монотерапією диклофенаком натрію.
4. Показник середнього зниження інтенсивності болю (ΔВАШ) у групі Фламідезу був вищим, ніж у групі диклофенаку натрію, що може свідчити про потенційні переваги мультимодального підходу до анальгезії при гострому поперековому болю.
5. Профіль безпеки обох режимів лікування протягом короткотривалого застосування був загалом сприятливим. У групі диклофенаку натрію відзначалося помірне підвищення рівнів печінкових трансаміназ, тоді як у групі Фламідезу подібної тенденції не спостерігалося; водночас ці результати потребують обережної інтерпретації з огляду на короткий період спостереження.
6. Отримані результати свідчать, що комбінований препарат Фламідез може розглядатися як один з можливих варіантів фармакотерапії гострого поперекового болю, проте для остаточного підтвердження його клінічних переваг необхідні подальші рандомізовані контрольовані дослідження з більш тривалим періодом спостереження.
Внески авторів:
Кононенко Н.М. – дослідження, методологія, формальний аналіз, написання – початковий проєкт, редагування;
Цивунін В.В. – концептуалізація, курування даних, адміністрування проєкту;
Брюханова Т.О. – дослідження, формальний аналіз, ресурси;
Співавтори (20)4 – дослідження, ресурси.
Фінансування. Дослідження не має зовнішніх джерел фінансування.
Конфлікт інтересів. Цивунін В.В. є головним медичним радником ТОВ «ОРГАНОСІН ЛТД» – компанії, що здійснює маркетування лікарського засобу Фламідез. Інші автори заявляють про відсутність потенційного конфлікту інтересів. Автори-дослідники не отримували фінансових винагород або інших стимулів за участь у проведенні цього дослідження. Дослідження було проведено як незалежне обсерваційне спостереження в умовах рутинної клінічної практики.
4 Співавтори (20) та їх внески в дослідження
| ПІБ | Місце роботи | Внесок автора в дослідження | ORCID |
|---|---|---|---|
|
Дзик І.М. |
Медичний центр Garvis м. Дніпро |
дослідження, ресурси |
|
|
Загранична Ю.П. |
АЗПСМ № 6а – КНП Білоцерківської міської ради «МЦПМСД № 1» |
дослідження, ресурси |
|
|
Сологуб А.Ю. |
Сквирська АЗПСМ – КНП Сквирської міської ради «Сквирський МЦПМСД» |
дослідження, ресурси |
|
|
Головай А.С. |
АЗПСМ №6а – КНП Білоцерківської міської ради «МЦПМСД № 1» |
дослідження, ресурси |
|
|
Гулевська К.В. |
КНП Усатівської сільської ради «Усатівський ЦПМСД» |
дослідження, ресурси |
|
|
Панасюк І.Ф. |
КНП «ЦПМСД № 18» Одеської міської ради |
дослідження, ресурси |
|
|
Гончарук К.О. |
КНП «ЦПМСД № 2» Одеської міської ради |
дослідження, ресурси |
|
|
Бутель О.М. |
АЗПСМ № 6 КНП «ЦПМСД» Печерського району міста Києва |
дослідження, ресурси |
|
|
Канська А.Я. |
Амбулаторія ЗПСМ № 7 КНП «ЦПМСД № 1» Голосіївського району міста Києва |
дослідження, ресурси |
|
|
Гришан М.А. |
Українська амбулаторія ЗПСМ Обухівського районного ЦПМСД |
дослідження, ресурси |
|
|
Безбах А.І. |
ФОП «Мандро» |
дослідження, ресурси |
|
|
Клановець К.С. |
Поліклініка № 3 КНП «Чернігівська міська лікарня № 2» Чернігівської міської ради |
дослідження, ресурси |
|
|
Сеник І.І. |
Амбулаторія сімейної медицини № 9 Ніжинського міського ЦПМСД |
дослідження, ресурси |
|
|
Титоренко В.В. |
Поліклініка № 3 КНП «Чернігівська міська лікарня №2» Чернігівської міської ради |
дослідження, ресурси |
|
|
Іскужина А.С. |
КНП «Павлоградська міська лікарня № 1» Павлоградської міської ради |
дослідження, ресурси |
|
|
Гайченя С.В. |
Амбулаторія ЗПСМ № 3 Кам'янець-Подільської міської ради |
дослідження, ресурси |
|
|
Мізіна О.А. |
КНП «Лівобережний центр первинної медико-санітарної допомоги № 2» Запорізької міської ради |
дослідження, ресурси |
|
|
Гриценко М.О. |
КНП «ДЦПМСД 9» Дніпровської міської ради |
дослідження, ресурси |
|
|
Краюшкіна І.А. |
ТОВ «Оксфорд Медікал» м. Кам'янське |
дослідження, ресурси |
|
|
Ситнік А.В. |
МЦ «Лікую.юа» |
дослідження, ресурси |
REFERENCES
1. Li Y, Zou C, Guo W, et al. Global burden of low back pain and its attributable risk factors from 1990 to 2021: a comprehensive analysis from the Global Burden of Disease Study 2021. Frontiers in Public Health. 2024;12:1480779. doi: https://doi.org/10.3389/fpubh.2024.1480779
2. Low back pain and sciatica in over 16s: assessment and management. NICE guideline [NG59]. National Institute for Health and Care Excellence (NICE). [Internet]. 2020 [cited 2025 Dec 23]. Available from: https://www.nice.org.uk/guidance/ng59
3. Ferreira ML, March L, Croft P, Maher CG, Lin CW, Buchbinder R, et al. Global, regional, and national burden of low back pain, 1990-2020, its attributable risk factors, and forecasts to 2050: a systematic analysis of the Global Burden of Disease Study 2021. Lancet Rheumatol. 2023;5(6):e316-e329. doi: https://doi.org/10.1016/S2665-9913(23)00098-X
4. American College of Physicians. Noninvasive Treatments for Acute, Subacute, and Chronic Low Back Pain: Clinical Practice Guideline. Ann Intern Med. 2021;174(3):391-8. doi: https://doi.org/10.7326/M19-2063
5. WHO report on non-steroidal anti-inflammatory drugs safety update. World Health Organization [Internet]. 2022 [cited 2025 Dec 23]. Available from: https://www.who.int/publications/i/item/NSAIDs-safety-2022
6. Marin T. Single‑dose intravenous diclofenac for acute postoperative pain in adults: A Cochrane review summary. Int J Nurs Stud. 2021;113:103410. doi: https://doi.org/10.1016/j.ijnurstu.2019.103410
7. Diclofenac safety profile. World Health Organization [Internet]. 2022 [cited 2025 Dec 23]. Available from: https://www.who.int/publications/i/item/NSAIDs-safety-2022
8. Alshargabi A, Mehta D, Elhassan GO, Singh N, Farooq U, Khan A, et al. Recent developments in diclofenac derivatives and drug delivery carriers: structural modification, pharmacokinetics, and toxicity reduction. Eur J Pharm Sci. 2024;192:106324. doi: https://doi.org/10.1016/j.ejps.2024.106324
9. Dammann P, Kirsch M, Bittersohl T, et al. Diclofenac-induced hepatotoxicity: a review of literature and recent case series. World J Hepatol. 2020;12(8):490-502. doi: https://doi.org/10.4254/wjh.v12.i8.4
10. García Rodríguez LA, Tacconelli S, Patrignani P. Role of dose potency in the risk of NSAID-induced hepatotoxicity: a systematic review. Br J Clin Pharmacol. 2021;87(6):2345-56. doi: https://doi.org/10.1111/bcp.14582
11. Derry S, Wiffen PJ, Moore RA. Single dose oral diclofenac for acute postoperative pain in adults. Cochrane Database Syst Rev. 2015;7:CD004768. doi: https://doi.org/10.1002/14651858.CD011509
12. Opryshko VI. Perspectives for using serratiopeptidase in systemic enzyme therapy for low-intensity chronic inflammation and pain syndromes: from mechanisms of action to practical implementation (literature review). Pain Joints spine. 2024;14(3):162-72. doi: https://doi.org/10.22141/pjs.14.3.2024.432
13. Bapat K, Kumar A, Katke P, Kulkarni K, Suryawanshi S. Serratiopeptidase with diclofenac sodium for the management of post-operative pain and inflammation in a day care obstetric and gynaecological surgeries. Indian Journal of Obstetrics and Gynecology Research. 2024;11(3):442-6. doi: https://doi.org/10.18231/j.ijogr.2024.080
14. [FLAMIDEZ®: proven efficacy and high safety profile of the original combination]. Zdorovia Ukrainy 21 storichchia. [Internet]. 2025 [cited 2025 Dec 23];5(591):55-7. Ukrainian. Available from: https://health-ua.com/neurology/bolyovi-sindromi/79956-flamidez-dovedena-efektivnist-ta-visokii-profil-bezpeki-originalnoyi-kombinaciyi
15. Kaplan RM, Bush JW. Health‑related quality of life measurement for evaluation research and policy analysis. Health Psychology. 1982;1:61-80. doi: https://doi.org/10.1037/0278-6133.1.1.61
16. Saki F, Mohammadi F, Chen H, Alizadeh M, Yamamoto A, Lee SY, et al. BodyBalance as an exercise therapy trial in knee osteoarthritis: visual analogue scale (VAS) for pain severity and its reliability in outcome assessment. Trials. 2025;26(75):1025. doi: https://doi.org/10.1186/s13063-025-09036-w
17. Koo М. Visual Analogue Scale. Encyclopedia. 2025;5(4):190. doi: https://doi.org/10.3390/encyclopedia504019
18. Lee SW. Methods for testing statistical differences between groups in medical research: statistical standard and guideline of Life Cycle Committee. Life Cycle. 2022;2:e1. doi: https://doi.org/10.54724/lc.2022.e1
19. Tena-Garitaonaindia M, Rubio JM, Martínez-Plata E, Martínez-Augustin O, Sánchez de Medina F. Pharmacological bases of combining nonsteroidal antiinflammatory drugs and paracetamol. Biomedicine & Pharmacotherapy. 2025;187:118069. doi: https://doi.org/10.1016/j.biopha.2025.118069
20. Derry S, Wiffen PJ, Moore RA. Single dose oral diclofenac for acute postoperative pain in adults. Cochrane Database Syst Rev. 2015;7:CD004768. doi: https://doi.org/10.1002/14651858.CD011509
21. Jadhav SB, Shah N, Rathi A, Rathi V, Rathi A. Serratiopeptidase: Insights into the therapeutic applications. Biotechnol Rep (Amst). 2020;28:e00544. doi: https://doi.org/10.1016/j.btre.2020.e00544
22. Nair SR, C SD. Serratiopeptidase: An integrated View of Multifaceted Therapeutic Enzyme. Biomolecules. 2022;12:1468. doi: https://doi.org/10.3390/biom12101468
23. Narayanan KB, Park JY, Lee YS, Choi HJ, Kim EK, Seo CH, et al. Enzyme-based anti-inflammatory therapeutics for inflammatory diseases: natural and engineered enzymes and their formulations. Pharmaceutics. 2025;17(5):606. doi: https://doi.org/10.3390/pharmaceutics17050606
24. Pellesi L, Guerzoni S, Cainazzo MM, Baraldi C, Pini LA. Pharmacological management of migraine: acute therapies including diclofenac potassium and other NSAIDs. Expert Rev Neurother. 2024;24(5):367-77. doi: https://doi.org/10.1080/14737175.2024.2349791
25. [Clinical aspects of the use of diclofenac potassium in the treatment of pain]. NeuroNews: psykhonevrolohiia ta neiropsykhiatriia. [Internet]. 2018 [cited 2025 Dec 23];2(95):36-38. Ukrainian. Available from: https://neuronews.com.ua/ua/archive/2018/2%2895%29/pages-36-38/klinichni-aspekti-zastosuvannya-diklofenaku-kaliyu-u-likuvanni-bolyu#gsc.tab=0