Ключові слова: променева терапія, медичні зображення, оптична щільність, поглинена доза, невизначеності
Key words: radiotherapy, medical images, optical density, absorbed dose, uncertainties
Реферат
Якість променевої терапії значно покращилася завдяки використанню нових джерел та видів опромінення, а також сучасного тривимірного планування. Проте рівень променевих пошкоджень залишається суттєвим, що зумовлює необхідність аналізу точності інструментів, які забезпечують формування зображень і розрахунок доз. Метою роботи було визначення ймовірних невизначеностей, що виникають при використанні програмного забезпечення рентген-комп’ютерного томографа «TOSHIBA Asteion Super 4» та планувальних систем прискорювача електронів «Elekta Synergy» (Elekta Limited), а також пошук шляхів зменшення цих невизначеностей. Було проаналізовано 28 планів променевої терапії хворих, яка проводилася на прискорювачі електронів «Elekta Synergy» за останні чотири роки. Для оцінювання параметрів зображення аналізували дані рентген-комп’ютерної томографії з товщиною реконструкції 1,5 мм, оброблені програмою «eFilm». Визначали розмір пікселя, кількість пікселів у заданому фрагменті, площу та оптичну щільність різних ділянок зображення. Невизначеності дозового планування оцінювали в програмі «Monaco Treatment Planning System» на основі значень поглинутих доз у зонах з мінімальною оптичною щільністю всередині контурів об’єкта опромінення, у чорному фоні внутрішніх порожнин та за межами зовнішнього контура тіла. Встановлено факт некоректного визначення програмою «eFilm» геометричних параметрів зображення з похибкою 8-15%. Значення оптичної щільності в чорному фоні варіювали від -1000 HU біля меж об’єкта до -834 HU на більшій відстані. Показано значні коливання поглинутих доз у зонах низької щільності: при однакових умовах вимірювання доза могла становити як 0,0 Гр, так і 15,4 Гр. На відстані 4 мм від зовнішнього контура при щільності -1001 HU доза дорівнювала 5,9 Гр і зростала при наближенні до контура. Отримані результати свідчать, що похибки формування DICOM-зображень і розрахунку доз можуть зумовлювати істотні невизначеності, які впливають на точність планування та ефективність лікування. Удосконалення програмного забезпечення комп'ютерної томографії (КТ) та планувальних систем розглядається як перспективний шлях для зменшення таких похибок.
Abstract
The uncertainties in radiation therapy planning. Kikhtenko I.M., Khvorostenko Y.M., Filonenko N.Yu., Haldina O.M. The quality of radiation therapy has significantly improved due to the introduction of new irradiation sources, advanced delivery techniques, and modern three-dimensional treatment planning. However, the level of radiation-induced damage remains considerable, necessitating an assessment of the accuracy of tools responsible for image generation and dose calculation. The aim of the study was to identify potential uncertainties arising from the use of the TOSHIBA Asteion Super 4 computed tomography software and the planning systems of the Elekta Synergy linear accelerator (Elekta Limited), as well as to determine approaches for reducing these uncertainties. Twenty-eight patient radiotherapy plans carried out on the Elekta Synergy accelerator within the past four years were subjected to analysis. To evaluate image parameters, computed tomography data with a slice reconstruction thickness of 1.5 mm processed using the eFilm software were analysed. Pixel size, the number of pixels within a selected region, area, and optical density of various image segments were measured. Dose-planning uncertainties were estimated in the Monaco Treatment Planning System software based on absorbed-dose values in regions with minimal optical density inside the irradiation target contours, in the black-background cavities within the object, and outside the external body contour at various distances. The analysis revealed incorrect determination of image geometric parameters by eFilm, with an error of 8-15%. Optical-density values in the black background ranged from –1000 HU near the object boundary to -834 HU at greater distances. Significant variations in absorbed dose were observed in low-density regions: under identical conditions, dose values ranged from 0.0 Gy to 15.4 Gy. At a distance of 4 mm from the outer contour, an optical density of -1001 HU corresponded to a dose of 5.9 Gy, increasing with proximity to the contour. These findings indicate that errors in DICOM-image formation and dose calculation may introduce substantial uncertainties affecting treatment-planning accuracy and therapeutic outcomes. Improving computed tomography (CT) image-processing software and radiotherapy planning systems is considered a promising approach to reducing such uncertainties.
Захворюваність на онкологічну патологію у світі невпинно зростає. За даними ВООЗ, у 2022 році було зареєстровано 20 млн нових випадків раку, з яких 9,7 млн завершилися летально; кількість пацієнтів, що пережили п’ятирічний рубіж, становила 53,3 млн. За прогнозами, до 2050 року захворюваність зросте на 77% і досягне 35 млн випадків, при цьому в країнах з низьким індексом розвитку людського потенціалу приріст може становити до 142% порівняно з 2022 роком [1]. У США у 2025 році очікується близько 2 041 910 нових випадків раку (приблизно 5600 щодня), тоді як у світі цей показник перевищить 52 900 випадків на добу [2, 3].
В Україні зберігається світова тенденція зростання онкологічної захворюваності. Так, за даними Національного канцер-реєстру України, у 2024 році на обліку перебувало понад 1,1 млн пацієнтів з онкологічними захворюваннями. Серед хворих, що перебували під спостереженням упродовж п’яти років, чоловіки працездатного віку становили 39,9%, жінки – 48,1%, з яких 9,9% були репродуктивного віку; решта – особи пенсійного віку [4]. Пропорційно зростає також кількість пацієнтів, які отримують комбіноване спеціалізоване лікування, що включає хірургічний, променевий та хіміо-гормональний або імунний компоненти [5].
Променева терапія є ключовою складовою багатокомпонентного лікування раку [6, 7]. За даними ВООЗ, понад 50% онкологічних пацієнтів потребують променевої терапії при лікуванні найбільш поширених форм злоякісних новоутворень [8], і щороку близько 7 млн хворих у світі проходять відповідні курси лікування. Водночас навіть застосування сучасних променевих технологій не усуває ризику розвитку променевих ушкоджень нормальних тканин і вторинних злоякісних новоутворень [9]. Зокрема, від 74 до 100% жінок після опромінення з приводу раку молочної залози мають прояви ушкодження шкіри, серед яких променевий фіброз є тяжким, прогресуючим та незворотним пізнім ускладненням. Частота радіаційно-індукованих уражень легень становить 4,5-63% у проспективних і 0,9-30% у ретроспективних дослідженнях [10], а ризик розвитку серцевої недостатності внаслідок дифузного фіброзу міокарда зростає в 16 разів [11].
Таким чином, зростання кількості онкологічних пацієнтів й обсягів променевої терапії робить проблему променевих ушкоджень нормальних тканин особливо актуальною. Незважаючи на вдосконалення технологій опромінення та сучасне тривимірне планування, променеві ускладнення залишаються поширеними, що пов’язують з невизначеностями, притаманними багатокомпонентному процесу підготовки та проведення лікування із застосуванням складної апаратури [12]. Через це питання невизначеностей активно опрацьовують на національному та міжнародному рівні [13]. Сучасні підходи до оцінювання невизначеностей у променевій терапії базуються на рекомендаціях провідних міжнародних організацій, зокрема AAPM та IAEA [15-19]. Згідно з AAPM TG-132 [20] та TG-179 [21], геометричні та дозиметричні невизначеності можуть виникати на всіх етапах – від отримання зображень до планування та реалізації лікування. Також у цитованих документах підкреслюється критична роль точності визначення об’ємів, зв’язку між HU й електронною щільністю та акцентується увага на необхідності систематичного контролю якості, калібрування перетворення КТ-чисел у щільність та врахування алгоритмічних похибок TPS.
Результати досліджень розподілу доз на фантомних моделях свідчать про зменшення доз поза полем із віддаленням від його краю та зі збільшенням глибини [22], водночас на периферії поля може спостерігатися локальне зростання дози. Так, для прискорювача Oncor зафіксовано пік периферичної дози до 1,4% на відстані 6 см від краю поля 10×10 см² для електронних пучків 6 і 9 МеВ, а для 15 МеВ – до 2,3% за аналогічних умов [23]. Це зумовлено інтенсивним розсіюванням електронів у головці прискорювача, аплікаторах, вирізах і повітрі, що призводить до утворення фотонного випромінювання та електронів низької енергії і формування клінічно неприйнятної півтіні. Інші дослідження виявили піки периферичної дози на відстані 12-15 см за краєм поля [24], а максимальні значення – для електронних пучків з енергією 18 МеВ [25]. У літературі підкреслюється критична важливість контролю периферичних доз й оптимізації апаратного забезпечення з метою підвищення безпеки пацієнтів [26], а одним з резервів покращення результатів лікування вважається виявлення та мінімізація неврахованих невизначеностей [27].
Для планування променевої терапії найчастіше використовують дані рентген-комп’ютерної томографії, що зберігаються у форматі DICOM – міжнародному стандарті медичних зображень, підтримуваному провідними виробниками радіологічного обладнання [28, 29]. Одним з поширених програмних продуктів для їх аналізу є «eFilm». Проведений нами аналіз КТ-зображень показав, що навіть за дослідження однієї й тієї ж анатомічної ділянки на одному апараті та за однакових режимів вимірювані параметри можуть відрізнятися за розмірністю пікселя та щільністю [30]. З огляду на те, що в окремих випадках межу між нормою і патологією визначають десяті частки міліметра та кілька одиниць Хаунсфілда, а піксель (воксель) є базовою структурною одиницею планування конформної променевої терапії, доцільним є детальне дослідження його характеристик [31] та особливостей розподілу поглинутих доз у системах планування і гарантії якості радіотерапії.
Сучасний розвиток технологій штучного інтелекту суттєво трансформує процеси планування променевої терапії, зокрема етап сегментації та контурингу [32]. Сучасні алгоритми реконструкції КТ-зображень, зокрема ітеративної реконструкції зображень та реконструкції КТ-зображень на основі глибинного навчання (deep learning-based reconstruction, DLR) [33], можуть змінювати значення HU, зменшувати шум та згладжувати границі структур, що потенційно впливає на точність сегментації та дозиметричних розрахунків. За даними сучасних досліджень [34-37], відхилення HU при використанні DLR можуть досягати клінічно значущих величин, особливо на межах тканин. Це створює додаткові джерела систематичних невизначеностей у плануванні променевої терапії.
Метою цієї роботи було наукове обґрунтування та експериментальне дослідження впливу геометричних і дозиметричних невизначеностей, пов’язаних із характеристиками пікселів і вокселів DICOM-зображень рентген-комп’ютерної томографії, на формування планів променевої терапії та визначення поглинутих доз у зонах клінічного інтересу.
МАТЕРІАЛИ ТА МЕТОДИ ДОСЛІДЖЕНЬ
Рентген-комп’ютерну томографію (РКТ) пацієнтів з пухлинами мозку виконували на комп’ютерному томографі TOSHIBA Asteion Super 4. Аналізували поперечні зрізи з товщиною реконструкції 1,5 мм за допомогою програми обробки DICOM-файлів «eFilm» («Phillips Medical MXLiteView Version 1.22 MS»), яка дозволяє визначати розміри пікселя, кількість пікселів у заданій області, площу та оптичну щільність зображення.
На площині зрізу прямокутним маркером ROI Rectangle виділяли ділянки пухлини розміром 1-28 суміжних пікселів, розташованих у ряд. На одному зрізі аналізували шість таких ділянок – максимальну кількість, що допускається програмою, кожну з яких маркували окремим кольором. Розміри полів, їх площа, кількість пікселів та оптична щільність автоматично визначалися програмою і відображалися у вигляді цифрових значень, які заносили до таблиць для подальшого порівняння з результатами ручних вимірювань.
Крім того, визначали оптичну щільність ділянок поза межами об’єкта дослідження (чорний фон). Для цього квадратним маркером виділяли шість ділянок розміром один піксель кожна на різній відстані по променю від краю контура зображення. Отримані дані також табулювали та аналізували.
Невизначеності, що виникають при плануванні променевої терапії на електронному прискорювачі Elekta Synergy з використанням планувальної системи Monaco TPS, оцінювали за даними розподілу поглинутих доз на поперечних зрізах. Аналіз проводили в зонах з мінімальною оптичною щільністю всередині контурів об’єкта, у чорному фоні порожнин, а також у ділянках поза зовнішніми контурами тіла пацієнта на різних відстанях.
Клінічні методи обстеження (інструментальні та лабораторні) застосовувалися відповідно до сучасних рекомендацій [14-16, 38-42]. Рандомізоване дослідження проведено за даними комп’ютерного планування у 28 хворих зі злоякісними новоутвореннями молочної залози, головного мозку, гортані та стравоходу.
Кількісні та якісні дані були подані відповідно до загальноприйнятих статистичних підходів. Статистичний аналіз даних 28 планів променевої терапії проводився із застосуванням критерію χ², критерію Вілкоксона – Манна – Вїтні та пермутаційного підходу [43, 44]. Для всіх оцінок використовувався рівень довірчої ймовірності 97,5%, що забезпечує високу надійність інтервалів. Обчислення виконувалися в програмному середовищі Python 3.14.2 (Python Software Foundation License, вільне програмне забезпечення) за допомогою хмарного застосунку Google Colab, Free License) з використанням модуля stats бібліотеки SciPy (безкоштовна бібліотека Python з відкритим кодом, яка використовується для наукових та технічних обчислень, що не передбачає індивідуального номера ліцензії).
Дослідження схвалені комісією з питань біомедичної етики ДДМУ (витяг з протоколу № 32 від 11.11.2025 р.) та проведені згідно з письмовою згодою учасників і відповідно до принципів біоетики, викладених у Гельсінській декларації «Етичні принципи медичних досліджень за участю людей» та «Загальній декларації про біоетику та права людини (ЮНЕСКО)».
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
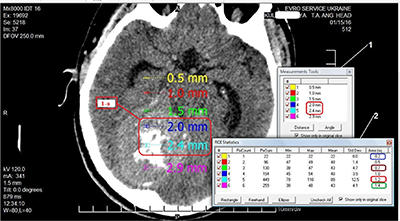
Дані вимірювання розміру пікселів на знімках хворої К. подано на рисунку 1.
Отримані дані програмного визначення розміру пікселя, довжини виділеної ділянки зображення, її площі, а також розрахункового розміру пікселя, довжини та площі зображення внесені до таблиці 1.
Кількість Пікселі (мм) Площа (мм2) розмір (програма) розмір (розрахунок) розмір (програма) розмір (розрахунок) 1 0,5 0,5 0,2 0,25 2 1 1 0,5 0,5 3 1,5 1,5 0,7 0,75 4 2,0 2,0 1,0 1,0 5 2,4 2,5 1,2 1,25 6 2,9 3,0 1,4 1,5
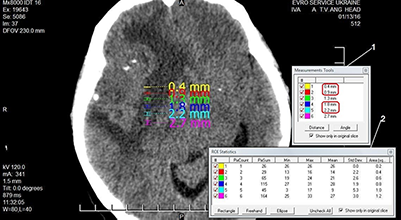
В іншої пацієнтки Ів., у якої поперечні зрізи головного мозку були виконані на тому ж апараті та за аналогічних умов, було отримано результати, подані на рисунку 2.
Отримані дані програмного визначення розміру пікселя, довжини та площі виділеної ділянки зображення, а також розрахункових значень розміру пікселя, довжини та площі зображення внесено до таблиці 2.
Кількість Пікселі (мм) Площа (мм2) розмір (програма) розмір (розрахунок) розмір (програма) розмір (розрахунок) 1 0,4 0,4 0,2 0,16 2 0,9 0,8 0,4 0,32 3 1,3 1,2 0,6 0,48 4 1,8 1,6 0,8 0,64 5 2,2 2,0 1,0 0,8 6 2,7 2,4 1,2 0,96
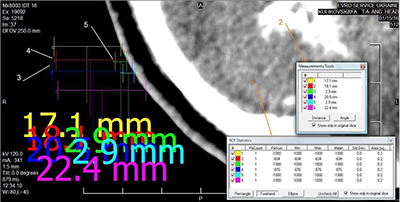
На рисунку 3 наведено результати вимірювання інструментами програми eFilm значень оптичної щільності чорного фону вздовж променя від краю зображення поперечного зрізу головного мозку пацієнтки К.
Розрахункові дані внесено до таблиці 3.
Ділянки Щільність (HU) % відповідності Відстань (мм) Різниця відстані (разів) 1 -1000 - 17,1 - По променю 2 -834 83,4 18,1 6,24 3 -1000 2,9 По променю 4 -876 87,6 20,5 7,07 5 -1000 2,9 6 -1000 - 22,4 -
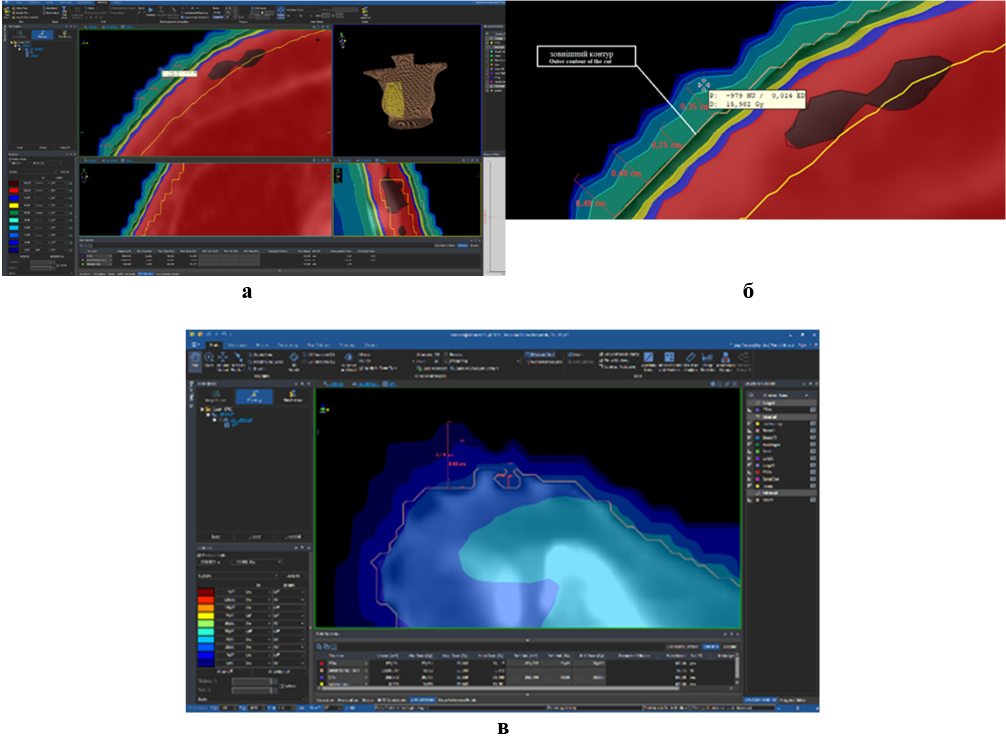
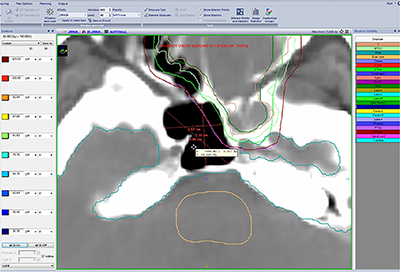
На рисунку 4 а, б, в наведено результати визначення поглинутих доз та оптичної щільності програмою планувальної системи на різних відстанях від зовнішнього контура.
Результати вимірювання поглинутої дози поза межами зовнішнього контура поперечного зрізу наведено в таблиці 4.
Номер заміру Відстань від зовнішнього контура поперечного зрізу (мм) Оптична цільність (HU) Поглинута доза (Гр) 1 4,0 –1001 5,9 2 3,5 –999 8,6 3 3,0 –979 16 4 1,5 –535 28
Наступні зображення (рис. 5 а, б) демонструють різні значення поглинутої дози в чорному фоні поза межами зрізу за однакових значень оптичної щільності.
На рисунку 6 наведено зображення поперечного зрізу пацієнта з раком носоглотки.
Сьогодні в плануванні променевої терапії засоби обробки та аналізу інформації на основі DICOM-файлів використовуються понад 30 років і стали міжнародним стандартом медичного зображення [28, 29]. МАГАТЕ (2021) наголосила на застосуванні DICOM-файлів на всіх етапах променевої терапії – діагностиці, дозиметрії, плануванні та реалізації лікування [45, 31].
Раніше нами були наведені результати щодо невизначеностей у рівномірності опромінення тканин за рахунок значущої розбіжності значень оптичної щільності суміжних пікселів та вокселів [30]. Аналіз даних вимірювання розміру пікселів та їхніх похідних у пацієнтки К. (рис. 1, табл. 1) показав таке.
Програмою визначено довжину сторони одного пікселя – 0,5 мм. До четвертого пікселя включно розмір відрізка залишався коректним, але між четвертим та п’ятим пікселем відстань мала бути 2,5 мм, тоді як фактично вона дорівнювала 2,4 мм. Виявлено також розбіжності між результатами визначення площі пікселя програмою (зображення 2, рис. 1) та ручним розрахунком. Програма показала площу 0,2 мм2, але з урахуванням розміру сторони пікселя (зображення 1, рис. 1) площа мала б становити 0,25 мм2. Для ділянок з двох та чотирьох пікселів площа, визначена програмою, збігалася з ручними розрахунками. Для ділянки з трьох пікселів відмінність становила 7,1%, з п’яти – 4,2%, з шести – 7,1%. Цілком можливо, що при збільшенні розмірів ділянки похибка виявить системність характеру, але точність планування променевої терапії ґрунтується на характеристиках вокселя, який складається з окремих пікселів, тому будь-які похибки в DICOM-файлах, що вважаються «золотим стандартом» якості медичного зображення, – неприпустимі.
В іншої пацієнтки (рис. 2, табл. 2) отримано інші результати, але теж з відмінностями. Як видно з даних, наведених у таблицях, в обох випадках спостерігається некоректне визначення програмою «eFilm» розмірів пікселя, довжини виділеної ділянки зображення та її площі, значення яких перевіряли ручними арифметичними розрахунками.
Так, у першому випадку на зрізі пацієнтки К. розмір пікселя становив 0,5 см, однак розмір відрізка з шести пікселів зменшився між четвертим та п’ятим пікселем (2,0 мм-2,4 мм), тобто замість 0,5 мм становив 0,4 мм, після чого знову дорівнював 0,5 мм (2,4 мм-2,9 мм). При аналізі програмного розрахунку площі виявилася певна закономірність. Площа з першого по другий піксель змінилася на 0,3 мм2, з другого по третій – на 0,2 мм2 , з третього по четвертий – знов на 0,3 мм2, з четвертого по п’ятий – на 0,2 мм2, з п’ятого по шостий – знов на 0,2 мм2, порушивши попередню послідовність. Можливо, при збільшенні кількості вимірювань та розрахунків закономірність виявилася би більш чіткою, але на цьому етапі її слід вважати відсутньою, а похибку програми – випадковою [14].
У пацієнтки Ів. аналіз даних, наведених у таблиці 2, виявив системну похибку 10% щодо площі зображення пікселів та 11% – щодо розмірів пікселів. При цьому фізичні умови томографії обох хворих були однаковими. Загалом проведений непараметричний аналіз програмних та розрахункових даних щодо геометричних невизначеностей виявив похибку 8-15% (статистична значущість визначалася за порогом p<0,025) залежно від того, яка ділянка розглядається – у центрі чи на периферії.
Слід зазначити, що в самому стандарті DICOM (https://www.dicomstandard.org/current) наведено перелік можливих причин порушень при відтворенні зображень. Найбільш схильними до геометричних спотворень є зображення, отримані МРТ (магнітно-резонансна томографія). У центрі поля зору (isocenter) типове середнє спотворення становить близько 0,4-0,8 мм, на периферії (на відстані 200 мм від центру) спотворення може зростати до 2-5 мм і більше. Для стереотаксичної радіохірургії критично важлива точність – похибка понад 1 мм для малих цілей (менше 20 мм) може вважатися клінічно неприйнятною (втрата якості/точності понад 5% в індексах планування). КТ (комп'ютерна томографія) та рентгенографія мають набагато менші геометричні спотворення, ніж МРТ, за винятком ефектів проекції (наприклад, видовження або вкорочення кісток на звичайному рентгенівському знімку через кут зйомки). При КТ спотворення можуть спричиняти різницю в розрахунках об'єму певних структур мозку (наприклад, кори) до 5,5% при порівнянні скоригованих і нескоригованих зображень. Відносне спотворення може бути від менше ніж 1% (у добре каліброваних системах КТ або в центрі поля зору МРТ) до понад 10-20% відносного відхилення розміру на периферії зображення. Це не просто «втрата якості» в загальному розумінні, а критична втрата геометричної точності (зміна розмірів пікселів/вокселів), що впливає на клінічну достовірність зображення [46].
Таким чином, у проведеному дослідженні спостерігали зміну розміру пікселів/вокселів в отриманих зображеннях – неточність, яка вже закладена в самому стандарті та може призвести до дуже серйозних наслідків при плануванні лікування.
Особливу увагу слід звернути на значення оптичної щільності поза зовнішніми контурами зображення об’єкта (чорний фон). Аналіз даних (рис. 3 та табл. 3) показав, що оптична щільність поза зображенням досліджуваної області («чорний фон», «нуль пікселів зображення») у першій парі по променю (2, 3) на відстані 18,1 мм дорівнює -834 HU, а на відстані 2,9 мм вона становить -1000 HU, тобто менша оптична щільність чорного фону знаходиться в 6,24 раза ближче до краю зображення поперечного зрізу черепа, ніж оптична щільність -834 HU, що суперечить очікуваній закономірності. У другій парі (4, 5) ця відстань ще більша – 7,07 раза.
Отже, оптична щільність чорного фону змінюється по променю від -1000 HU поблизу межі об'єкта, що досліджується, до -834 HU на відстані в 7 разів далі. Наявність ділянок різнорідної щільності поза зображенням зрізу, на тлі «абсолютного нуля», не виключає можливість аналогічних артефактів і на головному об'єкті – зображенні поперечного зрізу пацієнта. Це може негативно впливати на оцінку результатів лікування, а також на формування плану подальшої терапії, якщо в основу будуть покладені некоректні дані, оскільки дози для фотонної променевої терапії безпосередньо пов'язані зі значеннями Хаунсфілда (HU), отриманими з комп'ютерної томографії [47].
При аналізі результатів поглинутих доз та оптичної щільності, які визначила програма планувальної системи (рис. 4 а, б, в, табл. 4), можна констатувати, що на відстані 4 мм від зовнішнього контура поперечного зрізу при оптичній щільності зображення -1001 HU поглинута доза дорівнює 5,9 Гр. При зменшення відстані – доза зростає. Але зовнішній контур зображення поперечного зрізу, який окреслює лікар, є межею, де дія програми мала б припинитися. Разом з тим цього не відбувається і програма продовжує формувати план майбутнього опромінення. Отже аналогічні дії програми можуть відбуватися і за межами інших контурів, критично важливих – PTV, GTV та нормальних тканин. Така невизначеність може стати причиною некоректних значень поглинутих доз в об’ємах інтересу та призвести до погіршення результатів лікування пацієнта.
Привертає увагу наявність різних значень поглинутої дози в чорному фоні поза межами зрізу з однаковим значенням оптичної щільності (рис. 5 а, б). При однаковій оптичній щільності чорного фону -992 HU, на одному поперечному зрізі поглинута доза в одному вимірюванні дорівнювала 0,0 Гр, що відповідає фізичним закономірностям поглинання енергії випромінювання, тоді як в іншому вимірюванні вона становила 15,4 Гр, що пояснити складно.
Наступний приклад стосується поглинутої дози в повітрі порожнини основної пазухи (рис. 6). Якщо попередні результати складно пояснити, але вони не впливали на опромінення тканин хворого, бо знаходилися поза межами зовнішнього контура зрізу, то в цьому випадку виміряна поглинута доза в повітрі порожнини основної пазухи знаходиться всередині поперечного зрізу, поряд з пухлиною та критичними тканинами. Невизначеність полягає у великій поглинутій дозі – 56,2 Гр, яку визначає програма планувальної системи в повітряній порожнині основної пазухи. При цьому розміри порожнини досить великі, 3,05×2,3 см, а оптична щільність -994 HU.
Дослідження периферичних доз у пацієнтів є важливою задачею, оскільки буде вплив на сусідні органи та тканини, що знаходяться в зоні ризику. Слід зазначити, що під час лікування з використанням іонізуючого випромінення має вплив розсіювання, яке виникає як від компонентів прискорювача (утворюючи клінічно неприйнятну півтінь), так і від самого пацієнта. Це може сприяти збільшенню дози опромінення в тканинах за межами області лікування [48].
Резюмуючи, слід зазначити, що нами здійснено спробу визначити чинники, які можуть впливати на точність планування променевої терапії онкологічних хворих з використанням наведеної технології та відповідних засобів. Розбіжність між принципом недопущення перевищення толерантної дози для нормальних тканин і високою частотою променевих ушкоджень у більшості пацієнтів у світі може бути зменшена шляхом виявлення та усунення невизначеностей на будь-якому етапі радіаційної технології лікування. У перспективі планується системне дослідження невизначеностей у різних планувальних системах, проведення калібрування HU, аналіз впливу розміру вокселя та геометричних похибок на дозиметричні параметри, а також оцінювання потенціалу застосування штучного інтелекту для підвищення точності планування.
ВИСНОВКИ
1. Проведений аналіз показав, що програма формування зображень у форматі DICOM та програмне забезпечення планування променевої терапії на електронному прискорювачі можуть давати результати з різними видами похибок. Ці похибки зумовлюють невизначеності у визначенні поглинутих доз, що потенційно може призвести до зниження ефективності лікування онкологічних хворих.
2. Ймовірним шляхом зменшення похибок може бути удосконалення програмного забезпечення для обробки та аналізу DICOM-файлів рентген-комп’ютерної томографії, а також програмного забезпечення планувальних систем променевої терапії. Інтеграція технологій штучного інтелекту в процес планування променевої терапії відкриває нові можливості для підвищення ефективності та стандартизації, однак водночас формує нові джерела невизначеності, що потребують ретельного контролю якості та експертної оцінки.
Внески авторів:
Кіхтенко І.М. – концептуалізація, методологія, написання – початковий проєкт;
Хворостенко Ю.М. – дослідження, ресурси, курація даних, візуалізація;
Філоненко Н.Ю. – методологія, формальний аналіз, написання – рецензування та редагування;
Галдіна О.М. – формальний аналіз, написання – рецензування та редагування.
Фінансування. Дослідження не має зовнішніх джерел фінансування.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів.
REFERENCES
1. World Health Organization. Global cancer burden growing amidst mounting need for services [Internet]. 2024 [cited 2025 Dec 12]. Available from: https://www.who.int/news/item/01-02-2024-global-cancer-burden-growing--amidst-mounting-need-for-services
2. Siegel RL, Kratzer TB, Giaquinto AN, Sung H, Jemal A. Cancer statistics, 2025. CA Cancer J Clin. 2025;75(1):10-45. doi: https://doi.org/10.3322/caac.21871
3. Liu B, Zhou H, Tan L, Siu KTH, Guan XY. Exploring treatment options in cancer: tumor treatment strategies. Signal Transduct Target Ther. 2024;9:175. doi: https://doi.org/10.1038/s41392-024-01856-7
4. Fedorenko ZP, Gorokh Ye, Ryzhov A, Soumkina O. [Cancer in Ukraine, 2023-2024: Incidence, Mortality, and Performance Indicators of the Oncology Service]. Bull Natl Cancer Regist Ukr. Vol. 26. [Internet]. Kyiv; 2025 [cited 2025 Dec 12]. Ukrainian. Available from: http://www.ncru.inf.ua/publications/BULL_26/PDF_E/0-titul.pdf
5. Zafar A, Khatoon S, Khan MJ, Abu J, Naeem A. Advancements and limitations in traditional anti-cancer therapies: a comprehensive review. Discov Onc. 2025;16:607. doi: https://doi.org/10.1007/s12672-025-02198-8
6. Desai I, Thakur S, Pagariya P. Current advances in immunotherapy for cancer. Oral Oncol Rep. 2024;12:100652. doi: https://doi.org/10.1016/j.oor.2024.100652
7. Portik D, Lacombe D, Faivre-Finn C, Achard V, Andratschke N, Correia D, et al. The 2024 State of Science report from the the European Organisation for Research and Treatment of Cancer’s Radiation Oncology Scientific Council. Eur J Cancer. 2025;220:115334. doi: https://doi.org/10.1016/j.ejca.2025.115334
8. World Health Organization/IAEA. New WHO/IAEA publication provides guidance on radiotherapy equipment to fight cancer [Internet]. 2021 [cited 2025 Dec 12]. Available from: https://www.who.int/news/item/05-03-2021-new-who-iaea-publication-provides-guidance-on-radiotherapy-equipment-to-fight-cancer
9. Majeed H, Gupta V. Adverse effects of radiation therapy. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan [cited 2025 Dec 12]. Available from: https://www.ncbi.nlm.nih.gov/books/NBK563259/
10. Catalano O, Fusco R, Carriero S, Tamburrini S, Granata V. Ultrasound findings after breast cancer radiation therapy. Korean J Radiol. 2024;25(11):982-91. doi: https://doi.org/10.3348/kjr.2024.0672
11. Moisander M, Skyttä T, Kivistö S, et al. Radiotherapy-induced diffuse myocardial fibrosis in early-stage breast cancer patients. Radiat Oncol. 2023;18(1):124. doi: https://doi.org/10.1186/s13014-023-02319-z
12. Singh P, Mishra A, Mishra SK. Challenges and potential side effects of radiation therapy for palliative cancer treatment. Med Palliative. 2024;23(2):75-91. doi: https://doi.org/10.1016/j.medpal.2023.12.002
13. Ohno T, Kamiguchi A, Honda M, Shimohigashi Y, Kuraoka A, Toyota M, et al. Enhancing patient positioning precision: a comparative analysis of surface-guided radiation therapy systems. Radiol Phys Technol. 2025 Sep;18(3):833-50. doi: https://doi.org/10.1007/s12194-025-00937-8
14. International Atomic Energy Agency. Accuracy requirements and uncertainties in radiotherapy. [Internet]. Vienna: International Atomic Energy Agency; 2016 [cited 2025 Dec 12]. (IAEA Human Health Series. No. 31). Available from: https://www-pub.iaea.org/MTCD/Publications/PDF/P1679_HH31_web.pdf
15. International Atomic Energy Agency. Handbook of basic quality control tests for diagnostic radiology. [Internet]. Vienna: International Atomic Energy Agency; 2023 [cited 2025 Dec 12]. (IAEA Human Health Series. No. 47). Available from: https://www-pub.iaea.org/MTCD/Publications/PDF/PUB2021_web.pdf
16. International Atomic Energy Agency. Absorbed dose determination in external beam radiotherapy. [Internet]. Vienna: International Atomic Energy Agency; 2024 [cited 2025 Dec 12]. (Technical Reports Series. No. 398 (Rev. 1)). Available from: https://www-pub.iaea.org/MTCD/Publications/PDF/TRS398_scr.pdf
17. International Atomic Energy Agency. Dosimetry in Brachytherapy – An International Code of Practice for Secondary Standards Dosimetry Laboratories and Hospitals. [Internet]. Vienna: International Atomic Energy Agency; 2023 [cited 2025 Dec 12]. (Technical Reports Series. No. 492). Available from: https://www-pub.iaea.org/MTCD/Publications/PDF/DOC-010-492_web.pdf
18. American Association of Physicists in Medicine. Physical Uncertainties in the Planning and Delivery of Light Ion Beam Treatments: The Report of AAPM Task Group 202. [Internet]. Alexandria (VA): AAPM; 2020 [cited 2025 Dec 12]. 124 p. (AAPM Report. No. 202). Available from: https://www.aapm.org/pubs/reports/RPT_202.pdf
19. Siochi RA, Balter P, Bloch CD, Santanam L, Blodgett K, Curran BH, et al. Report of Task Group 201 of the American Association of Physicists in Medicine: quality management of external beam therapy data transfer. Med Phys. 2021;48:e86-114. doi: https://doi.org/10.1002/mp.14868
20. Brock KK, Mutic S, McNutt TR, Li H, Kessler ML. Use of image registration and fusion algorithms and techniques in radiotherapy: report of the AAPM Radiation Therapy Committee Task Group No. 132. Med Phys. 2017;44:e43-76. doi: https://doi.org/10.1002/mp.12256
21. Bissonnette JP, Balter PA, Dong L, Langen KM, Lovelock DM, Miften M, et al. Quality assurance for image-guided radiation therapy utilizing CT-based technologies: a report of the AAPM TG-179. Med Phys. 2012;39:1946-63. doi: https://doi.org/10.1118/1.3690466
22. Matuszak N, Kruszyna-Mochalska M, Skrobala A, Ryczkowski A, Romanski P, Piotrowski I, et al. Nontarget and out-of-field doses from electron beam radiotherapy. Life. 2022;12(6):858. doi: https://doi.org/10.3390/life12060858
23. Maharaj KD, Dass J, Ibrahim M, Mahmood T, Rowshanfarzad P. Peripheral Doses Beyond Electron Applicators in Conventional C-Arm Linear Accelerators: A Systematic Literature Review. Technology in Cancer Research & Treatment. 2024;23:15330338241239144. doi: https://doi.org/10.1177/15330338241239144
24. Gul OV. Experimental evaluation of out-of-field dose for different high-energy electron beams and applicators used in external beam radiotherapy. Radiat Phys Chem. 2024;215:111345. doi: https://doi.org/10.1016/j.radphyschem.2023.111345
25. Maharaj KD, Sabet M, Dass J, Ibrahim M, Mahmood T, Rowshanfarzad P. Comprehensive analysis of peripheral dose in electron beam therapy with a Varian TrueBeam Linac. Radiat Med Prot. 2025;6(1):28-36. doi: https://doi.org/10.1016/j.radmp.2024.10.003
26. Maharaj KD, Dass J, Ibrahim M, Mahmood T, Rowshanfarzad P. Peripheral doses beyond electron applicators in conventional C-arm linear accelerators: a systematic literature review. Technol Cancer Res Treat. 2024;23:1-9. doi: https://doi.org/10.1177/15330338241239144
27. van den Berg CAT, Meliadò EF. Uncertainty assessment for deep learning radiotherapy applications. Semin Radiat Oncol. 2022;32(4):304-18. doi: https://doi.org/10.1016/j.semradonc.2022.06.001
28. Yang L. DICOM standard and its application in radioinformatics. Int J Comput Sci Inf Technol. 2024;2(1):384-90. doi: https://doi.org/10.62051/ijcsit.v2n1.40
29. Larobina M. Thirty years of the DICOM standard. Tomography. 2023;9:1829-38. doi: https://doi.org/10.3390/tomography9050145
30. Khvorostenko MI, Kikhtenko IM, Khvorostenko YM. [Influence of tumor tissue heterogeneity on the quality of radiotherapy planning]. [Internet]. Ukr Radiol J. 2016 [cited 2025 Dec 12];24(2):67-72. Ukrainian. Available from: https://irbis-nbuv.gov.ua/cgi-bin/irbis_nbuv/cgiirbis_64.exe?C21COM=2&I21DBN=UJRN&P21DBN=UJRN&IMAGE_FILE_DOWNLOAD=1&Image_file_name=PDF/URLZh_2016_24_2_16.pdf
31. Moeller TB, Reif E. Normal findings in CT and MRI [Internet]. Stuttgart: Thieme; 2000 [cited 2025 Dec 12]. 256 p. Available from: https://radoir.org/en/wp-content/uploads/2018/06/NFCTMRI.pdf
32. Rasmussen ME, Akbarov K, Titovich E, et al. Potential of e-learning interventions and artificial intelligence-assisted contouring skills in radiotherapy: the ELAISA study. JCO Glob Oncol. 2024;10:e2400173. doi: https://doi.org/10.1200/GO.24.00173
33. Maduro Bustos LA, Sarkar A, Doyle LA, Andreou K, Noonan J, Nurbagandova D, et al. Feasibility evaluation of novel AI-based deep-learning contouring algorithm for radiotherapy. J Appl Clin Med Phys. 2023;24(11):e14090. doi: https://doi.org/10.1002/acm2.14090
34. Hu Y, Nguyen H, Smith C, Chen T, Byrne M, Archibald-Heeren B, et al. Clinical assessment of a novel machine-learning automated contouring tool for radiotherapy planning. J Appl Clin Med Phys. 2023;24(7):e13949. doi: https://doi.org/10.1002/acm2.13949
35. D'Aviero A, Re A, Catucci F, Piccari D, Votta C, Piro D, et al. Clinical Validation of a Deep-Learning Segmentation Software in Head and Neck: An Early Analysis in a Developing Radiation Oncology Center. Int J Environ Res Public Health. 2022;19(15):9057. doi: https://doi.org/10.3390/ijerph19159057
36. Finnegan RN, Quinn A, Horsley P, Chan J, Stewart M, Bromley R, et al. Geometric and dosimetric evaluation of a commercial AI auto-contouring tool on multiple anatomical sites in CT scans. J Appl Clin Med Phys. 2025;26(6):e70067. doi: https://doi.org/10.1002/acm2.70067
37. Soltaninejad A, Shahbazi-Gahrouei D, Khorasani A, Hemati S. Evaluation of CNN-based deep learning models for auto-contouring in glioblastoma radiotherapy: a review. Radiat Oncol. 2025;20(1):169. doi: https://doi.org/10.1186/s13014-025-02748-y
38. International Atomic Energy Agency. Setting Up a Radiotherapy Programme. [Internet]. Vienna: International Atomic Energy Agency; 2008 [cited 2025 Dec 12]. Available from: https://www-pub.iaea.org/MTCD/Publications/PDF/pub1296_web.pdf
39. International Atomic Energy Agency. A Handbook for the Education of Radiation Therapists (RTTs). [Internet]. Vienna: International Atomic Energy Agency; 2014 [cited 2025 Dec 12]. (Training Course Series. No. 58). Available from:
https://www-pub.iaea.org/MTCD/Publications/PDF/TCS-58_web.pdf
40. Brown SR, Van Hemelrijck M, Price G, Oppong FB, Verhoeff JJC, Faivre-Finn C. Novel methodologies for clinical research in radiation oncology: Time to think outside of the box? A narrative review. Radiother Oncol. 2025 Dec 9:111311. doi: https://doi.org/10.1016/j.radonc.2025.111311
41. Green H, Rieu R, Slevin F, Ashmore L, Bulbeck H, Gkogkou P, et al. CTRad Working Group 4. Best practice for patient-centred radiotherapy in clinical trials and beyond: A national multidisciplinary consensus. Clin Oncol (R Coll Radiol). 2025;39:103732. doi: https://doi.org/10.1016/j.clon.2024.103732
42. Schaue D, McBride WH. Opportunities and challenges of radiotherapy for treating cancer. Nat Rev Clin Oncol. 2015 Sep;12(9):527-40. doi: https://doi.org/10.1038/nrclinonc.2015.120
43. Schober P, Vetter TR. Nonparametric Statistical Methods in Medical Research. Anesth Analg. 2020;131(6):1862-3. doi: https://doi.org/10.1213/ANE.0000000000005101
44. Bonnini S, Assegie GM, Trzcinska K. Review about the Permutation Approach in Hypothesis Testing. Mathematics. 2024;12(17):2617. doi: https://doi.org/10.3390/math12172617
45. World Health Organization. Technical specifications of radiotherapy equipment for cancer treatment. [Internet]. Geneva: WHO; 2021 [cited 2025 Dec 12]. Available from: https://www.oncologysystems.com/wp-content/uploads/2021/03/2021-Handbook-on-Radiotherapy-Equipment.pdf
46. Mabizela S. Navigating parametric and non-parametric statistical analyses: a practical guide in health sciences research. Wits J Clin Med. 2025;7(1):41-4. doi: https://doi.org/10.18772/26180197.2025.v7n1a9
47. Mohan R. A review of proton therapy – Current status and future directions. Prec Radiat Oncol. 2022;6:164-76. doi: https://doi.org/10.1002/pro6.1149
48. Mendes RMS, Silva MG, Rebello WF, Oliveira CL, Stenders RM, Medeiros MPC, et al. Influence of radiotherapy room shielding on ambient dose equivalent due to photons H(10)p and neutrons H(10)n in the patient’s plane. Appl Radiat Isot. 2022;181:110095. doi: https://doi.org/10.1016/j.apradiso.2021.110095


 UK
UK  EN
EN