Ключові слова: Фламідез, диклофенак, люмбаго, люмбоішіалгія, ефективність, безпека, обсерваційне дослідження
Key words: Flamidase, diclofenac, lumbago, lumbosciatica, efficacy, safety, observational study
Реферат
Біль у поперековій ділянці (люмбалгія) посідає одне з провідних місць серед причин тимчасової непрацездатності в економічно активного населення в усьому світі, включаючи Україну. Нестероїдні протизапальні препарати на сьогодні залишаються препаратами першої лінії при лікуванні вертеброгенних больових синдромів, забезпечуючи анальгетичну та протизапальну дію, проте їх призначення обмежено гастропатіями. Фламідез – комбінований препарат на основі диклофенаку калію та парацетамолу, що містить також ензим серратіопептидазу. Така комбінація дозволяє досягати синергічного ефекту: парацетамол посилює анальгезивну дію диклофенаку калію, зменшуючи потребу в підвищенні дози нестероїдного протизапального препарату, а серратіопептидаза додатково чинить протизапальний та протинабряковий ефект. Метою роботи було оцінити ефективність та безпеку комбінованого лікарського засобу Фламідез (диклофенак калію, парацетамол, серратіопептидаза) порівняно з диклофенаком натрію при лікуванні гострого болю в нижній частині спини (люмбаго, люмбоішіалгія). Проведено порівняльне проспективне багатоцентрове обсерваційне дослідження за участі 157 пацієнтів з 15 регіонів України. Учасників було розподілено на 4 групи залежно від нозології та застосованого препарату: люмбаго-диклофенак (n=29), люмбоішіалгія-диклофенак (n=49), люмбаго-Фламідез (n=25), люмбоішіалгія-Фламідез (n=54). Ефективність оцінювали за динамікою больового синдрому з 1 до 7 дня лікування, безпеку – за активністю ферментів-трансаміназ (АЛТ, АСТ) у плазмі крові, а також суб’єктивними проявами побічних реакцій (нудота, біль у животі тощо). Як диклофенак натрію, так і Фламідез демонструють ефективність у зниженні інтенсивності болю в попереку, при цьому Фламідез значуще перевершує диклофенак за вираженістю та швидкістю розвитку анальгезивного ефекту (особливо при ноцицептивному компоненті). Середнє зменшення інтенсивності болю (ΔВАШ) за 7 днів лікування становило 5,76 бала в групі Фламідезу проти 4,12 бала в групі диклофенаку натрію, що є статистично значущим (p<0,05). У пацієнтів з люмбаго ΔВАШ становив 6,12 бала (Фламідез) проти 4,48 бала (диклофенак). У пацієнтів з люмбоішіалгією – 5,39 бала (Фламідез) проти 3,76 бала (диклофенак). Медіана ВАШ на 7-й день лікування: 0 балів у групі Фламідезу проти 2 балів у групі диклофенаку. У плані безпеки диклофенак натрію також дещо поступається Фламідезу, вірогідно (проте клінічно незначуще) збільшуючи активність АЛТ та АСТ, при цьому не було верифіковано статистично значущої різниці між препаратами за впливом на шлунок: побічні реакції з боку ШКТ спостерігались у 15% пацієнтів, які приймали диклофенак, і в 11%, які приймали Фламідез. Фламідез демонструє кращу за диклофенак натрію ефективність і безпеку при лікуванні гострого поперекового болю, особливо за наявності ноцицептивного компонента. Комбінована дія диклофенаку калію, парацетамолу та серратіопептидази забезпечує виражену анальгезивну дію, не створюючи при цьому додаткових гастральних та гепатобіліарних ризиків для пацієнта. Отримані результати свідчать, що комбінований препарат Фламідез може бути ефективним варіантом фармакотерапії гострого поперекового болю. Подальші рандомізовані контрольовані дослідження з більшим періодом спостереження необхідні для підтвердження цих результатів.
Abstract
Clinical efficacy and safety of Flamidase in the treatment of lumbar pain: results of a multicenter observational comparative study in Ukraine. Kononenko N.M., Tsyvunin V.V., Briukhanova T.O., co-authors (20)4. Pain in the lumbar region (lumbalgia) is one of the leading causes of temporary disability among the economically active population worldwide, including Ukraine. Nonsteroidal anti-inflammatory drugs remain the first-line treatment for vertebrogenic pain syndromes, providing analgesic and anti-inflammatory effects, but their use is limited by gastrointestinal disorders. Flamidase is a combination drug based on potassium diclofenac and paracetamol, which also contains the enzyme serratiopeptidase. This combination achieves a synergistic effect: paracetamol enhances the analgesic effect of potassium diclofenac, reducing the need to increase the dose of the nonsteroidal anti-inflammatory drug, while serratiopeptidase provides additional anti-inflammatory and anti-edema effects. The aim of the study was to evaluate the efficacy and safety of the combination drug Flamidase (potassium diclofenac, paracetamol, serratiopeptidase) compared to sodium diclofenac in the treatment of acute lower back pain (lumbago, lumbosciatica). A comparative prospective multicenter observational study was conducted involving 157 patients from 15 regions of Ukraine. Participants were divided into 4 groups depending on the nosology and the drug used: lumbago-Diclofenac (n=29), lumbosciatica-Diclofenac (n=49), lumbago-Flamidase (n=25), lumbosciatica-Flamidase (n=54). Efficacy was assessed based on the dynamics of pain syndrome from days 1 to 7 of treatment, safety was assessed based on the activity of transaminase enzymes (ALT, AST) in blood plasma, as well as subjective manifestations of side effects (nausea, abdominal pain, etc.). Both diclofenac sodium and Flamidase are effective in reducing the intensity of low back pain, with Flamidase significantly superior to diclofenac in terms of the severity and speed of the analgesic effect (especially in the nociceptive component). The average reduction in pain intensity (ΔVAS) over 7 days of treatment was 5.76 points in the Flamidase group versus 4.12 points in the diclofenac sodium group, which is statistically significant (p<0.05). In patients with lumbago, ΔVAS was 6.12 points (Flamidase) versus 4,48 points (diclofenac). In patients with lumbosciatica, it was 5.39 points (Flamidase) versus 3.76 points (diclofenac). The median VAS on the 7th day of treatment was 0 points in the Flamidase group versus 2 points in the diclofenac group. In terms of safety, diclofenac sodium is also slightly inferior to Flamidase, reliably (but clinically insignificantly) increasing ALT and AST activity, while no statistically significant difference between the drugs in terms of their effect on the stomach was verified: gastrointestinal side effects were observed in 15% of patients on diclofenac and 11% on Flamidase. Flamidase demonstrates better efficacy and safety compared to diclofenac sodium in the treatment of acute low back pain, especially in the presence of a nociceptive component. The combined action of potassium diclofenac, paracetamol, and seratopeptidase provides a pronounced analgesic effect without creating additional gastric and hepatobiliary risks for the patient. The results obtained indicate that the combination drug Flamidase may be an effective option for pharmacotherapy of acute low back pain. Further randomized controlled trials with a longer follow-up period are needed to confirm these results.
Біль у поперековій ділянці (люмбалгія) посідає одне з провідних місць серед причин тимчасової непрацездатності в економічно активного населення в усьому світі, включаючи Україну [1]. За даними Всесвітньої організації охорони здоров’я, до 80% людей хоча б раз у житті переживають епізод вираженого болю в попереку, що може мати як механічну, так і нейропатичну природу. Часті рецидиви, хронізація болю та пов’язане з цим зниження якості життя роблять проблему медико-соціальною та економічно значущою.
Найбільш поширеними клінічними формами гострого вертеброгенного болю є люмбаго (раптовий, гострий м’язово-зв’язковий біль у попереку, без іррадіації) та люмбоішіалгія (компресійно-нейропатичний біль з іррадіацією по ходу сідничного нерва), які часто асоціюються з міофасціальним синдромом, дегенеративно-дистрофічними змінами хребта, міжхребцевими грижами, фасетковим синдромом, спондилоартропатією та компресією корінців.
За даними Міністерства охорони здоров’я України та профільних інститутів, вертеброгенні больові синдроми посідають друге місце серед причин звернень до лікарів-неврологів, поступаючись лише судинним захворюванням мозку. Щороку понад 1,5 млн пацієнтів звертаються до медичних закладів із симптомами люмбалгії чи люмбоішіалгії [2].
Серед дорослого населення працездатного віку понад 40% осіб віком від 30 до 60 років повідомляють про епізоди болю в поперековій ділянці тривалістю понад 7 днів, а в 15-20% випадків цей біль рецидивує або хронізується [3]. Особливо тривожною є тенденція до зростання частоти первинної інвалідизації, спричиненої саме вертеброгенними ураженнями – до 5-6% щорічно.
За інформацією Національної служби здоров’я України (НСЗУ), у 2022 році понад 200 тисяч випадків було зареєстровано за кодами М54.3 (ішіас) та М54.5 (люмбалгія) згідно з МКХ-10. Ці показники значно зросли після пандемії COVID-19, що пов’язується з гіподинамією, порушенням постави при дистанційній роботі, зниженням фізичної активності населення.
Ураховуючи поліморфізм патогенезу, терапія потребує ретельного підбору фармакологічних засобів з урахуванням типу болю, тривалості та індивідуальних факторів ризику. У гострому періоді лікування основними завданнями є швидке та ефективне гальмування болю, зменшення запального процесу, нормалізація функціонального стану хребта, а також мінімізація ризику розвитку побічних реакцій фармакотерапії [4].
Нестероїдні протизапальні препарати (НПЗП) на сьогодні залишаються препаратами першої лінії при лікуванні вертеброгенних больових синдромів, забезпечуючи анальгетичну та протизапальну дію [5]. Диклофенак натрію залишається одним з найбільш поширених засобів цього фармакологічного класу завдяки доведеній ефективності в зменшенні інтенсивності болю та набряку [6]. Проте його призначення обмежене побічними діями, зокрема гастропатіями й гепатоксичністю [7, 8, 9, 10].
Останніми роками значну увагу привертають комбіновані препарати, зокрема Фламідез – комбінований препарат на основі диклофенаку калію та парацетамолу, що містить також ензим серратіопептидазу. Така комбінація дозволяє досягати синергічного ефекту: парацетамол посилює анальгезивну дію диклофенаку калію, зменшуючи потребу в підвищенні дози НПЗП, а серратіопептидаза додатково чинить протизапальний та протинабряковий ефект. Також диклофенак калію, що входить до складу Фламідезу, має доведені переваги над натрієвою сіллю диклофенаку у швидкості та вираженості ефекту. Існують також окремі дані щодо кращого профілю безпеки калієвої солі диклофенаку порівняно з натрієвою [11]. Серратіопептидаза при цьому є цінним ад’ювантом, що не лише вірогідно посилює знеболювальні та протизапальні властивості НПЗП, але й має потенціал до корекції можливих побічних ефектів диклофенаку [12, 13].
Фламідез продемонстрував високу клінічну ефективність при болю в спині, остеоартриті, міозитах, а також у лікуванні післяопераційного болю. За даними окремих досліджень, у пацієнтів, які отримували Фламідез, спостерігали не лише швидший знеболювальний ефект, але й також рідшу частоту виникнення побічних реакцій (у першу чергу диспептичних) [14].
Таким чином, комбіновані засоби на основі диклофенаку калію, такі як Фламідез, можуть становити альтернативу монотерапії класичними НПЗП, дозволяючи зменшити медикаментозне навантаження, особливо в пацієнтів із супутніми факторами ризику ураження шлунка та печінки.
Проте, незважаючи на широке застосування в клінічній практиці як монопрепаратів диклофенаку натрію, так і Фламідезу, порівняльна оцінка їхньої ефективності та безпеки для пацієнтів з гострим поперековим болем – як у контексті гастроінтестинальних ризиків, так і з урахуванням негативних впливів на функції печінки за змінами біохімічних маркерів аланінамінотрансферази (АЛТ) й аспартатамінотрансферази (АСТ) – залишається недостатньо дослідженою в українській популяції. Більшість наявних даних зосереджені на загальній ефективності знеболювання, тоді як фармакобезпека вивчена переважно на обмежених вибірках.
Зважаючи на вищезазначене, проведення багатоцентрового дослідження, спрямованого на порівняння ефективності та безпеки лікування Фламідезом та монотерапії диклофенаком натрію в пацієнтів з люмбаго та люмбоішіалгією, є актуальною, науково обґрунтованою та практично значущою задачею, що має важливе значення для оптимізації терапевтичних підходів у лікуванні вертеброгенних уражень та дозволить сформувати сучасні протоколи ефективної та безпечної терапії.
Сьогодні поняття «якість життя» є невід’ємною частиною системи охорони здоров’я, а також клінічних та медико-соціальних досліджень. У 1982 році Kaplan і Bush запровадили термін health-related quality of life (HRQoL – «якість життя, пов’язана зі здоров’ям»), що дозволило виділити параметри, які описують стан здоров’я, турботу про нього та якість медичної допомоги відповідно до загальної концепції якості життя [15].
Простота й легкість визначення методів візуально-аналогової шкали болю (ВАШ) дозволяє широко їх використовувати в багатьох різних ситуаціях. Надійність, валідність і можливість використання методів прямого рейтингу були продемонстровані в літературі [16]. Переваги ВАШ включають швидку адаптацію як у дослідницьких, так і в клінічних умовах. Також можна включити визначення балів за шкалою ВАШ для кожної з основних областей здоров’я, включаючи фізичне, соціальне та психічне здоров’я. Було встановлено, що лінія довжиною 10 см (100 мм) має найменшу похибку оцінювання порівняно з довжиною лінії 5 і 20 см. З точки зору психофізичного вимірювання, ВАШ вважається методом прямого оцінювання шкали та формою кросмодальності, у якій довжина лінії регулюється відповідно до інтенсивності болю [17].
Мета – оцінити ефективність та безпеку комбінованого лікарського засобу Фламідез (диклофенак калію, парацетамол, серратіопептидаза) порівняно з диклофенаком натрію при лікуванні гострого болю в нижній частині спини (люмбаго, люмбоішіалгія).
МАТЕРІАЛИ ТА МЕТОДИ ДОСЛІДЖЕНЬ
Дослідження мало дизайн проспективного обсерваційного багатоцентрового порівняльного дослідження, спрямованого на оцінювання ефективності та безпеки комбінованого лікарського засобу Фламідез порівняно з диклофенаком натрію в пацієнтів з гострим поперековим больовим синдромом.
Дослідження проводилося в період з березня до липня 2025 року за участю лікарів первинної ланки (сімейних лікарів та терапевтів), а також лікарів-неврологів з 15 регіонів України. У дослідження було включено 157 пацієнтів з клінічними діагнозами «люмбаго» або «люмбоішіалгія».
Пацієнти розподілялися на групи лікування відповідно до призначеної терапії в межах рутинної клінічної практики. Було сформовано чотири підгрупи залежно від клінічного діагнозу та застосованого препарату: люмбаго – диклофенак натрію (n=29), люмбоішіалгія – диклофенак натрію (n=49), люмбаго – Фламідез (n=25), люмбоішіалгія – Фламідез (n=54).
Фламідез призначали у формі таблеток у стандартній дозі 2 таблетки на добу (еквівалентно 100 мг диклофенаку калію). Диклофенак натрію (Ортофен-Форте) застосовували в дозі 100 мг на добу відповідно до інструкції для медичного застосування.
Критерії включення
До дослідження включали пацієнтів за наявності таких критеріїв:
1. Вік ≥18 років.
2. Наявність гострого поперекового болю тривалістю до 14 днів.
3. Клінічно встановлений діагноз люмбаго або люмбоішіалгія.
4. Підписана інформована згода на участь у дослідженні.
Критерії невключення
Пацієнти не включалися до дослідження за наявності:
- гіперчутливості до диклофенаку або компонентів досліджуваного препарату;
- застосування інших системних НПЗП протягом 48 годин до включення;
- застосування ацетилсаліцилової кислоти в кардіологічних дозах;
- тяжких порушень функції печінки або нирок;
- виразкової хвороби шлунка або дванадцятипалої кишки;
- тяжкої серцевої недостатності;
- вагітності або лактації;
- тяжких супутніх захворювань, що могли вплинути на результати оцінювання ефективності або безпеки терапії.
Пацієнтам дозволялося застосування базової терапії, включаючи місцеві форми нестероїдних протизапальних препаратів. Такий підхід відповідав умовам реальної клінічної практики, проте потенційно міг впливати на інтенсивність больового синдрому та швидкість його регресу, що враховувалося під час інтерпретації результатів дослідження.
Тривалість спостереження становила 7 днів для кожного пацієнта, що відповідає типовій тривалості лікування гострого поперекового болю.
Передбачалося два візити:
Початковий візит (1-й день) включав:
- перевірку відповідності критеріям включення/невключення;
- реєстрацію демографічних даних;
- клінічну оцінку інтенсивності болю за візуально-аналоговою шкалою (ВАШ, 0-10 балів);
- визначення рівнів печінкових ферментів (АЛТ, АСТ);
- підписання інформованої згоди;
- призначення терапії.
Пацієнтам видавали індивідуальну картку для щоденного самостійного оцінювання інтенсивності болю за шкалою ВАШ у період з 2-го до 6-го дня лікування.
Заключний візит (7-й день) включав:
- повторне оцінювання інтенсивності болю за ВАШ;
- збір щоденників самооцінки;
- повторне визначення рівнів АЛТ і АСТ;
- реєстрацію побічних реакцій, зокрема з боку шлунково-кишкового тракту (нудота, печія, біль або дискомфорт у животі).
Кінцеві точки дослідження
Первинною кінцевою точкою була зміна інтенсивності болю за візуально-аналоговою шкалою (ΔВАШ) між 1-м і 7-м днем лікування.
Вторинні кінцеві точки включали:
- щоденну динаміку інтенсивності болю за шкалою ВАШ;
- зміни рівнів печінкових трансаміназ (АЛТ, АСТ);
- частоту та характер побічних реакцій з боку шлунково-кишкового тракту.
Для оцінювання клінічної значущості змін використовували мінімально клінічно важливу різницю (MCID) для шкали ВАШ, що становить приблизно 1,5-2 бали.
Дослідження проводилося відповідно до принципів Гельсінської декларації Всесвітньої медичної асоціації. Усі учасники перед включенням підписали письмову інформовану згоду на участь у дослідженні. Протокол дослідження був схвалений комісією з питань біоетики Національного фармацевтичного університету (протокол № 5 від 25.03.2025 р.).
Статистичну обробку даних проводили за допомогою програмного забезпечення Statistica (версія 12), серійний номер ААА 12334567. Кількісні змінні наведено у вигляді медіани та міжквартильного розмаху (Me [Q1; Q3]). Категоріальні змінні наведені як абсолютна кількість та відсоток. Нормальність розподілу перевіряли за допомогою критерію Шапіро-Вілка. Для порівняння показників до та після лікування використовували парний t-критерій Стьюдента або критерій Вілкоксона залежно від характеру розподілу. Для міжгрупових порівнянь застосовували однофакторний дисперсійний аналіз (ANOVA) або критерій Краскела-Уолліса з відповідними post-hoc тестами (Тьюкі або Данна). Результати представлені з розрахунком 95% довірчих інтервалів (95% CI). Аналіз проводили за принципом per-protocol, оскільки всі включені пацієнти завершили період спостереження. Через відсутність втрат пацієнтів під час спостереження аналіз intention-to-treat не проводився. Статистично значущими вважали відмінності при p<0,05.
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
Демографічна характеристика учасників дослідження
За період проведення дослідження було залучено 157 пацієнтів з різних регіонів України, що забезпечило репрезентативність вибірки та можливість екстраполяції отриманих результатів на всю популяцію країни. Географічне охоплення було досить широким і включало 15 областей України: Дніпропетровську (n=19), Одеську (n=34), Полтавську (n=12), Київську (n=12), Тернопільську (n=9), Хмельницьку (n=10), Черкаську (n=9), Львівську (n=13), Харківську (n=9), Запорізьку (n=7), Миколаївську (n=6), Чернігівську (n=5), Вінницьку (n=4), Сумську (n=4) та Волинську (n=4).
Середній вік пацієнтів становив 51,4±14,2 року, що відповідає активній працездатній групі населення, для якої особливо важливим є швидке усунення больового синдрому. Розподіл пацієнтів за віковими групами показав, що найбільшу частку становили особи віком 43-59 років, що є типовим для захворювань опорно-рухового апарату.
Оцінка ефективності терапії
Динаміка больового синдрому в пацієнтів з різними формами болю в нижній частині спини наведена в таблиці 1.
Аналізуючи дані всіх пацієнтів, встановлено, що в початковий день лікування (1-й день) інтенсивність больового синдрому за ВАШ була високою та приблизно однаковою в обох групах (медіана 7 балів).
Препарат, кількість пацієнтів (n) ВАШ, бали 1-й день 2-й день 3-й день 4-й день 5-й день 6-й день 7-й день Усі пацієнти Диклофенак (n=78) 7 (5; 8) 6 (5; 8) 5 (4; 7) # 5 (3; 6) # 4 (3; 6) # 3 (2; 5) # 2 (1; 4) # Фламідез (n=79) 7 (6; 8) 6 (4; 7) # 4 (3; 6) #* 3 (2; 5) #* 2 (1; 4) #* 1 (1; 3) #* 0 (0; 1) #* Пацієнти з люмбаго Диклофенак (n=29) 6 (5; 8) 6 (5; 7) 5 (5; 7) 5 (4; 6) # 4 (3; 5) # 3 (2; 4) # 2 (1; 3) # Фламідез (n=25) 6 (6; 9) 5 (4; 7) # 4 (4; 5) #* 3 (2; 4) #* 2 (1; 3) #* 1 (0; 2) #* 0 (0; 1) #* Пацієнти з люмбоішіалгією Диклофенак (n=49) 7 (5; 8) 7 (4; 8) 6 (4; 7) # 5 (3; 7) # 4 (2; 6) # 3 (2; 5) # 2 (1; 4) # Фламідез (n=54) 7 (5; 8) 6 (4; 7) # 4 (3; 6) #* 3 (2; 5) #* 2 (2; 4) #* 1 (1; 3) #* 0 (0; 2) #* Примітки: n – кількість пацієнтів; # – достовірні відмінності порівняно з показником на 1-й день, р<0,05; * – достовірні відмінності порівняно з групою диклофенаку, р<0,05.
Протягом 7-денного курсу терапії в обох групах відзначалося поступове зниження болю, однак швидкість і вираженість цього зниження були різними для диклофенаку та Фламідезу. У групі диклофенаку зменшення вираженості болю набуло статистичної значущості порівняно з початковим рівнем лише на 3-й день, коли медіана ВАШ у цій групі знизилася до 5 балів (з 7 на початку; p<0,05 проти 1-го дня). Надалі показники болю в групі диклофенаку продовжували зменшуватися: медіана ВАШ становила 5 балів на 4-й день, 4 бали на 5-й день, 3 бали на 6-й день і 2 бали на 7-й день. Усі ці зміни були достовірними порівняно з початковим рівнем (p<0,05). Таким чином, за тиждень терапії диклофенаком інтенсивність болю зменшилася в середньому приблизно на 5 балів, до 2 балів на 7-й день, що вказує на суттєве полегшення больового синдрому, хоча в частини пацієнтів все ж зберігався помірний біль.
У цьому дослідженні комбінована терапія асоціювалася з більш швидким зниженням інтенсивності болю. Уже на 2-й день лікування інтенсивність болю достовірно знизилася порівняно з 1-м днем (p<0,05), тоді як у групі диклофенаку подібного достовірного поліпшення на 2-й день не спостерігалось. На 3-й день медіана болю в пацієнтів, які отримували Фламідез, становила 4 бали, що достовірно менше як вихідного рівня (p<0,05), так і показника групи диклофенаку на той самий день (p<0,05 між групами). З 3-го дня і до кінця спостереження різниця між групами зберігалася: показники ВАШ у групі Фламідезу були статистично нижчими, ніж у групі диклофенаку на кожному вимірюванні (p<0,05). Динаміка інтенсивності болю показувала щоденний регрес: на 4-й день медіана становила 3 бали, на 5-й – 2 бали, на 6-й – 1 бал. До кінця 7-го дня лікування в групі Фламідезу досягнуто майже повного регресу болю – медіана ВАШ становила 0 балів. Отже, за тиждень терапії комбінованим препаратом Фламідез інтенсивність болю знизилася приблизно на 7 балів (з 7 до 0), що свідчить про майже повне купірування больового синдрому в більшості пацієнтів.
Аналіз підгруп показав аналогічну тенденцію. Так, у пацієнтів з ізольованим люмбаго (поперековий біль без ішіасу, n=54) медіана початкового рівня болю становила 6 балів. У підгрупі диклофенаку достовірне зменшення болю настало лише на 4-й день лікування (p<0,05 проти початкового рівня); раніше (дні 2-3) різниця з базовим рівнем не досягала значущості. Натомість у підгрупі Фламідезу зниження болю при люмбаго досягло статистичної значущості вже на 2-й день (p<0,05). На 3-й день у цій підгрупі медіана ВАШ становила 4 бали, що достовірно нижче, ніж у групі диклофенаку (p<0,05 між групами). До 7-го дня лікування пацієнти з люмбаго, які отримували Фламідез, мали мінімальний залишковий біль (медіана 0 балів), тоді як у групі диклофенаку медіана становила 2 бали (p<0,05 між групами). Схожа картина спостерігалась і в пацієнтів з люмбаго, ускладненим ішіасом (n=103). У цій підгрупі диклофенак забезпечив достовірне полегшення болю з 3-го дня (p<0,05 проти 1-го дня), тоді як Фламідез знову ж таки спрацював швидше – вже на 2-й день відзначалось значуще зниження болю (p<0,05). Надалі різниця між препаратами виявилась ще більш вираженою: на 3-й день при застосуванні Фламідезу медіана ВАШ становила 4 бали проти 6 балів у групі диклофенаку (p<0,05), на 5-й день – 2 бали проти 4 балів відповідно (p<0,05). До кінця 7-го дня в підгрупі люмбоішіалгії медіана болю на фоні Фламідезу знизилась до 0 (міжквартильний розмах 0-2), що вказує на практично повне усунення болю, тоді як при лікуванні диклофенаком медіана становила 2 бали (міжквартильний розмах 1-4; p<0,05 між групами). Отже, в обох клінічних підгрупах комбінований препарат продемонстрував більш швидке настання анальгетичного ефекту та більш повне купірування болю порівняно з монотерапією диклофенаком натрію.
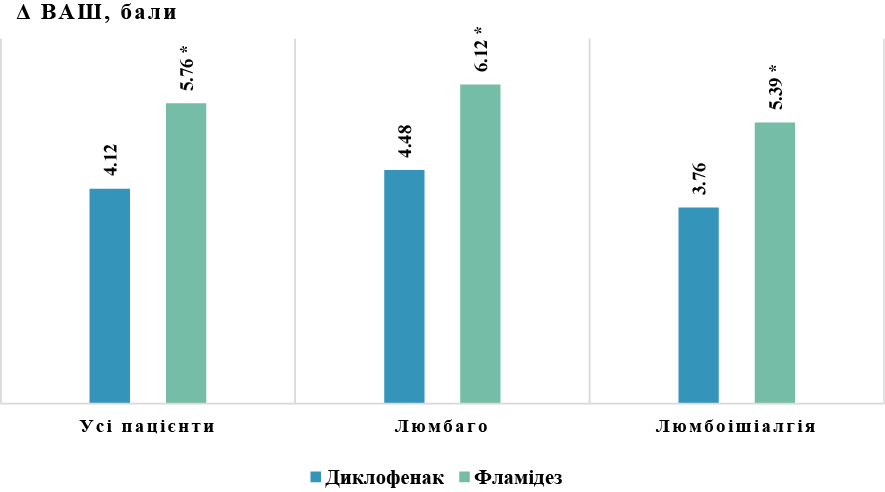
Середній показник зменшення болю Δ ВАШ (рис.), що його розраховували за різницею балів на початку та наприкінці лікування, становив 5,76 бала в групі Фламідезу проти 4,12 бала в групі диклофенаку (p<0,05) – для усіх пацієнтів. Аналогічно, у підгрупі пацієнтів з люмбаго зниження болю було більш вираженим при застосуванні Фламідезу (Δ ВАШ 6,12 бала проти 4,48 бала на тлі диклофенаку, p<0,05). У пацієнтів з люмбоішіалгією комбінована терапія також забезпечила кращий анальгезивний ефект: середній показник Δ ВАШ досягав 5,39 бала порівняно з 3,76 бала в групі диклофенаку (p<0,05). Таким чином, у всіх аналізованих категоріях пацієнтів комбінований препарат Фламідез забезпечив статистично достовірно більш виражену редукцію болю, аніж традиційна НПЗП-терапія диклофенаком натрію.
Важливо, що перевага Фламідезу спостерігалася як при ізольованому поперековому болю (люмбаго), так і при люмбоішіалгії, яка характеризується залученням корінцевого компонента болю. У хворих з люмбоішіалгією монотерапія диклофенаком виявилася менш ефективною (середнє зниження ВАШ становило 3,76 бала), ймовірно через більш інтенсивний запальний набряк та нейропатичний компонент болю. Застосування ж Фламідезу в якості фармакотерапевтичного агента дозволило суттєво посилити знеболювання в цій підгрупі пацієнтів (Δ ВАШ 5,39 бала), практично зрівнявши ступінь полегшення болю з таким у пацієнтів з люмбаго. Це свідчить, що комбінована дія диклофенаку калію, парацетамолу та серратіопептидази ефективно усуває як ноцицептивний, так і запально-компресійний (корінцевий) біль. Для пацієнтів з люмбаго ж отримані результати (Δ ВАШ 6,12 проти 4,48) вказують, що навіть при суто м’язово-скелетному болю в попереку мультимодальна анальгезія перевершує монотерапію: комбінований препарат зменшує біль майже на 40% ефективніше, ніж диклофенак натрію.
З погляду клінічної значущості, виявлені розбіжності між препаратами мають важливе практичне значення. Різниця приблизно в 1,6 бала за шкалою ВАШ на користь Фламідезу означає помітніше полегшення болю для пацієнта. Додаткова анальгезія, досягнута з Фламідезом, наближається до цього порогу або навіть перевищує його. Фактично пацієнти, які отримували Фламідез, у середньому відчули більше ніж на третину вираженіше полегшення болю порівняно з тими, хто отримував лише диклофенак. Така додана ефективність може означати перехід від помірного болю до легкого, що суттєво покращує здатність хворих до повсякденної активності та підвищує якість життя. У підгрупі з люмбоішіалгією, де початковий біль часто інтенсивніший і складніший для лікування, перевага комбінованої терапії (43% додаткового зниження болю на тлі Фламідезу проти диклофенаку) особливо підкреслює її клінічну цінність. Це вказує на те, що застосування мультимодального підходу дозволяє більш ефективно контролювати больовий синдром навіть за наявності корінцевого ураження.
Аналіз активності печінкових трансаміназ у пацієнтів
З метою оціювання безпечності терапії було проаналізовано зміни рівнів печінкових ферментів АЛТ та АСТ з 1-го до 7-го дня лікування (табл. 2).
Загалом по групах помітна різниця у впливі препаратів на ці показники. Аналізуючи дані всіх пацієнтів, визначено, що на тлі диклофенаку спостерігалося помірне підвищення рівнів АЛТ і АСТ за тиждень терапії, яке було статистично достовірним. Медіана АЛТ зросла з 26 Од/л (міжквартильний розмах 20,5-35) на 1-й день до 32 Од/л (25-41,5) на 7-й день (p<0,05 порівняно з початковим рівнем). Аналогічно, медіана АСТ підвищилася з 25 Од/л (20-32) до 30 Од/л (24-39) (p<0,05). Таким чином, монотерапія диклофенаком натрію була пов’язана з клінічно незначущою, але статистично вірогідною ескалацією рівня печінкових трансаміназ, що може вказувати на підвищене навантаження на печінку протягом лікування.
У групі Фламідезу змін показників печінкових ферментів майже не відбулося. Рівні АЛТ та АСТ залишалися близькими до початкових значень, і статистично значущого зростання не відзначено. Медіана АЛТ у групі Фламідезу становила 24 Од/л (19-34) на початку та 27 Од/л (21-34) на 7-й день, різниця статистично невірогідна (p>0,05). Медіана АСТ змінилася з 25 Од/л (18-31) до 27 Од/л (20-32) відповідно – різниця також статистично невірогідна. Важливо, що порівняння між групами в кінці дослідження продемонструвало достовірно нижчі значення трансаміназ у пацієнтів, які отримували Фламідез: на 7-й день рівні АЛТ та АСТ були вірогідно меншими в групі Фламідезу, ніж у групі диклофенаку (p<0,05). Іншими словами, диклофенак натрію спричиняв більш виражений вплив на печінкові показники, аніж комбінований препарат з калієвою сіллю диклофенаку.
Понял, добавил жирность текста (font-weight: bold;) ко всем ячейкам этого блока. Теперь и границы, и текст будут отображаться максимально «строго» и заметно. Вот готовый код: HTML Препарат, кількість пацієнтів (n) АЛТ, Од/л АСТ, Од/л 1-й день 7-й день 1-й день 7-й день Усі пацієнти Диклофенак (n=78) 26 (20,5; 35) 32 (25; 41,5) # 25 (20; 32) 30 (24; 39) # Фламідез (n=79) 24 (19; 34) 27 (21; 34) * 25 (18; 31) 27 (20; 32) * Пацієнти з люмбаго Диклофенак (n=29) 25 (21; 39) 31 (25; 41) # 25 (20; 31) 30 (23; 37) # Фламідез (n=25) 22,5 (19; 39) 26 (21; 36) * 25 (18; 29) 24,5 (20; 30) * Пацієнти з люмбоішіалгією Диклофенак (n=49) 26,5 (21; 31) 33,5 (25; 42) # 25 (17; 32) 32 (25; 39) # Фламідез (n=54) 25,5 (19; 33) 27 (20; 33) * 24,5 (19,5; 31) 27,5 (21; 32) * Примітки: n – кількість пацієнтів; # – достовірні відмінності порівняно з показником на 1-й день, р<0,05; * – достовірні відмінності порівняно з групою диклофенаку, р<0,05.
Подібні відмінності зафіксовано і при роздільному аналізі підгруп. У пацієнтів з люмбаго монотерапія диклофенаком натрію супроводжувалась зростанням АЛТ з медіани 25 до 31 Од/л за 7 днів (p<0,05) та АСТ з 25 до 30 Од/л (p<0,05). Натомість у підгрупі Фламідезу при люмбаго зміни АЛТ/АСТ були мінімальні та недостовірні (медіани АЛТ 22,5 → 26 Од/л; АСТ 25 → 24,5 Од/л; p>0,05), причому кінцеві рівні знову були нижчими, ніж на тлі диклофенаку (p<0,05 між групами). У пацієнтів з люмбоішіалгією спостерігали аналогічну ситуацію: у групі диклофенаку АЛТ зріс з 26,5 до 33,5 Од/л (p<0,05), АСТ – з 25 до 32 Од/л (p<0,05); тоді як при застосуванні Фламідезу зміни були несуттєвими (АЛТ 25,5 → 27 Од/л, АСТ 24,5 → 27,5 Од/л; p>0,05), причому медіанні рівні ферментів на 7-й день виявились достовірно нижчими, аніж у групі диклофенаку (p<0,05).
Отже, комбінований препарат Фламідез продемонстрував більш сприятливу динаміку показників печінкових трансаміназ протягом періоду спостереження. Водночас ці результати слід інтерпретувати обережно, оскільки спостереження тривало лише 7 днів і відображає переважно короткострокову реакцію організму на терапію. Для більш повної оцінки можливого впливу лікування на функціональний стан печінки необхідні дослідження з тривалішим періодом спостереження.
Оцінка частоти побічних реакцій з боку ШКТ
Оцінювання побічних ефектів з боку шлунково-кишкового тракту (ШКТ) виявило, що обидва препарати загалом добре переносились, проте частота шлунково-кишкових розладів була трохи вищою в групі диклофенаку натрію (табл. 3). За час спостереження мінімум одну побічну реакцію з боку ШКТ відзначили 12 із 78 пацієнтів, які отримували диклофенак (15%), у той час як у групі Фламідезу таких пацієнтів було 9 із 79 (11%). Різниця в загальній частоті шлунково-кишкових побічних явищ між групами не досягла статистичної значущості (p>0,05), але демонструвала тенденцію до кращої переносимості Фламідезу. Подібна картина спостерігалася і в підгрупах: при люмбаго частота гастроінтестинальних побічних реакцій становила 14% (4/29) у групі диклофенаку проти 12% (3/25) на тлі Фламідезу; при люмбоішіалгії – 16% (8/49) проти 11% (6/54) відповідно. Таким чином, у всіх аналізованих категоріях комбінований препарат мав номінально дещо нижчу частоту шлунково-кишкових ускладнень, хоча різниця не була статистично значущою.
Група Препарат Кількість пацієнтів, що мали мінімум одну побічну реакцію Усі пацієнти Диклофенак 12/78 (15%) Фламідез 9/79 (11%) Пацієнти з люмбаго Диклофенак 4/29 (14%) Фламідез 3/25 (12%) Пацієнти з люмбоішіалгією Диклофенак 8/49 (16%) Фламідез 6/54 (11%)
Характер побічних реакцій з боку ШКТ був переважно легким та передбачуваним для нестероїдних протизапальних засобів (табл. 4). Найбільш частими симптомами були біль або дискомфорт у животі, нудота та печія. Аналізуючи дані усіх пацієнтів, установлено, що на тлі диклофенаку 11,5% пацієнтів (9/78) скаржились на нудоту, 6% (5/78) – на печію, 14% (11/78) – на біль/дискомфорт у животі. У групі Фламідезу відповідні показники були дещо нижчими: нудота спостерігалась у 9% пацієнтів (7/79), печія – у 4% (3/79), біль або дискомфорт у животі – в 11% (9/79) пацієнтів. Відмінності за окремими реакціями між групами не були статистично значущими, проте відмічається тенденція до меншої частоти й вираженості цих симптомів при застосуванні Фламідезу. Важливо підкреслити, що в більшості випадків один і той самий пацієнт повідомляв про більше ніж один симптом (наприклад, абдомінальний дискомфорт часто поєднувався з нудотою або печією), тому сумарна частота окремих скарг перевищує відсоток пацієнтів із хоча б однією побічною реакцією. Серйозних ускладнень з боку ШКТ (таких як шлунково-кишкові кровотечі або виразки) протягом короткого 7-денного курсу терапії не спостерігалося в жодній групі.
Препарат, кількість пацієнтів (n) Нудота Печія Біль / дискомфорт у животі Усі пацієнти Диклофенак (n=78) 9/78 (11,5%) 5/78 (6%) 11/78 (14%) Фламідез (n=79) 7/79 (9%) 3/79 (4%) 9/79 (11%) Пацієнти з люмбаго Диклофенак (n=29) 3/29 (10%) 1/29 (3%) 3/29 (10%) Фламідез (n=25) 2/25 (8%) 1/25 (4%) 3/25 (12%) Пацієнти з люмбоішіалгією Диклофенак (n=49) 6/49 (12%) 4/49 (8%) 8/49 (16%) Фламідез (n=54) 5/54 (9%) 2/54 (4%) 6/54 (11%) Примітки: у переважній більшості випадків окремі пацієнти відмічали більше ніж одну побічну реакцію (наприклад, біль/дискомфорт у животі супроводжувався нудотою).
Отримані результати демонструють переваги комбінованої терапії з використанням калієвої солі диклофенаку (Фламідез) над монотерапією диклофенаком натрію в аспекті як клінічної ефективності, так і переносимості. З точки зору знеболювальної дії Фламідез забезпечує більш швидке настання та більш виражене полегшення болю в пацієнтів з гострим люмбаго та ішіасом. Уже на другий день лікування біль у групі Фламідезу достовірно зменшується, тоді як диклофенак натрію потребує більше часу для досягнення помітного ефекту. Різниця в показниках ВАШ між групами на користь Фламідезу проявилася з 3-го дня і зберігалася надалі, що свідчить про більш сильний та швидкий анальгетичний ефект комбінованого препарату. До кінця тижневого курсу в більшості пацієнтів, які отримували Фламідез, біль практично зник (медіана 0 балів), тоді як при застосуванні лише диклофенаку натрію в частини пацієнтів залишався помірний больовий синдром. Така динаміка є клінічно значущою, оскільки швидке купірування болю покращує якість життя пацієнтів і може сприяти швидшому відновленню активності.
Переваги Фламідезу можуть пояснюватися, у першу чергу, його складом: комбінація диклофенаку калію з парацетамолом та ферментом серратіопептидазою забезпечує мультифакторний вплив на больовий синдром. Диклофенак калію як НПЗП зменшує запалення і біль через інгібіцію синтезу простагландинів, парацетамол додає центральний анальгетичний ефект, а серратіопептидаза має протинабрякові та протизапальні властивості, що можуть покращувати мікроциркуляцію і зменшувати набряк у місці ураження нервових корінців. Синергічна дія цих компонентів, ймовірно, підсилює знеболювання без необхідності підвищувати дозу НПЗП, що пояснює швидше зниження болю та більшу кінцеву ефективність Фламідезу [19].
Отримані результати узгоджуються з даними інших клінічних досліджень, у яких комбіновані анальгетичні препарати демонстрували більш швидке зменшення больового синдрому порівняно з монотерапією НПЗП. Зокрема, у ряді рандомізованих досліджень показано, що мультимодальна анальгезія із застосуванням НПЗП у комбінації з іншими анальгетиками дозволяє підвищити ефективність контролю болю та зменшити потребу у високих дозах НПЗП.
Окремо варто зазначити можливі переваги калієвої солі диклофенаку. Диклофенак калію є швидкорозчинною формою, що забезпечує швидше всмоктування та, як наслідок, швидший та інтенсивніший анальгезивний ефект. Кокрейнівський метааналіз свідчить, що одноразова доза диклофенаку калію (50 мг) забезпечує значуще полегшення болю в значно більшої кількості пацієнтів, аніж аналогічна доза натрієвої солі диклофенаку [20]. Отже, калієва сіль забезпечує швидший і сильніший анальгетичний ефект при гострому болю, при цьому натрієва сіль діє повільніше й менш ефективна в таких ситуаціях.
Щодо безпечності, комбінований препарат Фламідез також продемонстрував кращий профіль. Незважаючи на те, що обидва досліджувані режими загалом добре переносилися протягом 7 днів, у групі диклофенаку натрію виявлено дещо більшу частоту побічних реакцій з боку ШКТ і помітніші зміни лабораторних показників. Підвищення рівнів АЛТ та АСТ при застосуванні диклофенаку натрію хоч і було відносно невеликим та клінічно незначущим, але статистично підтверджує наявність фармакологічного навантаження на печінку. У половини пацієнтів медіани трансаміназ наблизилися до верхньої межі норми вже за тиждень лікування. Навпаки, на тлі Фламідезу таких змін не спостерігалося, що свідчить про те, що навіть додавання парацетамолу не посилює гепатотоксичної дії, а можливо, дозволяє зменшити ефективну дозу диклофенаку калію в складі комбінації. При цьому варто зазначити можливий захисний вплив третього компонента Фламідезу – серратіопептидази, яка здатна не лише посилювати протизапальний та знеболювальний потенціал НПЗП [21], але й завдяки своїм мультимодальним позитивним властивостям теоретично запобігати негативному впливу на печінку [22], що потребує окремих досліджень.
В аспекті шлунково-кишкової переносимості відмінності між групами були менш виражені, проте загальна тенденція все ж складається на користь Фламідезу, на тлі якого спостерігали дещо меншу частоту розвитку нудоти, печії, абдомінального дискомфорту та взагалі нижчу сумарну кількість пацієнтів з гастроінтестинальними побічними реакціями. Це може бути пов’язано з тим, що комбінована терапія дозволяє досягти знеболювання при нижчому навантаженні на шлунково-кишковий тракт від НПЗП, а також з потенційними цитопротективними ефектами серратіопептидази. У деяких експериментальних і клінічних роботах повідомляється про потенційні протизапальні та протинабрякові властивості серратіопептидази, які можуть посилювати анальгетичний ефект НПЗП. Однак доказова база щодо її гастро- або гепатопротекторних властивостей залишається обмеженою і потребує подальших досліджень [23]. При цьому не можна виключати й можливі переваги калієвої солі диклофенаку. Визначено, що диклофенак калію в значно більшій дозі мав порівняну переносимість з диклофенаком натрію (150 мг/добу проти 100 мг/добу) [24]. Такі властивості калієвої солі можуть бути опосередковано пов’язані з фармакокінетичними особливостями, коли швидше всмоктування диклофенаку калію обмежує час його безпосереднього контакту зі слизовою ШКТ та, як наслідок, подразнювальну дію [25].
Важливо, що побічні реакції, які фіксували пацієнти, мали легкий перебіг та не призводили до відмови від лікування. При цьому жодного випадку серйозного ураження ШКТ (наприклад, виразки чи кровотечі) в обох групах не було, що підкреслює безпечність короткого курсу як
моно-, так і комбінованої терапії.
Таким чином, у цьому дослідженні застосування Фламідезу асоціювалося з більш сприятливим співвідношенням користі та ризику порівняно з диклофенаком натрію при лікуванні больового синдрому в нижній частині спини. Комбінація диклофенаку калію з парацетамолом і серратіопептидазою забезпечила швидше та повніше полегшення болю, не спричиняючи при цьому значного підвищення печінкових ферментів і з тенденційно меншою частотою побічних ефектів з боку ШКТ. Диклофенак як монотерапія, хоча й ефективно знижував біль, поступався комбінованому підходу за швидкістю анальгезії і мав дещо гіршу переносимість. З позицій клінічної фармакології та практичної медицини отримані дані свідчать про можливі клінічні переваги застосування комбінованого препарату Фламідез при гострому люмбаго та люмбоішіалгії, оскільки він дозволяє досягти кращого клінічного результату за коротший час і з меншою імовірністю розвитку побічних реакцій. Це особливо актуально для пацієнтів, яким потрібне швидке відновлення працездатності та мінімізація ризиків при знеболювальній терапії.
Обмеження дослідження.
Незважаючи на отримані клінічно значущі результати, інтерпретація даних цього дослідження повинна враховувати низку методологічних обмежень.
По-перше, дослідження мало відкритий обсерваційний дизайн без рандомізації та засліплення, що потенційно може впливати на порівнянність груп і створювати ризик систематичних похибок. Призначення терапії здійснювалося лікарями в умовах рутинної клінічної практики, тому розподіл пацієнтів між групами не був випадковим.
По-друге, тривалість спостереження становила лише 7 днів, що відповідає типовій тривалості лікування гострого поперекового болю, проте обмежує можливість оцінювання довгострокової ефективності та безпеки терапії. Зокрема, відмінності між групами щодо змін рівнів печінкових трансаміназ (АЛТ та АСТ) відображають переважно короткострокову реакцію організму на лікування і не дозволяють повною мірою оцінити потенційний вплив терапії при більш тривалому застосуванні.
По-третє, у межах дослідження дозволялося застосування супутньої терапії відповідно до стандартної клінічної практики, зокрема місцевих форм нестероїдних протизапальних препаратів. Використання таких засобів могло певною мірою впливати на інтенсивність больового синдрому та швидкість його регресу, що потенційно могло модифікувати кінцеві результати лікування. Водночас подібний підхід відображає реальні умови амбулаторної клінічної практики.
По-четверте, оцінка ефективності терапії ґрунтувалася переважно на суб’єктивному показнику інтенсивності болю за візуально-аналоговою шкалою (ВАШ). Незважаючи на широку валідність і поширене використання цього інструменту в клінічних дослідженнях, результати можуть частково залежати від індивідуального сприйняття болю пацієнтами.
З огляду на зазначені обмеження отримані результати слід розглядати як дані, що відображають ефективність і переносимість терапії в умовах короткострокового застосування в реальній клінічній практиці. Подальші рандомізовані контрольовані дослідження з більшим періодом спостереження та суворішим контролем супутньої терапії є необхідними для підтвердження отриманих результатів та більш повної оцінки довгострокової ефективності й безпеки застосування досліджуваних препаратів.
ВИСНОВКИ
1. У проспективному багатоцентровому обсерваційному дослідженні за участю 157 пацієнтів з гострим поперековим больовим синдромом (люмбаго та люмбоішіалгія) проведено порівняльне оцінювання ефективності та переносимості комбінованого лікарського засобу Фламідез (диклофенак калію, парацетамол, серратіопептидаза) та диклофенаку натрію.
2. Обидві досліджувані схеми терапії асоціювалися зі зменшенням інтенсивності больового синдрому за візуально-аналоговою шкалою протягом 7-денного курсу лікування.
3. У групі пацієнтів, які отримували комбінований препарат Фламідез, спостерігалася тенденція до більш швидкого та вираженого зниження інтенсивності болю порівняно з монотерапією диклофенаком натрію.
4. Показник середнього зниження інтенсивності болю (ΔВАШ) у групі Фламідезу був вищим, ніж у групі диклофенаку натрію, що може свідчити про потенційні переваги мультимодального підходу до анальгезії при гострому поперековому болю.
5. Профіль безпеки обох режимів лікування протягом короткотривалого застосування був загалом сприятливим. У групі диклофенаку натрію відзначалося помірне підвищення рівнів печінкових трансаміназ, тоді як у групі Фламідезу подібної тенденції не спостерігалося; водночас ці результати потребують обережної інтерпретації з огляду на короткий період спостереження.
6. Отримані результати свідчать, що комбінований препарат Фламідез може розглядатися як один з можливих варіантів фармакотерапії гострого поперекового болю, проте для остаточного підтвердження його клінічних переваг необхідні подальші рандомізовані контрольовані дослідження з більш тривалим періодом спостереження.
Внески авторів:
Кононенко Н.М. – дослідження, методологія, формальний аналіз, написання – початковий проєкт, редагування;
Цивунін В.В. – концептуалізація, курування даних, адміністрування проєкту;
Брюханова Т.О. – дослідження, формальний аналіз, ресурси;
Співавтори (20)4 – дослідження, ресурси.
Фінансування. Дослідження не має зовнішніх джерел фінансування.
Конфлікт інтересів. Цивунін В.В. є головним медичним радником ТОВ «ОРГАНОСІН ЛТД» – компанії, що здійснює маркетування лікарського засобу Фламідез. Інші автори заявляють про відсутність потенційного конфлікту інтересів. Автори-дослідники не отримували фінансових винагород або інших стимулів за участь у проведенні цього дослідження. Дослідження було проведено як незалежне обсерваційне спостереження в умовах рутинної клінічної практики.
4 Співавтори (20) та їх внески в дослідження
| ПІБ | Місце роботи | Внесок автора в дослідження | ORCID |
|---|---|---|---|
|
Дзик І.М. |
Медичний центр Garvis м. Дніпро |
дослідження, ресурси |
|
|
Загранична Ю.П. |
АЗПСМ № 6а – КНП Білоцерківської міської ради «МЦПМСД № 1» |
дослідження, ресурси |
|
|
Сологуб А.Ю. |
Сквирська АЗПСМ – КНП Сквирської міської ради «Сквирський МЦПМСД» |
дослідження, ресурси |
|
|
Головай А.С. |
АЗПСМ №6а – КНП Білоцерківської міської ради «МЦПМСД № 1» |
дослідження, ресурси |
|
|
Гулевська К.В. |
КНП Усатівської сільської ради «Усатівський ЦПМСД» |
дослідження, ресурси |
|
|
Панасюк І.Ф. |
КНП «ЦПМСД № 18» Одеської міської ради |
дослідження, ресурси |
|
|
Гончарук К.О. |
КНП «ЦПМСД № 2» Одеської міської ради |
дослідження, ресурси |
|
|
Бутель О.М. |
АЗПСМ № 6 КНП «ЦПМСД» Печерського району міста Києва |
дослідження, ресурси |
|
|
Канська А.Я. |
Амбулаторія ЗПСМ № 7 КНП «ЦПМСД № 1» Голосіївського району міста Києва |
дослідження, ресурси |
|
|
Гришан М.А. |
Українська амбулаторія ЗПСМ Обухівського районного ЦПМСД |
дослідження, ресурси |
|
|
Безбах А.І. |
ФОП «Мандро» |
дослідження, ресурси |
|
|
Клановець К.С. |
Поліклініка № 3 КНП «Чернігівська міська лікарня № 2» Чернігівської міської ради |
дослідження, ресурси |
|
|
Сеник І.І. |
Амбулаторія сімейної медицини № 9 Ніжинського міського ЦПМСД |
дослідження, ресурси |
|
|
Титоренко В.В. |
Поліклініка № 3 КНП «Чернігівська міська лікарня №2» Чернігівської міської ради |
дослідження, ресурси |
|
|
Іскужина А.С. |
КНП «Павлоградська міська лікарня № 1» Павлоградської міської ради |
дослідження, ресурси |
|
|
Гайченя С.В. |
Амбулаторія ЗПСМ № 3 Кам'янець-Подільської міської ради |
дослідження, ресурси |
|
|
Мізіна О.А. |
КНП «Лівобережний центр первинної медико-санітарної допомоги № 2» Запорізької міської ради |
дослідження, ресурси |
|
|
Гриценко М.О. |
КНП «ДЦПМСД 9» Дніпровської міської ради |
дослідження, ресурси |
|
|
Краюшкіна І.А. |
ТОВ «Оксфорд Медікал» м. Кам'янське |
дослідження, ресурси |
|
|
Ситнік А.В. |
МЦ «Лікую.юа» |
дослідження, ресурси |
REFERENCES
1. Li Y, Zou C, Guo W, et al. Global burden of low back pain and its attributable risk factors from 1990 to 2021: a comprehensive analysis from the Global Burden of Disease Study 2021. Frontiers in Public Health. 2024;12:1480779. doi: https://doi.org/10.3389/fpubh.2024.1480779
2. Low back pain and sciatica in over 16s: assessment and management. NICE guideline [NG59]. National Institute for Health and Care Excellence (NICE). [Internet]. 2020 [cited 2025 Dec 23]. Available from: https://www.nice.org.uk/guidance/ng59
3. Ferreira ML, March L, Croft P, Maher CG, Lin CW, Buchbinder R, et al. Global, regional, and national burden of low back pain, 1990-2020, its attributable risk factors, and forecasts to 2050: a systematic analysis of the Global Burden of Disease Study 2021. Lancet Rheumatol. 2023;5(6):e316-e329. doi: https://doi.org/10.1016/S2665-9913(23)00098-X
4. American College of Physicians. Noninvasive Treatments for Acute, Subacute, and Chronic Low Back Pain: Clinical Practice Guideline. Ann Intern Med. 2021;174(3):391-8. doi: https://doi.org/10.7326/M19-2063
5. WHO report on non-steroidal anti-inflammatory drugs safety update. World Health Organization [Internet]. 2022 [cited 2025 Dec 23]. Available from: https://www.who.int/publications/i/item/NSAIDs-safety-2022
6. Marin T. Single‑dose intravenous diclofenac for acute postoperative pain in adults: A Cochrane review summary. Int J Nurs Stud. 2021;113:103410. doi: https://doi.org/10.1016/j.ijnurstu.2019.103410
7. Diclofenac safety profile. World Health Organization [Internet]. 2022 [cited 2025 Dec 23]. Available from: https://www.who.int/publications/i/item/NSAIDs-safety-2022
8. Alshargabi A, Mehta D, Elhassan GO, Singh N, Farooq U, Khan A, et al. Recent developments in diclofenac derivatives and drug delivery carriers: structural modification, pharmacokinetics, and toxicity reduction. Eur J Pharm Sci. 2024;192:106324. doi: https://doi.org/10.1016/j.ejps.2024.106324
9. Dammann P, Kirsch M, Bittersohl T, et al. Diclofenac-induced hepatotoxicity: a review of literature and recent case series. World J Hepatol. 2020;12(8):490-502. doi: https://doi.org/10.4254/wjh.v12.i8.4
10. García Rodríguez LA, Tacconelli S, Patrignani P. Role of dose potency in the risk of NSAID-induced hepatotoxicity: a systematic review. Br J Clin Pharmacol. 2021;87(6):2345-56. doi: https://doi.org/10.1111/bcp.14582
11. Derry S, Wiffen PJ, Moore RA. Single dose oral diclofenac for acute postoperative pain in adults. Cochrane Database Syst Rev. 2015;7:CD004768. doi: https://doi.org/10.1002/14651858.CD011509
12. Opryshko VI. Perspectives for using serratiopeptidase in systemic enzyme therapy for low-intensity chronic inflammation and pain syndromes: from mechanisms of action to practical implementation (literature review). Pain Joints spine. 2024;14(3):162-72. doi: https://doi.org/10.22141/pjs.14.3.2024.432
13. Bapat K, Kumar A, Katke P, Kulkarni K, Suryawanshi S. Serratiopeptidase with diclofenac sodium for the management of post-operative pain and inflammation in a day care obstetric and gynaecological surgeries. Indian Journal of Obstetrics and Gynecology Research. 2024;11(3):442-6. doi: https://doi.org/10.18231/j.ijogr.2024.080
14. [FLAMIDEZ®: proven efficacy and high safety profile of the original combination]. Zdorovia Ukrainy 21 storichchia. [Internet]. 2025 [cited 2025 Dec 23];5(591):55-7. Ukrainian. Available from: https://health-ua.com/neurology/bolyovi-sindromi/79956-flamidez-dovedena-efektivnist-ta-visokii-profil-bezpeki-originalnoyi-kombinaciyi
15. Kaplan RM, Bush JW. Health‑related quality of life measurement for evaluation research and policy analysis. Health Psychology. 1982;1:61-80. doi: https://doi.org/10.1037/0278-6133.1.1.61
16. Saki F, Mohammadi F, Chen H, Alizadeh M, Yamamoto A, Lee SY, et al. BodyBalance as an exercise therapy trial in knee osteoarthritis: visual analogue scale (VAS) for pain severity and its reliability in outcome assessment. Trials. 2025;26(75):1025. doi: https://doi.org/10.1186/s13063-025-09036-w
17. Koo М. Visual Analogue Scale. Encyclopedia. 2025;5(4):190. doi: https://doi.org/10.3390/encyclopedia504019
18. Lee SW. Methods for testing statistical differences between groups in medical research: statistical standard and guideline of Life Cycle Committee. Life Cycle. 2022;2:e1. doi: https://doi.org/10.54724/lc.2022.e1
19. Tena-Garitaonaindia M, Rubio JM, Martínez-Plata E, Martínez-Augustin O, Sánchez de Medina F. Pharmacological bases of combining nonsteroidal antiinflammatory drugs and paracetamol. Biomedicine & Pharmacotherapy. 2025;187:118069. doi: https://doi.org/10.1016/j.biopha.2025.118069
20. Derry S, Wiffen PJ, Moore RA. Single dose oral diclofenac for acute postoperative pain in adults. Cochrane Database Syst Rev. 2015;7:CD004768. doi: https://doi.org/10.1002/14651858.CD011509
21. Jadhav SB, Shah N, Rathi A, Rathi V, Rathi A. Serratiopeptidase: Insights into the therapeutic applications. Biotechnol Rep (Amst). 2020;28:e00544. doi: https://doi.org/10.1016/j.btre.2020.e00544
22. Nair SR, C SD. Serratiopeptidase: An integrated View of Multifaceted Therapeutic Enzyme. Biomolecules. 2022;12:1468. doi: https://doi.org/10.3390/biom12101468
23. Narayanan KB, Park JY, Lee YS, Choi HJ, Kim EK, Seo CH, et al. Enzyme-based anti-inflammatory therapeutics for inflammatory diseases: natural and engineered enzymes and their formulations. Pharmaceutics. 2025;17(5):606. doi: https://doi.org/10.3390/pharmaceutics17050606
24. Pellesi L, Guerzoni S, Cainazzo MM, Baraldi C, Pini LA. Pharmacological management of migraine: acute therapies including diclofenac potassium and other NSAIDs. Expert Rev Neurother. 2024;24(5):367-77. doi: https://doi.org/10.1080/14737175.2024.2349791
25. [Clinical aspects of the use of diclofenac potassium in the treatment of pain]. NeuroNews: psykhonevrolohiia ta neiropsykhiatriia. [Internet]. 2018 [cited 2025 Dec 23];2(95):36-38. Ukrainian. Available from: https://neuronews.com.ua/ua/archive/2018/2%2895%29/pages-36-38/klinichni-aspekti-zastosuvannya-diklofenaku-kaliyu-u-likuvanni-bolyu#gsc.tab=0


 UK
UK  EN
EN