Select your language
Select your language
Key words: Nursing education, clinical learning environment, preceptorship, simulation-based education, Albania
Ключові слова: медсестринська освіта, клінічне навчальне середовище, прецепторство, симуляційне навчання, Албанія
Abstract
Nursing students’ perceptions of educational quality – particularly the clinical learning environment (CLE) – are an early indicator of whether programs are producing graduates who feel ready for practice. This study aimed to describe nursing students’ perceived educational quality and clinical learning environment (CLE) in two Albanian universities, and to identify factors independently associated with low perceived preparedness for practice. In May 2025, a cross-sectional questionnaire was administered to 367 students at the department of medical technical sciences, University “Aleksandër Moisiu” of Durrës and the University “Eqrem Çabej” of Gjirokastra. Items covered staff availability, teaching quality and clinical skills, preparedness for practice, teaching approaches, and placement conditions. Domain scales were created (Cronbach’s α ≥0.70) and low preparedness was defined as a preparedness score below the sample median. In multivariable binary and ordinal logistic regression, limited availability of clinical supervisors/preceptors, poorer overall CLE quality, and lower exposure to simulation-based teaching were independently associated with low preparedness. Descriptively, around half of respondents reported that key CLE domains need improvement, including distance to clinical practice sites (52.0%), transportation (49.6%), availability of equipment and supplies (50.1%), quality of supervision (50.1%), and student assessment (51.0%). Clinical supervisors/preceptors were often available for 31.9% of students. Only 23.4% rated clinical supervisors/preceptors’ teaching quality as good. Simulation and role-play were among the least frequently used teaching approaches. Students’ responses indicate systematic gaps in clinical supervision capacity, placement logistics, and clinical learning infrastructure. Strengthening structured preceptorship, clinical site agreements, and skills-lab/simulation capacity are practical targets for quality improvement.
Реферат
Сприйняття якості освіти медсестер з огляду на перспективи розвитку систем охорони здоров'я: перехресне дослідження двох університетів Албанії. Бімі Індріт, Бімі Даніела, Ллавданіті Мімоза. Сприйняття студентами медсестринства якості освіти – зокрема клінічного навчального середовища (КНС) – є раннім індикатором того, чи готують програми випускників, які відчувають готовність до практичної роботи. Метою цього дослідження було описати сприйману студентами якість освіти та клінічного навчального середовища у двох університетах Албанії, а також визначити чинники, незалежно пов’язані з низькою сприйманою готовністю до практики. У травні 2025 року між 367 студентами факультету медичних технічних наук університету «Александр Мойсіу» в Дурресі та університету «Екрем Чабей», Гірокастра, було проведено перехресне опитування. Пункти анкети охоплювали доступність персоналу, якість викладання та клінічні навички, готовність до практики, підходи до навчання та умови проходження практики. Було сформовано шкали доменів (α Кронбаха ≥0,70), а низьку готовність визначали як показник готовності нижче медіани вибірки. У багатофакторній бінарній та порядковій логістичній регресії обмежена доступність клінічних супервізорів/прецепторів, гірша загальна якість КНС та менший рівень залучення до симуляційного навчання були незалежно пов’язані з низькою готовністю. Описово приблизно половина респондентів повідомила, що ключові домени КНС потребують покращення, зокрема відстань до баз практики (52,0%), транспорт (49,6%), наявність обладнання та витратних матеріалів (50,1%), якість супервізії (50,1%) й оцінювання студентів (51,0%). Для 31,9% студентів клінічні супервізори/прецептори були доступні «часто». Лише 23,4% оцінили якість викладання клінічних супервізорів/прецепторів як добру. Симуляції та рольові ігри були серед найрідше застосовуваних підходів до навчання. Відповіді студентів свідчать про системні прогалини в спроможності клінічної супервізії, логістиці практик та інфраструктурі клінічного навчання. Посилення структурованого прецепторства, угод з клінічними базами та можливостей навичкових лабораторій/симуляцій є практичними цілями для підвищення якості.
Nursing education is ultimately judged by its ability to produce graduates who can deliver safe, competent, and patient-centred care within increasingly complex healthcare systems. This expectation extends beyond technical proficiency to include clinical reasoning, communication, ethical practice, teamwork, and adaptability to diverse care settings. Central to this formative process is the clinical learning environment (CLE), where theoretical knowledge acquired in classrooms is translated into practice, professional identity is shaped, and students internalize the norms and responsibilities of the nursing role [1, 2].
A substantial body of international literature demonstrates that students’ perceptions of the CLE are strongly associated with educational outcomes, including satisfaction, confidence, motivation, and perceived preparedness for practice. Key dimensions influencing these perceptions include the pedagogical atmosphere of the clinical setting, the quality and consistency of supervision, leadership and organizational culture on the ward, and the effectiveness of collaboration between academic institutions and clinical sites [3]. In particular, the supervisory relationship between students and clinical preceptors has been identified as one of the most influential determinants of learning quality, professional socialization, and students’ sense of belonging within the clinical team.
However, across many healthcare systems, the CLE is under increasing strain. Rising service demands, workforce shortages, and heightened administrative burdens have reduced the time and capacity available for clinical teaching and mentorship. As a result, students frequently report insufficient supervision, variability in mentoring quality, misalignment between theoretical instruction and clinical realities, inconsistent assessment practices, and limited access to essential equipment and learning resources during placements [4, 5]. These challenges are not trivial or merely perceptual; they reflect structural and organizational constraints that can undermine competency development, delay skill acquisition, and contribute to lower confidence during transition to professional practice.
Logistical and infrastructural factors further compound these challenges. Distance to clinical sites, lack of organized transportation, overcrowded placements, and uneven distribution of learning opportunities across clinical settings can restrict students’ exposure to diverse patient populations and limit hands-on practice. Evidence suggests that when clinical placements are poorly coordinated or inadequately resourced, students are more likely to experience observational rather than participatory learning, reducing the effectiveness of clinical education despite formal curriculum requirements [1, 6].
In response to these constraints, educational research increasingly highlights the complementary role of structured preceptorship models, standardized assessment frameworks, and simulation-based education. While simulation cannot replace real-world clinical exposure, high-quality simulation and skills-lab training have been shown to enhance students’ self-confidence, clinical reasoning, and readiness for practice, particularly in settings where clinical opportunities are limited or unevenly distributed [7]. The effectiveness of such approaches, however, depends on their integration within a coherent educational strategy that aligns classroom teaching, simulated learning, and clinical placements.
In Albania, nursing education programs have expanded over the past decade in response to workforce demands and broader health system reforms. Despite this quantitative growth, there is limited published evidence examining students’ experiences of the CLE and the organizational factors that shape the quality of clinical education. Clinical placement experiences may vary substantially across sites due to differences in supervision models, institutional capacity, patient mix, and available infrastructure. In this context, systematic assessment of students’ perceptions provides a valuable lens through which program-level strengths and weaknesses can be identified, particularly those that are amenable to improvement through curriculum design, formalized clinical partnerships, and targeted investment in supervision and educational resources.
Accordingly, the present study aimed to describe nursing students’ perceptions of educational quality in two Albanian universities, with a specific focus on: (I) availability of educational and support staff, (II) perceived teaching quality and clinical skills of instructors, (III) perceived preparedness for practice across common care settings and competencies, (IV) teaching approaches used within the program, and (V) key quality domains of the clinical learning environment during placements. By identifying areas consistently perceived as needing improvement, this study seeks to inform evidence-based strategies for strengthening clinical nursing education within the Albanian context.
MATERIALS AND METHODS OF RESEARCH
A descriptive cross-sectional study was conducted in May 2025 among nursing students enrolled in Bachelor and Master-level programs at two public universities in Albania: the Department of Medical Technical Sciences, Aleksandër Moisiu University of Durrës (DSHTM-UAMD), and the University of Gjirokastra (UGJ). The study was designed to capture students’ perceptions of the quality of nursing education and the clinical learning environment (CLE) at a single point in time, reflecting their cumulative academic and clinical training experiences. The study was planned and reported in accordance with the STROBE recommendations for cross-sectional observational research.
Eligible participants included students enrolled in Bachelor of Science (BSc) and Professional Master (MP) nursing programs who had exposure to clinical placements (completed or ongoing). Students from different years of study and academic tracks were included to ensure heterogeneity in exposure to clinical supervision models, teaching approaches, and placement settings. Participation was voluntary, anonymous, and unrestricted by age or gender. A total of 367 students completed the survey and were included in the final analysis.
Data collection procedure
Data were collected using a structured, self-administered questionnaire distributed both in classroom settings and online. Classroom distribution took place following scheduled teaching activities, while online administration was used to reach students who were unavailable due to clinical placements or scheduling constraints. This mixed-mode approach was adopted to maximize participation and minimize selection bias related to attendance, consistent with standard principles of survey methodology. Because the survey was distributed through classroom sessions and online, the number of students who received an invitation could not be precisely determined, and a formal response rate was therefore not calculated. Prior to completion, students received standardized instructions and were informed that their responses would be anonymous and would not affect their academic standing. Completion time was approximately 15-20 minutes.
Instrument development and validation
The questionnaire was specifically adapted for use in the Albanian nursing education context, drawing on established conceptual frameworks of clinical learning environment quality and nursing education evaluation. The adaptation process involved content review by academic nursing staff and clinical instructors to ensure relevance, clarity, and cultural appropriateness. The instrument was pilot-tested with a small group of nursing students, leading to minor linguistic and structural refinements before final deployment. The final questionnaire demonstrated satisfactory content and face validity for assessing students’ perceptions of educational quality and clinical training experiences, consistent with recommended procedures for questionnaire development and validation.
Measures
The questionnaire collected information across several domains. Sociodemographic and academic variables included gender, university affiliation, program of study, and year of study. Year of study was defined as the current year within the student’s enrolled program and treated as an ordinal (numeric) variable in regression models.
Perceived availability of educational and support staff was assessed through items evaluating the accessibility of classroom instructors, skills-lab instructors, clinical supervisors/preceptors, academic mentors, librarians, and information technology support staff. Responses were recorded using four ordered categories reflecting frequency of availability.
Perceived teaching quality and perceived clinical skills of instructors were assessed separately for classroom instructors, skills-lab instructors, and clinical supervisors/preceptors. Students rated each group using ordinal response options reflecting overall quality and competence.
Perceived preparedness for practice was assessed across sixteen competencies and work contexts, including primary care, hospital and emergency settings, teamwork, rural practice, use of digital technologies, clinical reasoning, management tasks, advocacy, lifelong learning, and research. Responses reflected graded levels of preparedness rather than binary competence.
Teaching approaches used within the program were assessed by asking students to indicate the frequency with which various instructional methods were employed, including lectures, demonstrations, supervised practice, simulations, role-play, small-group learning, self-directed learning, and community-based projects.
Finally, key quality indicators of the clinical learning environment were assessed, including logistical aspects of placements, supervision and teaching quality during practice, assessment and grading processes, alignment between theory and practice, patient mix, safety, and availability of equipment and supplies.
Methodological approach (sociological and epidemiological methods)
In line with sociological research methodology, this study used an anonymous questionnaire-based cross-sectional survey to quantify students’ perceptions and experiences in nursing education and clinical training. From an epidemiological perspective, the study applied descriptive epidemiology to characterize the distribution of key variables (university, program, year of study, and perception domains) and analytic epidemiology to assess associations between hypothesized determinants (e.g., supervision availability, CLE quality, simulation-based teaching) and preparedness outcomes.
Internal consistency reliability
For multi-item domains designed to measure coherent constructs (availability of staff, perceived teaching quality, perceived clinical skills, preparedness for practice, teaching approaches, and clinical learning environment quality indicators), internal consistency reliability was evaluated using Cronbach’s alpha coefficient. Cronbach’s alpha was calculated for each multi-item scale to assess the degree to which items within a domain measured the same underlying construct. Values of α ≥0.70 were considered acceptable, values ≥0.80 good, and values ≥0.90 excellent internal consistency [8].
Ethical considerations
This study was conducted in accordance with international ethical requirements for research involving human participants, including the principles of the Declaration of Helsinki, and in compliance with applicable institutional and national regulations. Ethical approval was obtained from “Aleksandër Moisiu”, Durrës, Albania (protocol No. 1197, date 28.04.2025 and “Eqrem Çabej” University of Gjirokastër (protocol No. 13 date 29,01.2026). Participation was voluntary. All participants provided written informed consent prior to enrolment. Data were collected anonymously, stored securely, and analysed in aggregated form to ensure confidentiality.
Statistical analysis
Statistical analysis was performed using R (version 4.3.2; free open-source software) (R Foundation for Statistical Computing, Vienna, Austria) [9]. Incomplete questionnaires were excluded before analysis, yielding a final analytic sample of 367 students with complete data for all variables included in the primary models. All analyses followed a pre-specified analytical plan consistent with the descriptive and explanatory aims of the study. The statistical modelling approach followed standard guidance for logistic and ordinal logistic regression, and scale reliability followed established psychometric methods (e.g., Hosmer & Lemeshow; Agresti; McCullagh; Cronbach).
Data preparation and coding
Questionnaire responses were screened for completeness and internal consistency prior to analysis. Likert-type items were coded numerically according to their ordinal structure, with higher values indicating more favorable perceptions (e.g., greater preparedness, better learning environment quality, or higher availability of support). Composite scores were created for multi-item domains, including perceived preparedness for practice, availability of educational and support staff, perceived teaching quality, perceived clinical skills, teaching approaches, and clinical learning environment (CLE) quality indicators, by summing item-level scores within each domain.
Reliability analysis
Internal consistency of multi-item scales was assessed using Cronbach’s alpha. Alpha values ≥0.70 were considered acceptable, ≥0.80 good, and ≥0.90 excellent. Reliability analysis was conducted prior to scale aggregation to justify the use of composite scores in subsequent analyses [10].
Descriptive analysis
Descriptive statistics were used to summarize participant characteristics and questionnaire responses. Categorical variables are presented as frequencies and percentages [n (%)]. Composite scores are described using measures of central tendency and dispersion, as appropriate. No imputation was performed. All questionnaires included in the analysis had complete data for variables used in the analyses; regression models used n=367.
Regression modelling
To examine factors independently associated with perceived preparedness for practice, multivariable regression analyses were conducted. The primary outcome was low perceived preparedness, defined as a composite preparedness score below the sample median and modeled as a binary variable. A multivariable binary logistic regression model was fitted to estimate adjusted odds ratios (aORs) and 95% confidence intervals (CIs). Independent variables were selected a priori based on educational theory and prior literature and included university affiliation, academic program, year of study, perceived availability of clinical supervisors/preceptors, overall CLE quality, and frequency of simulation-based teaching. Academic program was operationalized as BSc versus Master-level. Predictor domains (availability of clinical supervisors/preceptors, overall CLE quality, and simulation-based teaching frequency) were derived from composite scores and dichotomized at the sample median (low/poor vs high/good) to align with Tables 7-8 and to facilitate interpretation [11].
To assess robustness and account for the ordinal nature of preparedness perceptions, a secondary ordinal logistic regression model was performed using ordered categories of preparedness (good, somewhat prepared, poor/not at all prepared) as the outcome. Proportional odds assumptions were assessed and deemed acceptable [12].
Model diagnostics and statistical significance
Multicollinearity among independent variables was evaluated using variance inflation factors (VIFs). Model fit was assessed using standard goodness-of-fit measures. All statistical tests were two-sided, and a
p-value <0.05 was considered statistically significant.
RESULTS AND DISCUSSION
A total of 367 nursing students participated in the study. The majority were female (92.6%) and enrolled in the Bachelor of Science (BSc) program (88.3%). Most participants were affiliated with Aleksandër Moisiu University of Durrës (76.0%), while 24.0% were enrolled at the University of Gjirokastra. Students were relatively evenly distributed across the first and third years of study (40.3% and 40.1%, respectively). Detailed sample characteristics are presented in Table 1.
Reliability analysis
Internal consistency reliability of all multi-item scales was acceptable to good. The scale assessing availability of educational and support staff demonstrated acceptable internal consistency (Cronbach’s α=0.76). The perceived teaching quality scale showed good reliability (α=0.81), while the scale measuring perceived clinical skills of instructors also demonstrated good internal consistency (α=0.80).
Variable Frequency % Gender Female 340 92.6 Male 27 7.4 University DSHTM-UAMD 279 76.0 UGJ 88 24.0 Academic Program BSc 324 88.3 MP 43 11.7 Year of Study Year 1 148 40.3 Year 2 72 19.6 Year 3 147 40.1 Notes: DSHTM-UAMD = Department of Medical Technical Sciences, Aleksandër Moisiu University of Durrës; UGJ = University of Gjirokastra; BSc = Bachelor of Science; MP = Professional Master (Master’s level professional program).
The preparedness for practice scale, comprising 16 items, showed strong internal consistency (α=0.84), supporting its use as a composite outcome measure. Reliability for the teaching approaches scale was acceptable (α=0.78). The clinical learning environment (CLE) quality indicators scale demonstrated the highest internal consistency (α=0.86), indicating a high degree of coherence among items assessing logistical, supervisory, and infrastructural aspects of clinical placements.
Overall, Cronbach’s alpha coefficients ranged from 0.76 to 0.86, supporting the aggregation of items into composite scores for subsequent regression analyses.
Descriptive findings
Perceived availability of educational and support staff is presented in Table 2. Classroom instructors were most frequently reported as often available, whereas clinical supervisors/preceptors and academic mentors showed lower levels of perceived availability.
Perceived teaching quality and clinical skills of instructors are summarized in Tables 3a and 3b. Across both domains, clinical supervisors/preceptors received the lowest proportion of “good” ratings and the highest proportion of responses indicating need for improvement compared with classroom and skills-lab instructors.
Perceived preparedness for practice across clinical contexts and competencies is presented in Table 4. For all items, fewer than 40% of students reported “good” preparedness, with particularly low confidence observed for maternity services, rural practice, managerial tasks, and advocacy roles.
Staff role Often available n (%) Sometimes n (%) Rarely n (%) Never n (%) Classroom teachers/instructors 206 (56.1) 81 (22.1) 52 (14.2) 28 (7.6) Skills-lab/demonstration instructors 121 (33.0) 107 (29.2) 76 (20.7) 63 (17.2) Clinical supervisors/preceptors 117 (31.9) 85 (23.2) 98 (26.7) 67 (18.3) Academic advisors/mentors 126 (34.3) 91 (24.8) 84 (22.9) 66 (18.0) Librarians 116 (31.6) 86 (23.4) 71 (19.3) 94 (25.6) IT/technology support staff 107 (29.2) 94 (25.6) 76 (20.7) 90 (24.5)
Instructor group Good n (%) Adequate n (%) Needs improvement n (%) No opinion n (%) Classroom teachers/instructors 115 (31.3) 119 (32.4) 88 (24.0) 45 (12.3) Skills-lab/demonstration instructors 86 (23.4) 108 (29.4) 110 (30.0) 63 (17.2) Clinical supervisors/preceptors 86 (23.4) 97 (26.4) 119 (32.4) 65 (17.7)
Instructor group Good n (%) Adequate n (%) Needs improvement n (%) No opinion n (%) Classroom teachers/instructors 106 (28.9) 108 (29.4) 95 (25.9) 58 (15.8) Skills-lab/demonstration instructors 84 (22.9) 109 (29.7) 104 (28.3) 70 (19.1) Clinical supervisors/preceptors 87 (23.7) 104 (28.3) 102 (27.8) 74 (20.2)
Competency Good n (%) Somewhat prepared n (%) Poor n (%) Not at all Work in a primary care clinic 127 (34.6) 128 (34.9) 47 (12.8) 65 (17.7) Work in a municipal or regional hospital 140 (38.1) 123 (33.5) 45 (12.3) 59 (16.1) Work in a ward or outpatient clinic 130 (35.4) 130 (35.4) 51 (13.9) 56 (15.3) Work in maternity services 109 (29.7) 129 (35.1) 58 (15.8) 71 (19.3) Work in emergency units 122 (33.2) 129 (35.1) 50 (13.6) 66 (18.0) Work in a multidisciplinary healthcare team 138 (37.6) 125 (34.1) 45 (12.3) 59 (16.1) Work in rural settings 110 (30.0) 122 (33.2) 57 (15.5) 78 (21.3) Work with communities (community outreach) 113 (30.8) 127 (34.6) 55 (15.0) 72 (19.6) Provide services responding to local health needs using available resources 118 (32.2) 128 (34.9) 58 (15.8) 63 (17.2) Use information and communication technologies 117 (31.9) 123 (33.5) 72 (19.6) 55 (15.0) Apply clinical reasoning and critical thinking 122 (33.2) 141 (38.4) 56 (15.3) 48 (13.1) Perform managerial and administrative tasks 107 (29.2) 134 (36.5) 70 (19.1) 56 (15.3) Advocate for improved clinical practice environments 93 (25.3) 139 (37.9) 72 (19.6) 63 (17.2) Stay updated with new practices and service guidelines 114 (31.1) 137 (37.3) 66 (18.0) 50 (13.6) Engage in lifelong self-directed learning 132 (36.0) 137 (37.3) 54 (14.7) 44 (12.0) Conduct research 134 (36.5) 140 (38.1) 54 (14.7) 39 (10.6)
n (%)
Teaching approaches used in the programs are summarized in Table 5. Demonstrations by instructors and practical exercises were the most frequently used methods, whereas clinical simulations and role-play were among the least frequently reported.
Teaching approach Often used n (%) Sometimes used n (%) Never used n (%) Don’t know n (%) 1. Lectures 132 (36.0) 139 (37.9) 48 (13.1) 48 (13.1) 3. Recorded video lectures 99 (27.0) 145 (39.5) 72 (19.6) 51 (13.9) 7. Self-directed learning 124 (33.8) 153 (41.7) 45 (12.3) 45 (12.3) 8. Small-group learning 100 (27.2) 165 (45.0) 64 (17.4) 38 (10.4) 10. Demonstrations by instructors 148 (40.3) 150 (40.9) 37 (10.1) 32 (8.7) 12. Role-play 75 (20.4) 136 (37.1) 92 (25.1) 64 (17.4) 14. Community service-learning projects 92 (25.1) 153 (41.7) 74 (20.2) 48 (13.1) 16. Clinical simulations 91 (24.8) 159 (43.3) 67 (18.3) 50 (13.6) 19. Supervised practice 125 (34.1) 137 (37.3) 58 (15.8) 47 (12.8) 20. Practical exercises 146 (39.8) 146 (39.8) 36 (9.8) 39 (10.6) Note. Item numbers correspond to the original questionnaire numbering; only selected teaching approaches (most and least frequently used) are shown.
Ratings of key clinical learning environment domains during placements are shown in Table 6. Around half of students indicated that distance to clinical sites, transportation, supervision quality, assessment practices, and availability of equipment and supplies require improvement.
Domain No opinion n (%) Needs improvement n (%) Good n (%) Variety of clinical practice sites used (e.g., community clinics, district hospitals, referral hospitals) 54 (14.7) 185 (50.4) 128 (34.9) Distance to clinical practice sites 50 (13.6) 191 (52.0) 126 (34.3) Transportation to and from clinical sites 55 (15.0) 182 (49.6) 130 (35.4) Variety of patients in clinical settings 51 (13.9) 184 (50.1) 132 (36.0) Safety at clinical sites 54 (14.7) 186 (50.7) 127 (34.6) Quality of supervision at clinical practice sites 54 (14.7) 184 (50.1) 129 (35.1) Quality of teaching at clinical practice sites 50 (13.6) 191 (52.0) 126 (34.3) Quality of student assessment 52 (14.2) 187 (51.0) 128 (34.9) Alignment between classroom teaching and clinical training 52 (14.2) 185 (50.4) 130 (35.4) Availability of medical equipment and supplies 51 (13.9) 184 (50.1) 132 (36.0)
Multivariable logistic regression results
Multivariable logistic regression analysis showed that structural and pedagogical characteristics of the clinical learning environment were the primary factors associated with students’ perceived preparedness for practice. After adjustment, limited availability of clinical supervisors/preceptors was associated with more than a twofold increase in the odds of low perceived preparedness (aOR=2.17, 95% CI 1.45-3.25, p<0.001). Similarly, students exposed to a poorer overall clinical learning environment had significantly higher odds of low preparedness (aOR=2.84, 95% CI 1.89-4.27, p<0.001), representing the strongest association observed in the model.
Infrequent exposure to simulation-based teaching methods was also independently associated with low perceived preparedness (aOR=1.76, 95% CI 1.12-2.78, p=0.015), indicating a moderate but statistically significant effect. In contrast, university affiliation, academic program, and year of study were not significantly associated with preparedness after adjustment, suggesting that differences in perceived readiness were not driven by institutional or academic level factors but rather by qualitative aspects of clinical education.
Adjusted odds ratios, 95% confidence intervals, and p-values are presented in Table 7. Regression models used n=367.
Predictor Adjusted OR 95% CI p-value University (UGJ vs DSHTM-UAMD) 1.28 0.82-2.01 0.28 BSc program (vs Master) 1.41 0.77-2.59 0.26 Year of study 0.93 0.78-1.11 0.42 Low availability of clinical supervisors 2.17 1.45-3.25 <0.001 Poor clinical learning environment 2.84 1.89-4.27 <0.001 Low use of simulation-based teaching 1.76 1.12-2.78 0.015 Notes: Adjusted OR (aOR) = adjusted odds ratio from multivariable binary logistic regression; 95% CI = 95% confidence interval; p-value = probability value (two-sided). ORs are presented as aOR (95% CI).
Ordinal logistic regression (robustness analysis)
Findings from the ordinal logistic regression analysis were consistent with the binary model. Lower availability of clinical supervisors, poorer clinical learning environment quality, and limited use of simulation-based teaching remained significantly associated with progressively worse levels of perceived preparedness. Limited supervision nearly doubled the odds of reporting a lower preparedness category (aOR=1.94, 95% CI 1.34-2.81, p<0.001), while poor clinical learning environment quality was associated with a more than twofold increase in the odds of poorer preparedness (aOR=2.51, 95% CI 1.72-3.66, p<0.001). Reduced exposure to simulation-based teaching also showed a consistent association with lower preparedness levels (aOR=1.63, 95% CI 1.10-2.41, p=0.018).
As in the primary model, university affiliation, academic program, and year of study were not significantly associated with preparedness levels. The concordance between binary and ordinal models supports the robustness of the observed associations and confirms that preparedness deficits are primarily related to clinical supervision and learning environment quality rather than student seniority or institutional context. Full results of the ordinal model are presented in Table 8.
Predictor Adjusted OR 95% CI p-value Low availability of clinical supervisors 1.94 1.34-2.81 <0.001 Poor clinical learning environment 2.51 1.72-3.66 <0.001 Low use of simulation-based teaching 1.63 1.10-2.41 0.018 University (UGJ vs DSHTM-UAMD) 1.21 0.83-1.77 0.32 BSc program (vs Master) 1.19 0.71-2.01 0.50 Year of study 0.96 0.84-1.09 0.54 Notes: Adjusted OR (aOR) = adjusted odds ratio from ordinal logistic regression (proportional odds model); 95% CI=95% confidence interval;
p-value = probability value (two-sided). ORs are presented as aOR (95% CI) and represent the proportional odds of being in a lower preparedness category.
This study examined nursing students’ perceptions of educational quality and preparedness for practice, focusing on the clinical learning environment (CLE), supervision, teaching approaches, and structural conditions of clinical placements. The findings indicate that perceived preparedness is primarily shaped by organizational and pedagogical characteristics of clinical education, rather than by institutional affiliation, academic program, or year of study. This pattern is consistent with international evidence suggesting that preparedness for professional nursing practice is less a function of curricular content alone and more a product of how clinical education is structured, supported, and resourced [1, 13].
Clinical supervision emerged as one of the strongest determinants of perceived preparedness. Students reporting limited access to clinical supervisors or preceptors were significantly more likely to report low preparedness across both binary and ordinal regression models. This finding aligns with a substantial body of research identifying supervision as a cornerstone of effective clinical learning, influencing feedback quality, clinical reasoning development, professional identity formation, and patient safety awareness [14, 15].
From a learning theory perspective, supervision provides the scaffolding necessary for novice learners to transition from observation to independent performance. Inadequate supervision disrupts this process, leading to fewer guided learning opportunities, inconsistent feedback, and uncertainty regarding performance expectations [16]. Studies across Europe and Asia have similarly shown that insufficient supervision is associated with lower satisfaction, reduced confidence, and weaker perceived readiness for practice [2, 17]. Overall CLE quality – encompassing logistics, infrastructure, assessment practices, and theory-practice alignment – was the strongest predictor of preparedness in this study. Students exposed to poorer CLE conditions had substantially higher odds of reporting low preparedness, underscoring the role of system-level educational constraints rather than individual student characteristics.
Logistical barriers such as distance to clinical sites and transportation difficulties can reduce attendance, increase fatigue, and limit time available for reflective learning. Infrastructure limitations, including shortages of equipment and supplies, restrict hands-on practice and may shift learning toward observation-only experiences. These constraints have been widely documented in studies examining the theory–practice gap in nursing education [18, 19].
Assessment practices and alignment between theory and practice also emerged as areas of concern. When clinical assessment criteria are unclear or inconsistently applied across sites, students may perceive evaluations as subjective, undermining trust in the assessment process. Prior research has shown that transparent assessment frameworks and explicit linking of learning outcomes to clinical tasks are critical for reducing anxiety and improving perceived competence [20, 21].
Although demonstrations and supervised practice were frequently used teaching methods, simulation-based and role-play approaches were among the least utilized. Limited exposure to simulation was independently associated with poorer preparedness, supporting existing evidence that simulation-based education enhances clinical reasoning, psychomotor skill acquisition, and confidence, particularly when clinical exposure is inconsistent or constrained [22].
Simulation provides a structured environment where students can practice decision-making, receive immediate feedback, and learn from errors without patient risk. While it does not replace authentic clinical experience, it complements real-world practice by allowing repeated exposure to high-risk or low-frequency scenarios. Its underutilization may therefore contribute to persistent preparedness gaps, especially in resource-constrained educational systems [23].
After adjustment for CLE-related variables, institutional affiliation, academic program, and year of study were not significantly associated with preparedness. This finding suggests that preparedness is not simply a function of time spent in training or institutional context, but rather of the quality and organization of clinical education experiences. Similar findings have been reported in multi-institutional studies, where differences in preparedness were more strongly linked to supervision quality and learning environment than to program structure alone [24, 25, 26].
Implications for nursing education practice
The findings have several implications for nursing education. First, strengthening supervision systems through formalized preceptorship models, clear role definitions, and protected teaching time is likely to yield substantial gains in preparedness. Second, improving CLE conditions requires coordinated academic-clinical partnerships that address logistics, infrastructure, and assessment standardization. Third, systematic integration of simulation-based education may help mitigate variability in clinical learning opportunities and enhance readiness for practice.
Strengths and limitations
This study has several strengths that enhance its scientific relevance. First, it provides one of the most comprehensive empirical assessments of nursing students’ perceptions of educational quality and preparedness for practice in the Albanian context, addressing a notable gap in systematic data on the clinical learning environment, supervision, and teaching approaches using a structured and psychometrically sound instrument.
Second, the analytical strategy extends beyond descriptive reporting by integrating composite scale construction, reliability assessment, and multivariable modelling. The use of both binary and ordinal logistic regression enabled identification of robust, independent predictors of low perceived preparedness, strengthening inferential credibility.
Third, the study adopts a multidimensional perspective, capturing supervision, teaching quality, clinical skills, logistics, infrastructure, assessment practices, and pedagogical approaches simultaneously. This allows a more nuanced understanding of how interacting components of the clinical learning environment shape preparedness for practice.
Finally, inclusion of students from different academic levels and two public universities increased heterogeneity of clinical exposure and demonstrated that preparedness is driven primarily by system-level educational conditions rather than institutional affiliation. By aligning these findings with international evidence, the study contributes context-specific insights that reinforce the broader relevance and transferability of mechanisms influencing nursing preparedness across health systems.
Limitations include the cross-sectional design, which precludes causal inference, and reliance on self-reported preparedness rather than objective competency measures. Additionally, the inclusion of two universities limits generalizability to all nursing programs. Future research should incorporate objective assessments such as OSCE performance, supervisor ratings, and longitudinal follow-up to examine how CLE improvements translate into workforce readiness. Because the survey used mixed-mode distribution (classroom and online), the number of students who received an invitation could not be precisely determined, so a formal response rate could not be calculated.
CONCLUSION
1. Preparedness for nursing practice is strongly shaped by the conditions under which clinical education is delivered – particularly the availability and quality of clinical supervision, the overall clinical learning environment, and students’ exposure to simulation-based teaching.
2. Perceived readiness for practice is not primarily determined by institutional affiliation or academic seniority, but by modifiable system-level and pedagogical factors embedded within clinical training.
3. Insufficient supervision capacity, logistical barriers to clinical placements, and limited access to equipment and structured learning opportunities constrain students’ ability to translate theoretical knowledge into practical competence.
4. The underutilization of simulation-based and skills-lab teaching represents a missed opportunity to reduce variability in clinical exposure and supervision across sites and to strengthen competence development.
5. Addressing these gaps requires coordinated action between universities and clinical partners, prioritizing structured and supported preceptorship models, clearer alignment of clinical objectives with assessment criteria, improved placement planning and transport logistics, and strategic investment in simulation and skills-lab infrastructure.
6. Strengthening the clinical learning environment through targeted, system-level improvements offers a feasible, high-impact pathway to enhance nursing graduates’ readiness for practice and improve patient care quality and safety.
Contributors:
Bimi Indrit – Conceptualization, methodology, project administration, supervision, validation, writing – original draft;
Bimi Daniela – resources, data curation, software, formal analysis, writing – review & editing;
Llavdaniti Mimoza – investigation.
Funding. This research received no external funding.
Conflict of interests. The authors declare no conflict of interest.
REFERENCES
1. Panda S, Dash M, John S, et al. Challenges faced by student nurses and midwives in the clinical learning environment: a systematic review and meta-synthesis. Nurse Educ Today. 2021;105:105141. doi: https://doi.org/10.1016/j.nedt.2021.105141
2. Cant R, Ryan C, Cooper S. Nursing students’ evaluation of clinical practice placements using the Clinical Learning Environment, Supervision and Nurse Teacher scale (CLES+T): a systematic review of the psychometric properties and factors influencing student satisfaction. Nurse Educ Today. 2021;104:104983. doi: https://doi.org/10.1016/j.nedt.2021.104983
3. Zhang Y, Wei W, Zhang L, et al. The clinical learning environment, supervision and future intention to be a nurse in nursing students: a cross-sectional and descriptive study. BMC Med Educ. 2022;22:548. doi: https://doi.org/10.1186/s12909-022-03609-y
4. World Health Organization. State of the world’s nursing 2025: investing in education, jobs, leadership and service delivery [Internet]. Geneva: World Health Organization; 2025 [cited 2025 Nov 28]. Available from: https://www.who.int/publications/i/item/9789240110236
5. Forbes H, Järvinen T, Korhonen A, et al. Exploring assessment policies for clinical practice: a scoping review. Nurse Educ Pract. 2023;68:103588. doi: https://doi.org/10.1016/j.nepr.2023.103588
6. Davis K, Stipcevich M, Cant R, Ryan C, Bogossian F. Addressing nursing student clinical placement poverty concerns: a discussion paper. Nurse Educ Today. 2025;144:106483. doi: https://doi.org/10.1016/j.nedt.2024.106483
7. Alhassan A, Duke M, Phillips NM. Nursing students’ satisfaction with the quality of clinical placement and their perceptions of preceptors competence: a prospective longitudinal study. Nurse Educ Today. 2024;133:106081. doi: https://doi.org/10.1016/j.nedt.2023.106081
8. Cronbach LJ. Coefficient alpha and the internal structure of tests. Psychometrika. 1951;16(3):297-334. doi: https://doi.org/10.1007/BF02310555
9. R Core Team. R: a language and environment for statistical computing [Internet]. Vienna: R Foundation for Statistical Computing; 2023 [cited 2025 Nov 28]. Available from: https://www.R-project.org/
10. Hosmer DW, Lemeshow S, Sturdivant RX. Applied logistic regression. 3rd ed. Hoboken (NJ): Wiley; 2013. doi: https://doi.org/10.1002/9781118548387
11. Agresti A. An introduction to categorical data analysis. 3rd ed. Hoboken (NJ): Wiley; 2019.
12. McCullagh P. Regression models for ordinal data. J R Stat Soc Ser B. 1980;42(2):109-42. doi: https://doi.org/10.1111/j.2517-6161.1980.tb01109.x
13. Cant R, Ryan C, Cooper S, et al. Nursing student voices: a qualitative thematic synthesis of education elements supporting nursing students’ clinical learning during placement. Nurse Educ Pract. 2024;80:104150. doi: https://doi.org/10.1016/j.nepr.2024.104150
14. Russ D, Whiteing N, Aggar C. An integrative review of nursing students’ clinical placement experiences throughout their nursing degrees. Collegian. 2023;30(1):154-62. doi: https://doi.org/10.1016/j.colegn.2022.07.002
15. Kurt E, Eskimez Z. Examining self-regulated learning of nursing students in clinical practice: a descriptive and cross-sectional study. Nurse Educ Today. 2022;109:105242. doi: https://doi.org/10.1016/j.nedt.2021.105242
16. Jadalla A, Hardan-Khalil K, Dyo M, et al. The perceived preparedness of prelicensure nursing students to transition to practice. Teach Learn Nurs. 2024;19(3):260-4. doi: https://doi.org/10.1016/j.teln.2024.04.001
17. Ugwu SN, Ogbonnaya NP, Chijioke VC, Esievo JN. Causes and effects of theory-practice gap during clinical practice: the lived experiences of baccalaureate nursing students. Int J Qual Stud Health Well-being. 2023;18:2164949. doi: https://doi.org/10.1080/17482631.2023.2164949
18. Ota Y, Aikawa G, Nishimura A, et al. Effects of educational methods using extended reality on pre-registration nursing students’ knowledge, skill, confidence, and satisfaction: a systematic review and meta-analysis. Nurse Educ Today. 2024;141:106313. doi: https://doi.org/10.1016/j.nedt.2024.106313
19. Lee TW, Damiran D, Konlan KD, Ji Y, Yoon YS, Ji H. Factors related to readiness for practice among undergraduate nursing students: a systematic review. Nurse Educ Pract. 2023;68:103614. doi: https://doi.org/10.1016/j.nepr.2023.103614
20. Lee TW, Damiran D, Konlan KD, et al. Clinical readiness for practice of nursing students: a concept analysis. Int J Environ Res Public Health. 2024;21(12):1610. doi: https://doi.org/10.3390/ijerph21121610
21. von Elm E, Altman DG, Egger M, et al. The Strengthening the Reporting of Observational Studies in Epidemiology (STROBE) statement: guidelines for reporting observational studies. PLoS Med. 2007;4(10):e296. doi: https://doi.org/10.1371/journal.pmed.0040296
22. Groves RM, Fowler FJ Jr, Couper MP, et al. Survey methodology. 2nd ed. Hoboken (NJ): Wiley; 2009. ISBN: 978-0-470-46546-2
23. Fowler FJ Jr. Survey research methods. 5th ed. [Internet]. Thousand Oaks (CA): SAGE; 2014 [cited 2025 Nov 28]. Available from: https://www.perlego.com/book/4792018/survey-research-methods-pdf
24. Szklo M, Nieto FJ. Epidemiology: beyond the basics. 4th ed. Burlington (MA): Jones & Bartlett Learning; 2019. ISBN: 9781284116595
25. Görücü Y, Günüşen NP, Arslan GG, et al. The effect of simulation-based learning on nursing students’ clinical decision-making skills: systematic review and meta-analysis. Nurse Educ Today. 2024;137:106270. doi: https://doi.org/10.1016/j.nedt.2024.106270
26. Ryan C, Hyun A, Hughes L, Bogossian F, Cooper S. Nursing students’ evaluation of clinical placement education quality: a national database analysis. Nurse Educ Pract. 2024;81:104185. doi: https://doi.org/10.1016/j.nepr.2024.104185
Key words: disability, acute cerebral stroke, functional impairment, adult population, labor force
Ключові слова: інвалідність, гострий мозковий інсульт, порушення життєдіяльності, доросле населення, працездатне населення
Abstract
Acute cerebral stroke is a disease that ranks among the leading causes of today's “non-infectious” epidemic, becoming a significant economic burden for global economies. The aim of the study was to investigate the dynamics of disability rates due to acute cerebral stroke and their features among the adult and working-age population in Ukraine under conditions of martial law. This work is fragment of the DSMU research project “Improvement of scientific and methodological approaches to determining the criteria for identifying signs of permanent disability, optimization of rehabilitation programs for patients and persons with disabilities”, No. 0124U005028, 2025-2028. Medical and social cases and referrals for medical and social examination (Form 088/o) of patients who were diagnosed with disability for the first time during the period of 2014-2024 were analyzed in accordance with ICD-10 codes: stroke (I 60 I 64), hemorrhagic stroke (I 60, I 61, I 62), ischemic stroke (I 63, I 64), and consequences of stroke (I 69). Statistical processing was performed using parametric and nonparametric statistical methods implemented in the STATISTICA 6.1 software package (StatSoftInc., serial number AGAR909E415822FA).The results of the study conducted over the last decade from 2013 to 2024 in Ukraine determined the dynamics of primary disability rates due to acute cerebral stroke. Among the adult and working-age population during 2011-2019, a stable dynamic of the indicator was found, which averaged 1.67 per 10,000 people, with a minimum level in 2020 – 1.3 and 1.7 per 10,000 people, respectively. The conclusions of the study are the identified characteristics of primary disability rates due to acute cerebral stroke ubder conditions of martial law. In 2022-2024, an increase in this indicator among both the adult and working-age population was identified, being approximately twice as compared to pre-war indicators.
Реферат
Інвалідність унаслідок гострих мозкових інсультів в Україні за період 2014-2024 років та особливості динаміки в умовах воєнного стану. Борисова І.С., Сафонов Д.О. Гострий мозковий інсульт є захворюванням, що займає основні позиції серед причин неінфекційної епідемії сьогодення, стаючи значним економічним тягарем для світових економік. Метою роботи було дослідити динаміку показників інвалідності серед дорослого та працездатного населення внаслідок гострого мозкового інсульту в Україні та їх особливості в умовах воєнного стану. Робота є фрагментом НДР ДДМУ «Удосконалення науково-методичних підходів до визначення критеріїв визначення ознак стійкої непрацездатності, оптимізації програм реабілітації хворих та осіб з інвалідністю», № 0124U005028, 2025-2028 рр. Проаналізовано медико-соціальні справи та направлення на медико-соціальну експертизу (форма 088/о) пацієнтів, яким було встановлено інвалідність уперше за період 2011-2024 рр. відповідно до кодів МКБ Х: інсульт (I 60 I 64), геморагічний інсульт (I 60, I 61, I 62), ішемічний інсульт (I 63, I 64), наслідки інсульту (I 69). Статистична обробка проводилась методами параметричної та непараметричної статистики, реалізованими в пакетах програмних продуктів STATISTICA 6.1 (StatSoftInc., серійний № AGAR909E415822FA). Результатами проведеного дослідження за період останнього десятиріччя з 2011 до 2024 року в Україні визначено динаміку показників первинної інвалідності внаслідок гострого мозкового інсульту. Серед дорослого і працездатного населення впродовж 2011-2019 рр. виявлено стабільну динаміку показника, який становив у середньому 1,67 на 10 тис. нас. з мінімальним рівнем у 2020 р – 1,3 та 1,7 на 10 тис. нас. відповідно. Висновками дослідження є визначені особливості показників первинної інвалідності внаслідок гострого мозкового інсульту в період воєнного стану. У 2022-2024 роках визначено підвищення цього показника як серед дорослого, так і працездатного населення приблизно у 2 рази порівняно з довоєнними показниками.
Acute cerebral stroke (ACS) is a disease that occupies a leading position among the causes of the “non-infectious” epidemic of today, becoming a significant economic burden for world economies.
In 2017, 1.5 million people in 32 European countries suffered from ACS, while 0.4 million of them died. At the same time, direct costs for care for ACS amounted to 27 billion euro, which amounted to 1.7% of healthcare expenditures in Europe as a whole [1]. In the same year, according to the Global Burden of Disease study, 24.1 million of new cases of ACS were registered worldwide [2]. And already in 2019 this figure reached 101 million (93.2-111) of common ACS and 6.55 million (6.00-7.02) of deaths from stroke, ranking second among the leading causes of death globally, accounting for 11.6% [10.8-12.2] of the total number of deaths recorded in 2019. According to the analysis, the dynamics is disappointing: from 1990 to 2019, the absolute number of strokes increased by 70.0% (67.0-73.0) [3]. At the same time, it is predicted that in the coming decades, the number of cases of ACS will increase by 34%, which will lead to a 27% increase in costs, amounting to 1.7% of total healthcare costs [1]. It is known that direct medical costs per patient with ACS in the first year are $59,900 in the USA, $52,725 in Sweden, and $41,950 in Spain [4].
According to estimates by the National Health Service (NHS) in Ukraine in 2021, 118 thousand cases of ACS were diagnosed, and already in 2024 the number of hospitalizations for this reason reached 137.6 thousand cases, which is by 16% higher. Diagnosis and treatment of ACS in Ukraine are completely free of charge, as they are a priority service in the Medical Guarantees Program. Currently, there are 229 healthcare institutions (HCIs) in the country that provide care for ACS. For the treatment of one patient with ACS, the HCI receives 131,472 hryvnias from the National Health Service of Ukraine (NHSU) for the provision of care with the use of endovascular interventions; 62,565 hryvnias for care with the use of thrombolytic therapy; 14,952 hryvnias for care without endovascular interventions or thrombolytic therapy. In 2023 alone, under the “Medical Care for ACS” package, Ukrainian HCIs received reimbursement of over 1.7 billion hryvnias for the services provided [5]. Unfortunately, the mortality rate from ACS in Ukraine remains 2-3 times higher than in the EU: in 2024, the hospital mortality rate was 16.62%, and the 30-day mortality rate was 21.85%. In September 2025, the fourth UN meeting on non-communicable diseases noted that the European target of reducing mortality by 1/3 by 2030 had not yet been achieved, and that prevention was the key to progress [5].
It is also important to note that the consequences of ACS among surviving patients are becoming one of the leading causes of disability in the world, despite modern advances in methods [6]. In both the United States and European countries, ACS remains the leading neurological disease in terms of the number of DALYs (Disability-Adjusted Life Years) – an indicator of "life years adjusted for disability", which measures the total "burden" of disease, disability and premature death. The indicator is equal to the time of healthy life lost due to premature death or disability [7]. Thus, the financial burden of ACS on society is enormous, taking into account rehabilitation services, costs of homes for people with additional supervision and assistance with self-care, reimbursement of drug costs by insurance, informal care from the state, volunteers or relatives and potential loss of earnings. Thus, the DALY indicator in 2017 amounted to 15.7 million disability-adjusted life years [8]. And in 2019, the global economy lost 143 million (133-153) years of life due to ACS. The consequences of ACS have become the third leading cause of disability in the world, with an increase in DALYs by 32.0% (22.0-42.0) and a decrease in life expectancy by 36.0% (31.0-42.0) compared to studies done in 2017 [3]. Indirect costs of ACS in Europe include social security for people who have suffered ACS, which is estimated at €5 billion. The annual cost of caring for people with GMI in 2019 was €59 per EU citizen on average, ranging from €11 in Bulgaria to €140 in Finland. Productivity losses cost the European economy €12 billion, and were divided equally between causes of premature death and lost working hours. In total, €1.3 billion in informal care hours were provided to people who had suffered a stroke, costing Europe another €16 billion. [1]. The highest costs per patient after a stroke over a lifetime were recorded in Australia, which amounted to $232,000 [9].
In the USA, indirect costs exceed 60% of total costs for ACS and amount to $103.5 billion as of the beginning of 2020, with a loss of productivity due to disability, being $38.1 billion [10]. At the same time, according to the calculations of the American Heart Association, the average cost of treatment for a person who has suffered ACS may exceed $100 thousand. [11]. Linear interpolation shows that if current trends continue, by 2050, there will be up to 200 million people with the past stroke worldwide annually, who will need rehabilitation and social assistance, which will inevitably lead to a 27% increase in medical and social assistance costs, which will approach 1.7% of total global health care costs [1].
It is also important to emphasize that in Ukraine among people with past ACS about 35% are those of working age. According to official data, from 20 to 40% of people who have survived ACS cease to be independent and are completely dependent on outside help, another 12.5% fall into the category of primary disability. And only 10% return to the state they had before the onset of the disease. Such annual losses cannot but affect the state economy. According to some scientists, the total losses of the Ukrainian economy associated with the consequences of ACS can reach about 100 billion UAH per year [12]. The Framingham study showed that after past ACS, signs of disability were formed in 22-40% of patients after 6 months [13], and after 1 year - in almost 50% [14]. The share of people with disabilities due to ACS in China in 2020 was 63.8%; including the share of mild, moderate, severe and complete disability – 30.1%, 18.0%, 10.7% and 5.0% respectively [15]. According to the Korean National Survey for the period of 2007-2018 (KNHANES), it is known that 38.0% of those who survived ACS became disabled [16].
According to previous studies, in Ukraine in 2009, among people with past ACS of all forms, 32.7% died, and 7.8% received one or another degree of disability [17]. It is known that among the main groups of disabling diseases, cerebrovascular diseases (the main contribution among which is the consequences of ACS) rank forth among the main causes of disability by the cause of “general disease” (after neoplasms, injuries and diseases of the musculoskeletal system and connective tissue) both among the adult and among the able-bodied population [17].
The aim of the study was to investigate the dynamics of disability rates due to acute cerebral stroke and their features among the adult and working-age population in Ukraine under conditions of martial law.
MATERIALS AND METHODS OF RESEARCH
The work is a fragment of the research work (R&D) of the Department of Medical and Social Expertise and Rehabilitation of the Dnipro State Medical University (DSMU) "Improvement of scientific and methodological approaches to determining the criteria for limiting vital activity due to the consequences of injuries and diseases (in the system of medical and social expertise)", No. 0121U100080, 2021-2024 and "Improvement of scientific and methodological approaches to determining the criteria for determining signs of persistent disability, optimizing rehabilitation programs for patients and persons with disabilities", No. 0124U005028, 2025-2028. By its type the research consisted of two stages. In the course of the research, primary disability indicators in Ukraine according to state statistical materials and data of scientific literature during 2010-2019 were studied [17, 18]. The next stage of the work was carried out at the clinical base of the state institution “Ukrainian State Scientific Research Institute of Medical and Social Problems of Disability of the Ministry of Health of Ukraine” according to the reports of regional centers of medical and social expertise (MSE) during 2020-2024. The MSE commissions [19] were asked to submit aggregate statistical information according to the ICD codes: cerebrovascular pathology: stroke (I 60 I 64), hemorrhagic stroke (I 60, I 61, I 62), ischemic stroke (I 63, I 64), consequences of stroke (I 69) and transient ischemic attacks (G 45). We analyzed the medical and social cases and referrals for medical and social expertise (Form 088/o) of 29,024 patients who were examined by specialized cardio-neurological commissions and formed the study group, quantization by years: 2021 – 4,619 people; 2022 – 7,219 people; 2023 – 9,431 people; 2024 – 7,779 people. The disability criteria were considered to be persistent functional impairments, associated limitations in life activity criteria and the need for state assistance, in accordance with the regulatory documents in force at the time of the study [20].
The research calculated intensive indicators of the prevalence of primary disability due to ASC among adults and able-bodied people (per 10,000 population) and specific gravity (in %), their dynamics over the period of the 2011-2024 was studied [21]. In connection with the declaration of martial law in Ukraine on February 22, 2022, the State Statistics Service put on pause the publication of data on the demographic situation in Ukraine, which does not allow the calculation of real intensive indicators for 2022, 2023 and 2024. In this regard, the calculation of intensive indicators was carried out based on the latest state statistical data by regions of Ukraine as of January 1, 2022 [22].
The processing of the obtained research results using biostatistical methods was carried out using the STATISTICA v.6.1 software product (StatsoftInc., USA), license number AGAR909E415822FA. In particular, an analysis of the 10-year dynamics of disability indicators was carried out with the calculation of average growth rates (Δ) according to the formula:
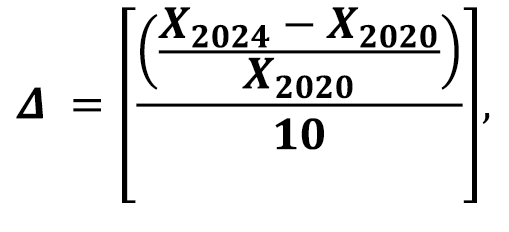
where
X – is the studied indicator for a specific year of statistical observation;
10 – is the number of years of observation.
The study was conducted in compliance with the basic norms of bioethics and the requirements of the Helsinki Declaration on Human Rights and Biomedicine (1977) and relevant laws of Ukraine and was permitted by the Commission on Biomedical Ethics of the DSMU (Protocol No. 32 dated November 11, 2025).
RESULTS AND DISCUSSION
Figures 1 and 2 present the determined intensive indicators of primary disability due to ACS in Ukraine, calculated per 10 thousand population for the period of 2011-2024 among the adult and working-age population, respectively. The prevalence rate of primary disability among the adult population of Ukraine due to the consequences of ACS was: 1.9 per 10 thousand population in 2011; 1.6 – in 2012; 1.8 – in 2013; 1.7 – in 2014; 1.6 – in 2015; 1.5 – in 2016; 1.6 – in 2017; 1.8 – in 2018; 1.6 – in 2019; 1.3 – in 2020; 1.5 – in 2021; 2.1 – in 2022; 3.1 – in 2023, and 3.1 – in 2024.
Thus, a stable dynamics of the prevalence rate of primary disability among the adult population during 2011-2019 was revealed – from 1.9 in 2011 to 1.6 in 2019. During this period, the rate averaged 1.67 per 10 thousand people. It is important to note that well-known Ukrainian epidemiological studies on the “consequences of stroke”, which were the cause of primary disability over the period of 2002-2012 in Ukraine also determined a certain stable dynamics and were, respectively: 10.3; 10.3; 9.4; 10.7; 12.3; 10.6; 9.3; 9.0-10.1; 9.7 people per 100 thousand adults[18]. Other researchers also determined the absence of significant changes in the rate of primary disability due to ACS among the adult population in 2008-2010, which was 10.6-9.3-9.9 cases per 100 thousand people [17]. In our study, the minimum prevalence rate of primary disability among the adult population was determined in 2020, which was 1.3 per 10 thousand people, with a slight increase in 2021 to 1.5 per 10 thousand people. A significant increase in the indicator was found during the martial law period, when the indicator grew from 2.1 in 2022 to 3.1 in 2023-2024. The increase in the indicator during the war years grew by 1.6 times (+51.6%) compared to the stable period. The average annual growth rate (Δ) for the studied period was 0.277 or 27.7% per year.
The prevalence rate of primary disability of the working-age population due to the consequences of ACS in Ukraine in 2011 was 2.4 per 10,000 population, in 2012 – 2.2; in 2013 – 2.3; in 2014 – 2.3; in 2015 – 2.1; in 2016 – 1.9; in 2017 – 2.0; in 2018 – 2.1; in 2019 – 2.0; in 2020 – 1.7; in 2021 – 1.9; in 2022 – 2.7; in 2023 – 3.4 and in 2024 – 2.5.
Among the working-age population, the results of the study revealed a stable dynamics of the prevalence rate of primary disability during 2011-2019 – from 2.4 in 2011 to 2.0 in 2017-2019. During this period, the rate averaged 2.4 per 10 thousand people. The minimum rate of primary disability among the working-age population was determined in 2020, being 1.7 per 10 thousand people, with an insignificant increase to 1.9 per 10 thousand people in 2021. During the period of martial law in 2022-2024, a significant increase in this rate among the working-age population was detected, which rose to 3.4 per 10 thousand people in 2023. At the same time, the increase in the indicator during the war years was 1.7 times (+50%) as compared to the stable period. The average annual growth rate (Δ) for the studied period was 0.094 or 9.4%.
In the process of discussing the results obtained, it is important to emphasize the reasons for the consistent decrease in primary disability rates up to 2020, both among adults and the able-bodied population, due to the fact that in these years the state introduced contracting of health care institutions (HCIs) through the NHSU with clear requirements for the provision of primary care for ACS and a list of mandatory diagnostic and treatment procedures. In 2020 alone, the NHSU contracted 192 HCIs to provide care to patients with ACS, reimbursing over 965 million UAH. At the same time, in Ukraine, 31,151 patients received primary care for ACS [23]. In the case of therapeutic endovascular interventions, the NHSU tariff for 1 person is over 97 thousand hryvnias, and the cost of ACS treatment using thrombolytic therapy is 54 thousand hryvnias [24]. In the same year, the Order of the Ministry of Health on the organization of medical care for patients with suspected ACS in the emergency medical care system was updated [25]. A significant increase in the rate of primary disability due to ACS during the period of martial law, both among the adult and able-bodied population of Ukraine, despite the adoption of new standards for providing care for ischemic and hemorrhagic types of ACS is noteworthy [26]. The increase in disability rates due to ACS in 2021 can be explained by the accumulation of disabling consequences of strokes associated with COVID-19. Neurological complications of COVID-19 are known to occur in more than a third of patients [27]. In patients with severe SARS-CoV-2 infection requiring intensive care unit treatment, the prevalence of neurological complications was as high as 84% [28]. The incidence of ACS in one of the first studies of neurological complications of COVID-19 in Wuhan was 2.34%. A large-scale meta-analysis including 24 cohort studies and more than 108 patients with COVID-19 found the incidence of ACS to range from 0.4 to 8.1% [29], making it the most common neurological complication among hospitalized patients with COVID-19 [30].
The reasons for the further increase in disability rates during the martial law period, which undoubtedly affected both the adult and working-age population of Ukraine, are special. Thus, it is known that the impact of armed conflicts significantly affects the increase in the prevalence of CVD with a chronic and acute course [31]. As a rule, this occurs due to the increase in the prevalence of risk factors associated with martial law, in particular, this has been confirmed in national studies of recent years: acute events on the background of CVD due to chronic or acute stress increased by 4.3 times and by 2 times due to excessive alcohol consumption [32]. Ukrainian researchers record an increase in the number of ACS by 22% against the background of an increase in the total number of hospitalizations in some front-line areas up to 60% [33]. Thus, according to the National Health Service, the regions where the largest number of patients with ACS were treated in 2023 are: Dnipropetrovsk (8,176 people), Kharkiv (6,443 people), Kyiv (5,993 people) and Lviv (5,184 people) regions and the city of Kyiv (7,889 people). It is these features of the course of ACS in modern conditions that have become the reasons for the increase in the rate of primary disability among Ukrainians of working age.
The features of understanding “disability” as a social phenomenon are: persons with disabilities in any state have the right to certain social measures of protection and assistance. As for the disability rate due to ACS among the adult population, it should be understood that under martial law, this rate increased due to the so-called “hidden disability”. In Ukraine, it is legally established that a person is not entitled to receive several social material benefits at the same time. Thus, some actual persons with disabilities due to ACS who reached retirement age did not apply for disability status before the war. At the same time, under martial law, these persons were forced to apply for this status in connection with other social benefits related to the specifics of this period.
CONCLUSIONS
1. The results of the study conducted in Ukraine for the period from 2011 to 2024 determined the dynamics of primary disability indicators due to acute cerebral stroke. Among the adult and able-bodied population during 2011-2019, a stable dynamics of this indicator was found, being an average of 1.67 per 10 thousand people with a minimum level in 2020 – 1.3 and 1.7 per 10 thousand people, respectively.
2. The study identified certain features of primary disability indicators due to acute cerebral stroke under the conditions of martial law. In 2022-2024, an increase in this indicator was established among both the adult and able-bodied population by approximately 2 times compared to the pre-war period. This may be explained by a number of factors, including: increased prevalence of risk factors, stress associated with martial law, and the phenomenon of “hidden disability.”
Contributors:
Borysova I.S. – conceptualization, methodology, formal analysis, visualization, writing – review & editing, project administration;
Safonov D.O. – investigation, resources, visualization, writing – original draft.
Funding. The article is a fragment of the scientific and research work of DSMU "Improvement of scientific and methodological approaches to determining the criteria for limiting vital activity due to the consequences of injuries and diseases (in the system of medical and social expertise)", No. 0121U100080, 2021-2024 and "Improvement of scientific and methodological approaches to determining the criteria for identifying signs of persistent disability, optimization of rehabilitation programs for patients and persons with disabilities" No. 0124U005028, 2025-2028.
Conflict of interests. The authors declare no conflict of interest.
REFERENCES
1. Luengo-Fernandez R, Violato M, Candio P, Leal J. Economic burden of stroke across Europe: A population-based cost analysis. Eur Stroke J. 2020 Mar;5(1):17-25. doi: https://doi.org/10.1177/2396987319883160
2. GBD 2016 Stroke Collaborators. Global, regional, and national burden of stroke, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol. 2019 May;18(5):439-58. doi: https://doi.org/10.1016/S1474-4422(19)30034-1
3. GBD 2019 Stroke Collaborators. Global, regional, and national burden of stroke and its risk factors, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet Neurol. 2021 Oct;20(10):795-820. doi: https://doi.org/10.1016/S1474-4422(21)00252-0
4. Strilciuc S, Grad DA, Radu C, Chira D, Stan A, Ungureanu M, et al. The economic burden of stroke: a systematic review of cost of illness studies. J Med Life. 2021 Sep-Oct;14(5):606-19. doi: https://doi.org/10.25122/jml-2021-0361
5. Shepelya V. [How much does the National Health Insurance Fund pay to medical institutions for the treatment of each patient with a stroke?]. [Internet]. 2024 [cited 2025 Aug 25]. Ukrainian. Available from: https://medicine.rayon.in.ua/news/670492-skilki-platit-nszu-medzakladam-za-likuvannya-kozhnogo-patsienta-z-insultom
6. Benjam EJ, Munter P, Alonso A, Bittencourt Refer MS, Calloway CW, Carson AP, et al. Heart sickness A stoke information-2019 update: A report from the yank heart affiliation flow. Circulation. 2019;139(10):e56-C528. doi: https://doi.org/10.1161/CIR.00000000000000659
7. GBD 2017 US Neurological Disorders Collaborators. Burden of Neurological Disorders Across the US From 1990-2017: A Global Burden of Disease Study. JAMA Neurol. 2021 Feb 1;78(2):165-76. doi: https://doi.org/10.1001/jamaneurol.2020.4152
8. Krishnamurthi RV, Ikeda T, Feigin VL. Global, Regional and Country-Specific Burden of Ischaemic Stroke, Intracerebral Haemorrhage and Subarachnoid Haemorrhage: A Systematic Analysis of the Global Burden of Disease Study 2017. Neuroepidemiology. 2020;54(2):171-9. doi: https://doi.org/10.1159/000506396
9. Strilciuc S, Grad DA, Radu C, Chira D, Stan A, Ungureanu M, et al. The economic burden of stroke: a systematic review of cost of illness studies. J Med Life. 2021 Sep-Oct;14(5):606-19. doi: https://doi.org/10.25122/jml-2021-0361
10. Girotra T, Lekoubou A, Bishu KG, Ovbiagele B. A contemporary and comprehensive analysis of the costs of stroke in the United States. J Neurol Sci. 2020 Mar 15;410:116643. doi: https://doi.org/10.1016/j.jns.2019.116643
11. The True Cost of a Stroke in the US [Internet]. Resolve. 2023 Oct 31 [cited 2025 Sep 15]. Available from: https://www.resolvemedicalbills.com/blog/the-true-cost-of-a-stroke-in-the-us
12. [Stroke statistics in Ukraine. Life-House Stroke Rehabilitation Center]. Health of Ukraine in the 21st century [Internet]. 2025 [cited 2025 Aug 10];7(593). Ukrainian. Available from:
https://life-house.center/statystyka-insultiv-v-ukrain/
13. Kelly-Hayes M, Beiser A, Kase CS, Scaramucci A, D'Agostino RB, Wolf PA. The influence of gender and age on disability following ischemic stroke: the Framingham study. J Stroke Cerebrovasc Dis. 2003 May-Jun;12(3):119-26. doi: https://doi.org/10.1016/S1052-3057(03)00042-9
14. Jönsson AC, Delavaran H, Iwarsson S, Ståhl A, Norrving B, Lindgren A. Functional status and patient-reported outcome 10 years after stroke: the Lund Stroke Register. Stroke. 2014 Jun;45(6):1784-90. doi: https://doi.org/10.1161/STROKEAHA.114.005164
15. Lv Y, Sun Q, Li J, Zhang W, He Y, Zhou Y. Disability Status and Its Influencing Factors Among Stroke Patients in Northeast China: A 3-Year Follow-Up Study. Neuropsychiatr Dis Treat. 2021;17:2567-73. doi: https://doi.org/10.2147/NDT.S320785
16. Ju YW, Lee JS, Choi YA, Kim YH. Causes and Trends of Disabilities in Community-Dwelling Stroke Survivors: A Population-Based Study. Brain Neurorehabil. 2022;15(1):e5. doi: https://doi.org/10.12786/bn.2022.15.e5
17. Khobzey NK, Mishchenko TS, Golik A, Gondulenko NA. [Features of Epidemiology of disability in diseases of the nervous system in Ukraine]. Mezhdunarodnyi nevrologicheskii zhurnal. [Internet]. 2011 [cited 2025 Aug 10];5(43):15-9. Russian. Available from: https://www.mif-ua.com/archive/article/21505
18. Golik VA, Gondulenko NA, Moroz YeN, Boguslavskii DD, Pogorelova VA. [Peculiarities of the epidemiology of disability in diseases of the nervous system in Ukraine: clinical and expert comparisons (10-year Ukrainian experience)]. Ukrainskyi visnyk medyko-sotsialnoi ekspertyzy. [Internet]. 2013 [cited 2025 Nov 10];7(1):33-41. Russian. Available from: http://irbis-nbuv.gov.ua/cgi-bin/irbis_nbuv/cgiirbis_64.exe?C21COM=2&I21DBN=UJRN&P21DBN=UJRN&IMAGE_FILE_DOWNLOAD=1&Image_file_name=PDF/ujmse_2013_1_7.pdf
19. [Issues of medical and social expertise. Resolution of the Cabinet of Ministers of Ukraine No. 1317 of 3.12.2009 (as amended in accordance with Resolutions of the Cabinet of Ministers No. 752 of 18.08.2010, No. 762 of 20.07.2011; No. 485 of 31.05.2012; No. 482 of 26.06.2015; No. 874 of 21.10.2015; No. 569 of 31.08.2016)]. [Internet]. 2016 [cited 2025 May 02]. Ukrainian. Available from: http://zakon3.rada.gov.ua/laws/show/1317-2009-%D0%BF
20. [Some issues of introducing assessment of daily functioning of a person. Resolution of the Cabinet of Ministers of Ukraine No. 1338 of 2024 Nov 15 [Internet]. 2024 [cited 2025 Jul 21]. Ukrainian. Available from: https://zakon.rada.gov.ua/laws/show/1338-2024-%D0%BF#Text
21. Hruzieva TS, Lekhan VM, Ohniev VA, et al. [Public Health: textbook]. [Internet]. Vinnytsia: New book; 2023 [cited 2025 Jul 21]. Ukrainian. Available from: http://ir.librarynmu.com/bitstream/123456789/11903/1/Громадське%20здоров%27я%202023.pdf
22. [Population of Ukraine – 2021: statistical collection]. [Internet]. Kyiv: State statistics service of Ukraine; 2022 [cited 2026 Nov 10]. Ukrainian. Available from: https://www.ukrstat.gov.ua/druk/publicat/kat_u/2022/zb/10/zb_nasel%20_2021.pdf
23. [The National Health Insurance Fund of Ukraine paid over UAH 965 million to medical institutions for providing assistance to patients with heart attacks and strokes]. LB.ua [Internet]. 2020 Sep 22 [cited 2025 Jul 09]. Ukrainian. Available from: https://lb.ua/society/2020/09/22/466514_nszu_viplatila_medzakladam_ponad_965.html
24. [The NHSU pays for the treatment of each stroke patient: assistance can be obtained in 238 hospitals across the country]. Government portal [Internet]. 2021 Oct 28 [cited 2025 Oct 13]. Ukrainian. Available from: https://www.kmu.gov.ua/news/za-likuvannya-kozhnogo-paciyenta-z-insultom-platit-nszu-otrimati-dopomogu-mozhna-u-238-likarnyah-po-vsij-krayini
25. [On approval of the Procedure for organizing the provision of medical care to patients with suspected acute cerebral stroke in the emergency medical care system. Order of the Ministry of Health of Ukraine No. 2203 dated 2020 Sept 25]. [Internet]. 2020 [cited 2025 Oct 09]. Ukrainian. Available from: https://zakon.rada.gov.ua/laws/show/z1120-20#Text
26. [On approval of the Standard of medical care «Ischemic Stroke». Order of the Ministry of Health of Ukraine dated 2024 Jun 20, No. 1070]. [Internet]. 2024 [cited 2025 Oct 09]. Ukrainian. Available from: https://moz.gov.ua/uk/decrees/nakaz-moz-ukrayini-vid-20-06-2024-1070-pro-zatverdzhennya-standartu-medichnoyi-dopomogi-ishemichnij-insult
27. Mao L, Jin H, Wang M, Hu Y, Chen S, He Q, et al. Neurologic Manifestations of Hospitalized Patients With Coronavirus Disease 2019 in Wuhan, China. JAMA Neurol. 2020 Jun 1;77(6):683-90. doi: https://doi.org/10.1001/jamaneurol.2020.1127
28. Helms J, Kremer S, Merdji H, Clere-Jehl R, Schenck M, Kummerlen C, et al. Neurologic Features in Severe SARS-CoV-2 Infection. N Engl J Med. 2020 Jun 4;382(23):2268-70. doi: https://doi.org/10.1056/NEJMc2008597
29. Nannoni S, de Groot R, Bell S, Markus HS. Stroke in COVID-19: A systematic review and meta-analysis. Int J Stroke. 2021 Feb;16(2):137-49. doi: https://doi.org/10.1177/1747493020972922
30. Jawad M, Vamos EP, Najim M, Roberts B, Millett C. Impact of armed conflict on cardiovascular disease risk: a systematic review. Heart. 2019 Sep;105(18):1388-94. doi: https://doi.org/10.1136/heartjnl-2018-314459
31. Jawad M, Vamos EP, Najim M, Roberts B, Millett C. Impact of armed conflict on cardiovascular disease risk: a systematic review. Heart. 2019 Sep;105(18):1388-94. doi: https://doi.org/10.1136/heartjnl-2018-314459
32. Okunieva S-MS, Prokopiv MM. [The impact of military events on risk factors for cerebral stroke among residents of Kyiv]. Ukrainian Medical Journal. 2025;1:113-5. Ukr. doi: https://doi.org/10.32471/umj.1680-3051.260598
33. Shkoruta DP, Senkiv V, Vovchuk V, Popadynets O, Kotyk T. Impact of war on stroke incidence in Ivano-Frankivsk, Ukraine. Sci Rep. 2024;14(1):18996. doi: https://doi.org/10.1038/s41598-024-70270-4
Ключові слова: меланоцитарний невус, дерматоскопія, патоморфологія, зворотний невус, рецидив, методи лікування
Key words: melanocytic nevus, dermoscopy, histopathology, recurrent nevus, recurrence, treatment methods
Реферат
Доброякісні меланоцитарні невуси є одними з найпоширеніших новоутворень шкіри та часто потребують діагностичних і лікувальних втручань у практиці лікаря-дерматолога. Незважаючи на широке впровадження дерматоскопії, зберігаються труднощі диференційної діагностики різних клініко-морфологічних форм невусів і вибору оптимальної лікувальної тактики. Неповне видалення пігментних утворень асоціюється з розвитком зворотного (рецидивного) невуса, формуванням рубців і появою діагностично складних пігментних змін, що зумовлює необхідність узагальнення сучасних наукових даних щодо клініко-дерматоскопічних і патоморфологічних кореляцій. Метою дослідження було проаналізувати та обґрунтувати сучасні наукові дані щодо клінічних, дерматоскопічних і патоморфологічних особливостей різних клініко-морфологічних форм доброякісних меланоцитарних невусів шкіри для обґрунтування індивідуалізованого вибору методу лікування, спрямованого на зниження частоти розвитку зворотного невуса, мінімізацію післяопераційних ускладнень і досягнення оптимального косметичного результату. Огляд виконано у форматі наративного аналітичного огляду з елементами систематизованого пошуку відповідно до рекомендацій PRISMA. У роботі застосовано бібліографічний, аналітичний, синтетичний, порівняльний методи, а також методи систематизації та узагальнення даних. Аналіз літератури проведено в базах даних PubMed/MEDLINE та PubMed Central у часовому інтервалі 2009-2025 років. У ході первинного пошуку ідентифіковано 312 публікацій, після виключення дублікатів проаналізовано 268 джерел, за результатами скринінгу назв й анотацій відібрано 97 статей, з яких 54 публікації включено до фінального якісного аналізу. Критеріями включення були оглядові, клінічні та клініко-морфологічні дослідження, а також міжнародні консенсусні рекомендації, що містили дані щодо дерматоскопічних і патоморфологічних характеристик доброякісних меланоцитарних невусів та методів їх лікування. Критеріями виключення були ізольовані клінічні випадки без аналітичного узагальнення, публікації, присвячені виключно меланомі, а також роботи без доступу до повного тексту. Як ключові слова використовували такі: «меланоцитарні невуси», «дерматоскопія», «патоморфологічні кореляції», «рецидивний невус», «методи лікування». За результатами аналізу встановлено, що дерматоскопічні патерни доброякісних меланоцитарних невусів відображають особливості їх патоморфологічної організації та змінюються залежно від віку пацієнта, тривалості існування й анатомічної локалізації утворення. Виявлено тісний зв’язок між дерматоскопічними ознаками та глибиною розташування меланоцитарних компонентів, що має принципове значення для вибору методу лікування. Часткові методи видалення, зокрема shave-ексцизія та аблятивні методики, асоційовані з вищою частотою репігментації та розвитку рецидивного невуса, тоді як повне хірургічне висічення забезпечує найвищу діагностичну безпеку за рахунок можливості первинної гістологічної верифікації, хоча може супроводжуватися більш вираженим рубцюванням. Отримані результати свідчать про доцільність індивідуалізованого підходу до лікування доброякісних меланоцитарних невусів на основі інтеграції клінічних, дерматоскопічних і патоморфологічних даних з метою зниження частоти рецидивів, мінімізації діагностичних труднощів і покращення косметичних результатів.
Abstract
Clinico-dermoscopic and histopathological correlations of benign melanocytic nevi of the skin as a basis for the choice of treatment and recurrence prevention (literature review). Torbenko Ye.L., Litus V.I. Benign melanocytic nevi are among the most common skin lesions and frequently require diagnostic and therapeutic interventions in dermatological practice. Despite the widespread implementation of dermoscopy, difficulties in the differential diagnosis of various clinico-morphological types of nevi and in the selection of optimal treatment strategies persist. Incomplete removal of pigmented lesions is associated with the development of the recurrent nevus phenomenon, scar formation, and diagnostically challenging pigmentation changes, highlighting the need for a comprehensive synthesis of current evidence on clinico-dermoscopic and histopathological correlations. The aim of the study was to analyze and substantiate current scientific data on the clinical, dermatoscopic, and pathomorphological features of various clinical and morphological forms of benign melanocytic skin nevi to justify the individualized choice of treatment method aimed at reducing the frequency of inverse nevus development, minimizing postoperative complications, and achieving optimal cosmetic results. The review was conducted as a narrative analytical with elements of a one structured search in accordance with PRISMA recommendations. Bibliographic, analytical, synthetic, and comparative methods, as well as data systematization and generalization techniques, were applied. The literature search was performed in the PubMed/MEDLINE and PubMed Central databases, covering the period from 2009 to 2025. A total of 312 publications were identified during the initial search. After duplicates removal, 268 records were screened, and 97 articles were selected based on title and abstract evaluation. Following full-text assessment, 54 publications were included in the final qualitative analysis. Inclusion criteria comprised review articles, clinical and clinico-morphological studies, as well as international consensus recommendations that reported data on dermoscopic and histopathological characteristics of benign melanocytic nevi and treatment methods. Exclusion criteria included isolated case reports without analytical synthesis, publications focused exclusively on melanoma, and studies without full-text availability. The keywords used were “melanocytic nevi,” “dermoscopy,” “histopathological correlations,” “recurrent nevus,” and “treatment methods.” The analysis demonstrated that dermoscopic patterns of benign melanocytic nevi reflect their underlying histopathological architecture and vary depending on patient age, lesion duration, and anatomical localization. A strong association was identified between specific dermoscopic features and the depth of melanocytic components, which is of critical importance for treatment selection. Partial removal techniques, including shave excision and ablative procedures, were associated with a higher risk of repigmentation and recurrent nevus development, whereas complete surgical excision provided the highest diagnostic reliability due to the possibility of primary histopathological verification, but it may be accompanied by a more pronounced scarring. The findings support the rationale for an individualized management strategy for benign melanocytic nevi based on the integration of clinical, dermoscopic, and histopathological data, aiming to reduce recurrence rates, minimize diagnostic uncertainty, and improve cosmetic outcomes.
Доброякісні меланоцитарні невуси шкіри є одними з найпоширеніших пігментних новоутворень у загальній популяції та становлять значну частку об’єктів клінічного оцінювання в дерматологічній практиці. За даними епідеміологічних досліджень, понад 80% дорослого населення мають принаймні один меланоцитарний невус, а у 20-30% осіб виявляються множинні утворення, кількість і розподіл яких залежать від віку, фототипу шкіри, генетичних чинників та рівня ультрафіолетового опромінення [1, 2]. Клінічна значущість меланоцитарних невусів виходить за межі їх поширеності, оскільки вони розглядаються як фенотипічний маркер підвищеного ризику розвитку меланоми – однієї з найбільш агресивних злоякісних пухлин шкіри [3].
Згідно з даними Всесвітньої організації охорони здоров’я та Міжнародного агентства з вивчення раку (IARC, GLOBOCAN), захворюваність на меланому шкіри у світі демонструє стійку тенденцію до зростання, особливо в регіонах із переважанням світлого фототипу населення [4]. У країнах Європи стандартизовані показники захворюваності в окремих регіонах перевищують 20-30 випадків на 100 000 населення, що зумовлює підвищену увагу до пігментних утворень як потенційних маркерів онкологічного ризику [5]. Хоча більшість меланом не розвивається безпосередньо з наявних невусів, численні та атипові меланоцитарні утворення розглядаються як незалежні фактори підвищеного ризику, що обґрунтовує необхідність їх ретельного оцінювання та обґрунтованого лікування [6].
В Україні проблема діагностики та лікування пігментних утворень шкіри, зокрема доброякісних меланоцитарних невусів, набуває особливої актуальності у зв’язку з нерівномірним упровадженням дерматоскопічних методів, обмеженим доступом до спеціалізованої допомоги та відсутністю уніфікованих національних рекомендацій щодо вибору методу лікування. За даними вітчизняних авторів, у клінічній практиці досі широко застосовуються деструктивні та часткові методи видалення пігментних утворень, зокрема shave-ексцизія та коагуляційні методики, нерідко без подальшої патоморфологічної верифікації, що підвищує ризик розвитку зворотного невуса та ускладнює подальшу диференційну діагностику пігментних змін у зоні рубця [13, 14]. Окремі українські дослідження також підкреслюють недостатню інтеграцію дерматоскопічних даних з патоморфологічними висновками та значну варіабельність клінічних підходів залежно від спеціальності лікаря й рівня закладу охорони здоров’я [15].
У сучасній дерматології дерматоскопія визнана стандартним неінвазивним методом первинного оцінювання пігментних утворень шкіри, що суттєво підвищує точність диференційної діагностики порівняно з клінічним оглядом неозброєним оком завдяки візуалізації підепідермальних структур і патернів росту [7]. Водночас її діагностична ефективність значною мірою залежить від коректної інтерпретації ознак та розуміння їх патоморфологічних корелятів, що стало підґрунтям для розробки міжнародних консенсусів й уніфікованої дерматоскопічної термінології [8].
Попри прогрес у діагностиці, вибір оптимального методу лікування доброякісних меланоцитарних невусів залишається предметом наукової дискусії. Часткові методи видалення, хоча й привабливі з косметичної точки зору, асоційовані з підвищеним ризиком неповного видалення меланоцитарної тканини та розвитку зворотного (recurrent) невуса [9]. За даними клініко-патологічних досліджень, частота неповних висічень меланоцитарних утворень навіть при первинному намірі радикального втручання може сягати 8-12%, тоді як після часткових методів видалення ризик репігментації та формування зворотного невуса зростає в кілька разів [10]. Відсутність первинної патоморфологічної верифікації після косметичного або часткового видалення суттєво ускладнює подальшу діагностичну тактику та часто зумовлює необхідність повторних або більш агресивних втручань [11, 12].
Таким чином, проблема лікування доброякісних меланоцитарних невусів має міждисциплінарний характер і потребує інтеграції клінічних, дерматоскопічних і патоморфологічних даних. Відсутність уніфікованого підходу до вибору методу лікування зумовлює варіабельність клінічних рішень і неоднозначність результатів, що визначає актуальність систематизації сучасних доказів та формування індивідуалізованої, алгоритмізованої моделі ведення пацієнтів.
Мета дослідження – проаналізувати та обгрунтувати сучасні наукові дані щодо клінічних, дерматоскопічних і патоморфологічних особливостей різних клініко-морфологічних форм доброякісних меланоцитарних невусів шкіри для обґрунтування індивідуалізованого вибору методу лікування, спрямованого на зниження частоти розвитку зворотного невуса, мінімізацію післяопераційних ускладнень і досягнення оптимального косметичного результату.
МАТЕРІАЛИ ТА МЕТОДИ ДОСЛІДЖЕНЬ
Цей огляд виконано у форматі систематизованого огляду літератури з елементами наративного аналізу відповідно до принципів доказової медицини та рекомендацій PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses). Процес відбору джерел відповідав основним етапам рекомендацій PRISMA; формування повноцінної PRISMA-діаграми не здійснювалося у зв’язку з оглядовим характером дослідження та відсутністю кількісного метааналізу.
Методологія дослідження була спрямована на всебічний і відтворюваний пошук, відбір та критичний аналіз наукових джерел, присвячених клінічним, дерматоскопічним і патоморфологічним особливостям доброякісних меланоцитарних невусів шкіри, а також результатам застосування різних методів їх лікування.
Для досягнення поставленої мети в процесі проведення дослідження застосовано такі методи: бібліографічний (систематизований пошук і відбір наукових джерел), аналітичний (критичний аналіз й оцінювання отриманих даних), синтетичний (узагальнення результатів окремих досліджень), порівняльний (зіставлення клінічних, дерматоскопічних і патоморфологічних характеристик, а також результатів різних методів лікування), системно-структурний та формально-логічний методи, а також методи систематизації та узагальнення наукової інформації.
Електронний пошук наукових публікацій здійснювали в міжнародних біомедичних базах даних PubMed/MEDLINE, Google Scholar та Scopus у часовому інтервалі 2009-2025 років. Пошукову стратегію формували з використанням комбінацій ключових слів і MeSH-термінів англійською мовою, зокрема: melanocytic nevi, benign melanocytic nevi, dermoscopy, clinico-dermoscopic correlation, histopathological correlation, recurrent nevus phenomenon, shave excision, surgical excision, treatment outcomes. Пошукові запити комбінувалися за допомогою логічних операторів AND та OR, що дозволяло розширювати або звужувати вибірку відповідно до завдань огляду. Додатково здійснювався ручний перегляд бібліографічних списків ключових оглядових статей, міжнародних консенсусних документів і рекомендацій професійних дерматологічних асоціацій.
Відбір публікацій проводився в кілька етапів. На етапі первинного пошуку ідентифіковано 312 публікацій. Після виключення дублікатів проаналізовано 268 джерел. За результатами скринінгу назв і анотацій відібрано 97 статей, з яких після повнотекстового аналізу 54 публікації включено до фінального якісного огляду відповідно до рекомендацій PRISMA.
Критеріями включення були оглядові та систематичні статті, міжнародні консенсусні рекомендації, клінічні, клініко-дерматоскопічні та клініко-патоморфологічні дослідження, у яких аналізувалися дерматоскопічні ознаки доброякісних меланоцитарних невусів, їх патоморфологічні кореляції та результати різних методів лікування з оцінкою частоти розвитку зворотного невуса і косметичних наслідків. Критеріями виключення були ізольовані клінічні випадки без аналітичного узагальнення, публікації, присвячені виключно злоякісним меланоцитарним новоутворенням без аналізу доброякісних невусів, експериментальні дослідження без клінічної верифікації, а також роботи без доступу до повного тексту або опубліковані в нерецензованих джерелах.
Оцінювання відібраних публікацій здійснювали шляхом якісного критичного аналізу з урахуванням дизайну досліджень, характеристик вибірок, клінічного контексту, застосованих діагностичних методів і терапевтичних підходів. Отримані результати систематизували за тематичними напрямами, що дало змогу провести порівняльний аналіз, виявити узгоджені та суперечливі положення літератури й сформулювати обґрунтовані висновки, релевантні для клінічної практики та подальших наукових досліджень.
Дослідження виконано з дотриманням принципів біоетики, викладених у Гельсінській декларації «Етичні принципи медичних досліджень за участю людей» та «Загальній декларації про біоетику та права людини» (ЮНЕСКО). Проведення дослідження схвалено локальною комісією з питань біоетики (протокол № 9 від 24.12.2025, Національний університет охорони здоров’я України).
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
Доброякісні меланоцитарні невуси шкіри є гетерогенною групою новоутворень, що демонструють значну варіабельність клінічних проявів і морфологічної структури. У фундаментальних роботах, присвячених біології невусів, показано, що їх формування відбувається за принципом послідовної міграції меланоцитів від дермо-епідермального з’єднання (dermo-epidermal junction, DEJ) до дерми з подальшим клітинним дозріванням, що лягло в основу класичної клініко-морфологічної класифікації [24, 25]. Саме ця концепція пояснює існування пограничних, складних і інтрадермальних форм невусів та їх відмінності в клінічній і дерматоскопічній картині.
Клініко-морфологічні форми доброякісних меланоцитарних невусів шкіри та їх клінічне значення
Клініко-морфологічна класифікація доброякісних меланоцитарних невусів є фундаментальною складовою сучасної дерматології, оскільки безпосередньо визначає особливості клінічного перебігу, дерматоскопічної картини та тактику лікування. Сучасні багатоцентрові дослідження та узагальнені огляди підтверджують, що різні морфологічні типи невусів демонструють характерні дерматоскопічні патерни, які корелюють з глибиною та архітектурою меланоцитарних компонентів [24, 25].
Установлено, що дерматоскопічні патерни доброякісних меланоцитарних невусів корелюють з глибиною та архітектурою меланоцитарного компонента, що має принципове значення для прогнозування ризику неповного видалення та вибору методу лікування (рис. 1).
Пігментна сітка відповідає поверхневому (пограничному) розташуванню меланоцитів на рівні дермо-епідермального з’єднання; глобулярні та безструктурні патерни корелюють з інтрадермальним компонентом; гетерогенні патерни характерні для комбінованих форм невусів. Схему розроблено авторами на основі узагальнення даних літератури [11, 12, 25]
За даними систематизованого аналізу дерматоскопічних патернів, пограничні меланоцитарні невуси частіше виявляються в молодих пацієнтів і зазвичай характеризуються регулярною пігментною сіткою та симетричною архітектурою [21]. Водночас сучасні дослідження свідчать, що в 15-25% таких утворень можуть бути наявні дерматоскопічні ознаки атипії, зокрема фокальна асиметрія або варіабельність товщини сітки, що істотно ускладнює їх диференціацію з ранніми формами меланоми, особливо за відсутності динамічного дерматоскопічного спостереження [22].
Комбіновані (складні) меланоцитарні невуси, за даними сучасних оглядів, демонструють значно більшу дерматоскопічну гетерогенність. У таких утвореннях часто поєднуються мереживні, глобулярні та безструктурні елементи, що відображає наявність меланоцитарних компонентів як на рівні дермо-епідермального з’єднання, так і в дермі [25, 33]. Саме ця морфологічна та дерматоскопічна неоднорідність зумовлює підвищену варіабельність діагностики і різні клінічні рішення лікарів щодо тактики ведення, зокрема у випадках косметичного видалення [24].
Інтрадермальні невуси залишаються найбільш поширеною клініко-морфологічною формою в дорослій популяції. За даними сучасних клінічних серій, вони становлять до 50-60% усіх меланоцитарних невусів, що підлягають видаленню в дерматологічній практиці [13]. Дерматоскопічно ці утворення переважно представлені глобулярними або однорідними безструктурними патернами з мінімальною архітектурною атипією, що загалом відповідає їх доброякісному морфологічному перебігу. Водночас саме інтрадермальні та комбіновані невуси найчастіше піддаються частковому видаленню з косметичною метою, що має суттєві клінічні наслідки [13, 30].
Окрему клінічну та прогностичну проблему становлять диспластичні (атипові) меланоцитарні невуси. Згідно із сучасними систематичними оглядами та метааналізами, наявність множинних диспластичних невусів асоціюється зі статистично значущим підвищенням ризику розвитку меланоми, однак абсолютний ризик трансформації окремого невуса залишається низьким [19, 20]. Саме диспластичні невуси найчастіше створюють складні діагностичні ситуації та є причиною як надмірних хірургічних втручань, так і недостатнього клінічного контролю.
Клініко-морфологічна форма невуса має безпосередній вплив не лише на діагностику, а й на результати лікування. За даними сучасних досліджень, ризик неповного видалення та розвитку зворотного невуса є статистично значуще вищим при поверхневих і комбінованих формах у разі застосування часткових методів, зокрема shave-ексцизії, порівняно з повним хірургічним висіченням [6, 13, 26]. Частота репігментації в зоні рубця в таких випадках може досягати 20-30%, що підтверджує необхідність урахування морфологічної структури утворення при виборі методу лікування [26].
Таким чином, дані сучасних досліджень переконливо свідчать, що клініко-морфологічна класифікація меланоцитарних невусів має не лише описовий, а й прогностичний характер. Вона визначає особливості дерматоскопічної картини, ризик діагностичних помилок і ймовірність розвитку зворотного невуса після лікування. Інтеграція морфологічних уявлень із сучасними дерматоскопічними критеріями є ключовою передумовою персоналізованого вибору тактики ведення пацієнтів з доброякісними меланоцитарними невусами шкіри [24, 30].
Узагальнення клініко-дерматоскопічних і патоморфологічних характеристик основних форм меланоцитарних невусів та їх значення для вибору методу лікування наведено в таблиці 1.
Клініко-морфологічна форма Типовий дерматоскопічний патерн Морфологічний субстрат Рекомендований метод лікування Ризик рецидиву Пограничний невус Регулярна пігментна сітка Меланоцити в DEJ Повне висічення Низький Комбінований невус Гетерогенний (сітка + глобули) DEJ + дерма Повне висічення Середній Інтрадермальний невус Глобулярний/ безструктурний Дермальний компонент Shave (обмежено)/ висічення Підвищений при shave Диспластичний невус Асиметрія, атипія Архітектурна атипія Висічення з гістологією Вищий
при сумнівах
У вітчизняному контексті проблема ведення пігментних утворень шкіри має додаткові детермінанти, пов’язані з нерівномірною доступністю дерматоскопії, відсутністю уніфікованих національних алгоритмів тактики та зростанням навантаження на систему охорони здоров’я в умовах воєнного часу. Українські автори підкреслюють актуальність дерматоонкологічних захворювань і потребу в організаційно-діагностичних рішеннях для зменшення частоти пізньої верифікації та тактичних помилок, що безпосередньо стосується і «сірої зони» пігментних утворень, де косметичні втручання нерідко виконуються без морфологічного підтвердження [49, 50].
Окремим практичним наслідком є підвищення частоти ситуацій, коли репігментація в рубці після часткового видалення потребує повторної діагностичної тактики (до повного висічення), оскільки первинної гістологічної верифікації не було [49]. У цьому аспекті українські оглядові роботи з біопсії шкіри наголошують на ключовій ролі морфологічного підтвердження в дерматоонкології, що має бути враховано при виборі методу видалення меланоцитарних утворень, особливо за наявності атипових ознак [51, 53, 54].
Додатково, українські хірургічні публікації, присвячені пігментним пухлинам у дитячій популяції, акцентують на необхідності методик, які забезпечують мінімізацію рецидивів і діагностичну визначеність, що логічно підтримує концепцію обґрунтованого вибору між косметичними частковими методами та повним висіченням з контролем країв/морфологічною верифікацією [51, 52].
Дерматоскопічні патерни доброякісних меланоцитарних невусів та їх патоморфологічні кореляції
Дерматоскопія суттєво розширила можливості неінвазивної диференційної діагностики пігментних утворень завдяки візуалізації структур, які мають морфологічний субстрат. Проте практична цінність дерматоскопії прямо залежить від уніфікованої мови опису. У межах третьої консенсус-конференції International Society of Dermoscopy (IDS) запропоновано стандартизовану рамку термінів (аналітичних/описових і метафоричних), а також продемонстровано, що серед учасників 23,5% переважно використовують описову термінологію, 20,1% – метафоричну, а 56,5% комбінують обидві; водночас значна частина нових термінів залишалася маловідомою для більшості респондентів [31]. Це підкреслює методологічну проблему: без стандартизації термінів зростає варіабельність діагностики, а отже – ризик різних клінічних рішень щодо того самого невуса.
З позицій доказовості, алгоритмізація дерматоскопічного оцінювання дозволила кількісно оцінювати діагностичну ефективність. Класичний приклад – ABCD-правило дерматоскопії, перспективно протестоване на 172 меланоцитарних пігментних утвореннях: за порогового значення Total Dermoscopic Score >5,45 як злоякісні класифікувалися 64/69 меланом (92,8%), тоді як серед утворень з нижчим балом як доброякісні класифікувалися 93/103 невуси (90,3%) [32]. Отже, навіть ранні алгоритми демонстрували високу інформативність в сумнівних клінічних ситуаціях, але їх обмеженням залишалася залежність від коректного визначення структури та кольорів і, відповідно, від навченості лікаря.
Подальший розвиток отримали чек-листки, які поєднують структурний аналіз із сумарною оцінкою ознак. У класичному порівняльному дослідженні Argenziano et al. 7-пунктовий чек-листок продемонстрував чутливість 95% і специфічність 75%, тоді як ABCD-правило 85% і 66% відповідно (у загальному порівнянні методик на навчальній/тестовій вибірках), що дало підстави розглядати 7-пунктовий підхід як більш чутливий інструмент для виявлення меланоми в сумнівних випадках [33]. Важливо, що автори також показали різницю між підходами залежно від досвіду лікаря, що напряму пов’язує результати дерматоскопії з питанням стандартизації навчання та інтерпретації.
Надалі ці алгоритми були переоцінені в умовах сучасної клініки, коли лікар частіше бачить ранні меланоми та множинні атипові невуси, а не лише «класичні» форми. У дослідженні «Seven-point checklist revisited» (8 експертів; набори: 100 висічених меланом, 100 висічених невусів, 100 невусів під спостереженням) показано, що за pattern analysis 82% меланом були правильно оцінені як такі, що підлягають висіченню, а 87,5% моніторованих невусів як доброякісні [34]. Для 7-пунктового чек-листка перехід до зниженого порогу (revised threshold) підвищував частку рекомендацій щодо висічення в групі меланом із 77,9% до 87,8%, але зменшував частку рекомендацій «не висікати» у групі моніторингу з 85,6% до 74,5% [34]. Ці цифри добре ілюструють принципову дилему: підвищення чутливості в реальній практиці часто супроводжується «ціною» у вигляді більшої кількості втручань у доброякісних випадках, що особливо важливо при плануванні тактики для невусів з урахуванням косметичних очікувань пацієнта.
Окреме практичне значення має 2-кроковий підхід, де першим завданням є класифікація утворення як меланоцитарного або немеланоцитарного. У дослідженні Tschandl et al. (707 послідовних випадків) чутливість першого кроку становила 97,1% в пацієнтів з Австралії та 96,8% в пацієнтів з Центральної Європи, однак специфічність була низькою й різнилася між популяціями (33,6% та 67,9% відповідно) [35]. Автори деталізували причини помилок: зокрема, пігментна сітка в немеланоцитарних ураженнях була причиною помилкової класифікації в 68 випадках (25,2%), а відсутність характерних дерматоскопічних ознак – у 69 випадках (25,6%) немеланоцитарних утворень [35]. Для клінічної практики це означає, що високочутливий скринінговий перший крок може навмисно «перестраховуватися», але без другого кроку (оцінки патернів/ознаки атипії) він не забезпечує достатньої точності рішень щодо лікування.
Ключовим підґрунтям для побудови дерматоскопічних критеріїв лікувальної тактики є саме клініко-дерматоскопічно-патоморфологічні кореляції. У роботі Woltsche et al. запропоновано узагальнений погляд на доброякісні невуси, які підкреслюють, що дерматоскопічні патерни відображають конкретні гістологічні субстрати, формуючи міст між клінічною оцінкою та морфологічною верифікацією [36]. У практичному сенсі це підтримує концепцію, що вибір методу видалення (повне висічення з верифікацією країв vs часткові косметичні методи) має ґрунтуватися не лише на зовнішньому вигляді, а й на прогнозованій глибині/архітектурі меланоцитарного компонента, яку частково можна оцінити через патерн-аналіз та узгоджені дерматоскопічні критерії [31, 36].
Дерматоскопічні ознаки, що визначають вибір методу лікування та ризик розвитку зворотного невуса
Одним з ключових практичних завдань сучасної дерматології є трансляція дерматоскопічних даних в обґрунтоване клінічне рішення щодо вибору методу лікування меланоцитарного невуса. На відміну від діагностичних алгоритмів, спрямованих передусім на виявлення меланоми, лікувальна тактика потребує оцінювання не лише ступеня дерматоскопічної атипії, а й прогнозованої морфологічної структури утворення, глибини залягання меланоцитарного компонента та ризику його неповного видалення.
Сучасні дослідження підтверджують, що певні дерматоскопічні патерни мають тісний зв’язок з гістологічною архітектурою невусів. Регулярна пігментна сітка частіше корелює з поверхневим (пограничним) розташуванням меланоцитів, тоді як глобулярні та однорідні безструктурні патерни асоціюються з інтрадермальними або комбінованими формами [21, 25]. З клінічної точки зору це має принципове значення, оскільки поверхневі та комбіновані утворення при застосуванні часткових методів видалення частіше залишають резидуальну меланоцитарну тканину, що створює умови для розвитку зворотного (recurrent) невуса [6, 13].
За даними сучасних клінічних серій і ретроспективних аналізів, частота репігментації в зоні рубця після shave-ексцизії меланоцитарних невусів коливається в межах 20-30% залежно від морфологічного типу утворення та анатомічної локалізації, тоді як після повного хірургічного висічення цей показник є статистично значуще нижчим [13, 26]. В інших дослідженнях також показано, що поєднання поверхневого дерматоскопічного патерна з косметичними методами видалення є одним з найважливіших предикторів розвитку зворотного невуса та повторних втручань [6, 11].
Особливої клінічної уваги потребує дерматоскопічна оцінка рубцевих змін після попередніх втручань. Сучасні дослідження демонструють, що репігментація в межах рубця після неповного видалення невуса може мати асиметричний характер і включати безструктурні зони, сіро-коричневі ділянки або нерівномірні глобули, що морфологічно відповідає залишковій або реактивній меланоцитарній проліферації [8, 9]. Водночас ключовим диференційно-діагностичним критерієм між зворотним невусом і рецидивом меланоми вважається поширення пігментації за межі рубця, що підтверджено як дерматоскопічними, так і гістологічними даними [9, 26].
У дослідженнях, присвячених аналізу діагностичних помилок, показано, що відсутність первинного гістологічного висновку після косметичного або часткового видалення істотно підвищує діагностичну невизначеність при появі пігментації в рубці. У таких клінічних ситуаціях більшість сучасних рекомендацій розглядають повне хірургічне висічення як метод вибору незалежно від початкової дерматоскопічної оцінки [6, 14, 26]. Це підкреслює важливий практичний аспект: дерматоскопічні ознаки не можуть інтерпретуватися ізольовано від анамнестичних і морфологічних даних, а первинний вибір методу лікування має довготривалі діагностичні наслідки.
Косметичний аспект лікування меланоцитарних невусів, хоча й не є первинним з онкологічної точки зору, суттєво впливає на клінічні рішення. Порівняльні сучасні дослідження свідчать, що shave-ексцизія асоціюється з менш вираженим первинним рубцем і швидшим загоєнням, однак ці переваги часто нівелюються в разі розвитку рецидиву, який потребує повторного, більш радикального та травматичного втручання [13]. Таким чином, короткостроковий косметичний виграш може трансформуватися в гірший довгостроковий клінічний та естетичний результат.
Порівняльні характеристики основних методів видалення меланоцитарних невусів з урахуванням ризику рецидиву та косметичних результатів узагальнено в таблиці 2.
Системний аналіз літератури також демонструє, що ризик неповного видалення та рецидиву залежить не лише від вибраного методу, а й від анатомічної локалізації утворення. У ділянці голови та шиї, а також на тулубі частота маргінальних або неповних резекцій є вищою, що пов’язано як з анатомічними особливостями, так і з прагненням мінімізувати косметичний дефект [6, 11]. Це додатково підкреслює необхідність індивідуалізованого підходу до вибору методу лікування з урахуванням дерматоскопічних, клінічних і морфологічних характеристик невуса.
Метод Переваги Недоліки Частота рецидиву Косметичний результат Shave-ексцизія Швидко, мінімальний рубець Неповне видалення 10-30% Короткостроково кращий Еліптичне висічення Повнота, гістологія Рубець <5% Довгостроково стабільний Лазер Косметика Без гістології Невідомо Варіабельний
Узагальнюючи наведені дані, можна стверджувати, що дерматоскопія відіграє ключову роль не лише в диференційній діагностиці доброякісних меланоцитарних невусів, а й у стратифікації ризику їх неповного видалення та розвитку зворотного невуса. Проте її ефективність як інструменту вибору лікувальної тактики реалізується лише за умови інтеграції з клінічними параметрами, морфологічними уявленнями та чітким усвідомленням обмежень часткових методів втручання. Саме такий інтегрований підхід розглядається в сучасній літературі як основа персоналізованого ведення пацієнтів з доброякісними меланоцитарними невусами шкіри [21, 36].
Перспективи індивідуалізованого підходу до лікування доброякісних меланоцитарних невусів шкіри
Актуальність удосконалення підходів до ведення меланоцитарних невусів посилюється глобальними онкоепідеміологічними трендами. За оцінками Всесвітньої організації охорони здоров’я, надмірна експозиція ультрафіолетового випромінювання у 2020 році була асоційована приблизно з 325 000 випадків меланоми шкіри та 57 000 смертей у світі [3]. Додатково, за даними Міжнародного агентства з вивчення раку (IARC), у 2022 році у світі було зареєстровано близько 331 700 нових випадків і 58 700 смертей від меланоми, причому понад 80% випадків були атрибутовані ультрафіолетовому опроміненню (267 тис. із 332 тис.) [4]. Хоча меланома не є безпосереднім об’єктом цього огляду, ці дані формують важливий контекст: точна оцінка пігментних утворень й обґрунтований вибір тактики щодо меланоцитарних невусів є складовою ширшої системи раннього виявлення та профілактики злоякісних новоутворень шкіри. Прогностичні розрахунки свідчать про суттєве зростання глобального тягаря меланоми в найближчі десятиліття. Очікується, що до 2040 року кількість уперше виявлених випадків цього захворювання може перевищити півмільйона, що відповідає приросту більше ніж на 50% порівняно з показниками 2020 року. Паралельно прогнозується істотне збільшення летальності: орієнтовна кількість смертей від меланоми може зрости майже на дві третини з приблизно 57 тис. у 2020 році до близько 96 тис. у 2040 році, за умови відсутності змін у поточних вікових показниках ризику. Важливо зазначити, що наведені прогнози базуються виключно на демографічних чинниках, зокрема зростанні чисельності населення та його старінні, і не враховують можливих змін у віковоспецифічній захворюваності на рівні окремих країн або регіонів. За таких умов лише стійке глобальне зниження показників захворюваності та смертності більше ніж на 2% могло б запобігти абсолютному зростанню кількості випадків меланоми у 2040 році (рис. 2) [1].
Незважаючи на стандартизацію дерматоскопічної «мови», реальна клінічна практика демонструє суттєву варіабельність у використанні термінології та існування різних «шкіл» опису. У консенсусі International Society of Dermoscopy щодо стандартизації термінології показано, що 23,5% фахівців переважно використовують описову термінологію, 20,1% – метафоричну, тоді як 56,5% комбінують обидві; при цьому значна частина нових термінів після попереднього консенсусу залишалася маловідомою для більшості учасників [31]. Це має прямі практичні наслідки: різне «кодування» однакових дерматоскопічних структур може призводити до різної оцінки ризику та, відповідно, до різних клінічних рішень щодо спостереження або вибору методу видалення.
З позицій доказової медицини дерматоскопія, порівняно з оглядом неозброєним оком, демонструє значно вищу діагностичну інформативність у клінічних умовах. У метааналізі Vestergaard et al. відносне діагностичне відношення шансів для виявлення меланоми при використанні дерматоскопії становило 15,6 (95% ДІ 2,9-83,7), а після корекції на викиди – 9,0 (95% ДІ 1,5-54,6) [32]. Для теми цього огляду принципово важливо, що ця перевага стосується саме підозрілих утворень тієї зони клінічної невизначеності, де виникає найбільше тактичних помилок при веденні меланоцитарних невусів.
Водночас ключова прогалина полягає в тому, що більшість дерматоскопічних алгоритмів розроблялися для виявлення меланоми, а не для прогнозування ризику неповного видалення або рецидиву доброякісних невусів. Навіть перший крок двокрокового алгоритму – класифікація «меланоцитарне/немеланоцитарне» – характеризується дуже високою чутливістю (97,1% в Австралії та 96,8% в Центральній Європі), але демонструє істотну варіабельність специфічності (33,6% і 67,9 % відповідно) [35]. Аналіз структури помилок показав, що наявність пігментної сітки в немеланоцитарних ураженнях зумовлювала хибну класифікацію у 25,2% випадків, а відсутність характерних ознак – у 25,6 % [35]. Це свідчить про те, що навіть високочутливий інструмент первинної ідентифікації не гарантує оптимального вибору лікувальної тактики без інтеграції з прогнозуванням морфологічної структури утворення.
Найбільш значущою практичною проблемою залишається неповне видалення меланоцитарних утворень і пов’язані з цим рецидиви або феномен зворотного невуса. У великому дослідженні Berglund et al. (2782 послідовні висічення) 9,7% меланоцитарних уражень були видалені неповно; серед факторів ризику виділялися локалізація в ділянці голови та шиї, а також організаційні й технічні чинники [6]. Це підтверджує системний характер проблеми: навіть за наміру радикального лікування в реальній практиці зберігається суттєва частка маргінальних резекцій, що створює передумови для рецидивів і повторних втручань.
Водночас частота клінічно помітного повернення невуса після часткового видалення може бути відносно низькою, але стабільно асоціюється саме з технікою shave. У дослідженні Goodson et al. рецидив був зафіксований у 3,6% диспластичних і 3,3% звичайних невусів, причому статистично значуща асоціація спостерігалася саме з shave-технікою, а не зі ступенем дисплазії чи позитивними краями резекції [33].
Порівняльні дослідження методів видалення також демонструють різницю не лише в косметичних результатах, а й у частоті рецидивів. У роботі Camini et al. рецидиви (11,7%) виникали виключно після shave-ексцизії, причому в 94,1% випадків уже на 3-місячному контролі; при цьому shave-метод асоціювався з частішим залученням латеральних і глибоких країв, тоді як еліптичне висічення формувало більші рубці [13].
Окрему групу доказів становлять дані щодо ведення диспластичних невусів з позитивними краями. У дослідженні Fleming et al. частота рецидиву в групі спостереження становила 3,3%, тоді як у групі реексцизії 0% при середній тривалості спостереження 5,5 року (p=0,02) [34]. Це підкреслює, що навіть відносно невелика частка рецидивів має накопичувальний клінічний ефект, оскільки кожна репігментація в рубці перетворюється на діагностичну подію з потенційною потребою повторного втручання.
У сукупності наведені дані свідчать, що ключова прогалина сучасної практики полягає не у відсутності дерматоскопічних алгоритмів як таких, а в нестачі валідованих дерматоскопічних критеріїв лікувального вибору, які б інтегрували прогнозовану морфологію і глибину невуса, анатомічну локалізацію, техніку видалення та ризик рецидиву або формування рубця в єдину практичну модель [6, 13, 31, 35]. Саме розробка й впровадження таких критеріїв дозволяє перейти від емпіричної тактики до прогнозованого, відтворюваного та персоналізованого підходу, що мінімізує повторні втручання та забезпечує оптимальний косметичний результат.
Доброякісні меланоцитарні невуси шкіри є біологічно та морфологічно гетерогенною групою новоутворень, що відображається в значній варіабельності їх клінічних проявів, дерматоскопічних патернів і результатів лікування. Отримані в ході цього огляду результати підтверджують положення класичної концепції поетапної міграції меланоцитів від дермо-епідермального з’єднання до дерми з подальшим клітинним дозріванням, яка лежить в основі поділу невусів на пограничні, комбіновані та інтрадермальні форми (Yélamos et al., 2019) [9], (Wang et al., 2022) [28].
Аналіз сучасних публікацій свідчить, що дерматоскопічні патерни мають чіткий морфологічний субстрат. Регулярна пігментна сітка найчастіше корелює з поверхневим розташуванням меланоцитарних гнізд у межах дермо-епідермального з’єднання, тоді як глобулярні та однорідні безструктурні патерни відповідають дермальному компоненту невуса (Errichetti, Stinco, 2016) [27], (Zalaudek et al., 2019) [32]. Ці спостереження узгоджуються з результатами порівняльних досліджень дерматоскопії та високочастотного ультразвуку, де було продемонстровано, що глибина залягання меланоцитарного компонента може бути частково прогнозована за допомогою дерматоскопічного аналізу (Wang et al., 2022) [28].
Практичне значення зазначених кореляцій полягає в можливості прогнозування ризику неповного видалення невуса при застосуванні часткових методів лікування. У клінічній практиці shave-ексцизія та інші косметичні методики широко використовуються з огляду на кращу короткострокову переносимість і менш виражене первинне рубцювання. Водночас результати порівняльних досліджень переконливо демонструють, що саме ці методи асоційовані з вищою частотою репігментації та розвитку феномену зворотного невуса (Camini et al., 2021) [19]. Аналогічні висновки отримали Goodson et al. (2010) [20], які показали, що клінічні рецидиви частіше виникають після shave-біопсії незалежно від ступеня дисплазії невуса.
Системний характер проблеми неповного видалення меланоцитарних утворень підтверджено у великому клініко-патологічному дослідженні Berglund et al. (2021) [6], де частота маргінальних або неповних резекцій становила близько 10% навіть за умови первинного наміру радикального втручання. Основними факторами ризику були анатомічна локалізація (ділянка голови та шиї) та технічні обмеження, пов’язані з прагненням мінімізувати косметичний дефект. Ці дані узгоджуються з результатами Rasner et al. (2023) [32], які описали розвиток зворотного невуса навіть у складних рубцевих структурах, що підкреслює важливість первинного вибору методу лікування.
Окремої уваги заслуговує проблема диференціації зворотного невуса та рецидиву меланоми в зоні рубця. За даними Heck et al. (2019) [8], дерматоскопічні ознаки репігментації після неповного видалення можуть включати асиметрію, нерівномірні глобули та сіро-коричневі безструктурні зони, що морфологічно відповідає залишковій або реактивній меланоцитарній проліферації. Navarrete-Dechent et al. (2020) [18] додатково продемонстрували, що вирішальним диференційно-діагностичним критерієм між зворотним невусом і рецидивом меланоми є поширення пігментації за межі рубця, тоді як ізольована репігментація в його межах частіше має доброякісний характер.
Водночас дані щодо ведення диспластичних невусів з позитивними краями резекції залишаються неоднозначними. Fleming et al. (2016) [21] та Engeln et al. (2017) [22] повідомляють про відносно низьку частоту клінічних рецидивів у разі динамічного спостереження без негайної реексцизії. Водночас Fleming et al. (2020) [23] показали, що повторне хірургічне висічення практично повністю усуває ризик рецидиву, що має особливе значення в умовах діагностичної невизначеності або за відсутності повного первинного гістологічного висновку. Розбіжності між результатами досліджень можуть бути зумовлені різними критеріями відбору пацієнтів, тривалістю спостереження та методологічними підходами до оцінювання рецидивів.
З позицій доказової медицини дерматоскопія демонструє суттєву перевагу порівняно з оглядом неозброєним оком у діагностиці меланоцитарних утворень. Метааналізи підтверджують її високу чутливість і специфічність у клінічних умовах (Vestergaard et al., 2008) [16], (Dinnes et al., 2018) [17]. Проте більшість дерматоскопічних алгоритмів, зокрема ABCD-правило, 7-пунктовий чек-листок та двоетапний підхід, були розроблені передусім для виявлення меланоми, а не для прогнозування ризику неповного видалення доброякісних невусів (Kittler et al., 2016) [40], (Tschandl et al., 2019) [33].
Таким чином, отримані результати та дані сучасної літератури свідчать, що ефективне ведення пацієнтів з доброякісними меланоцитарними невусами потребує переходу від емпіричного вибору методу лікування до алгоритмізованої, індивідуалізованої моделі. Така модель повинна інтегрувати клінічні характеристики, дерматоскопічні патерни, прогнозовану морфологічну структуру невуса, анатомічну локалізацію та анамнестичні дані. Саме комплексний підхід дозволяє знизити ризик розвитку зворотного невуса, мінімізувати діагностичні помилки та досягти оптимального довгострокового косметичного результату.
ВИСНОВКИ
1. Аналіз сучасної літератури свідчить, що доброякісні меланоцитарні невуси шкіри є надзвичайно поширеною патологією, а їх клінічне значення виходить за межі суто косметичної проблеми. З огляду на глобальні епідеміологічні тенденції меланоми та доведену роль ультрафіолетового опромінення, підвищення точності діагностики пігментних утворень й обґрунтованості лікувальної тактики щодо невусів має важливе профілактичне значення.
2. Дерматоскопія є високоефективним неінвазивним методом оцінювання меланоцитарних утворень, що достовірно перевершує огляд неозброєним оком за діагностичною інформативністю. Водночас більшість наявних дерматоскопічних алгоритмів і чек-листків розроблені переважно для виявлення меланоми та недостатньо адаптовані для прогнозування морфологічної структури доброякісних невусів і вибору оптимального методу їх лікування.
3. Дані клінічних і патоморфологічних досліджень переконливо демонструють, що ризик неповного видалення меланоцитарних утворень залишається суттєвим і може досягати близько 10% навіть у сучасній клінічній практиці, особливо при локалізації в ділянці голови та шиї. Часткові методи видалення, зокрема shave-ексцизія, асоціюються з вищою частотою репігментації та розвитку зворотного невуса, що в різних дослідженнях коливається від 3% до понад 20% залежно від морфологічного типу утворення, локалізації та термінів спостереження.
4. Зворотний (recurrent) невус становить не лише косметичну, а й серйозну діагностичну проблему, оскільки його клінічні та дерматоскопічні прояви можуть імітувати рецидив меланоми. Найбільш значущими диференційними ознаками визнано обмеження пігментації межами рубця, час появи репігментації та облік віку пацієнта і первинної гістологічної верифікації, відсутність якої суттєво ускладнює подальше клінічне рішення.
5. Наявні дані свідчать, що клініко-морфологічна форма невуса, його дерматоскопічний патерн, анатомічна локалізація та обраний метод лікування перебувають у тісному взаємозв’язку та визначають як ризик рецидиву, так і довгостроковий косметичний результат. Ігнорування морфологічного контексту при виборі методу втручання підвищує ймовірність повторних процедур і формування косметично несприятливих рубців.
6. Таким чином, сучасний стан проблеми свідчить про необхідність переходу від емпіричного та уніфікованого підходу до лікування меланоцитарних невусів до індивідуалізованої моделі, заснованої на інтеграції клінічних, дерматоскопічних і патоморфологічних даних. Розробка та впровадження валідованих дерматоскопічних критеріїв диференційної діагностики й вибору методу лікування має потенціал знизити частоту зворотного невуса, мінімізувати післяопераційні ускладнення та забезпечити прогнозований косметичний результат, що визначає перспективність подальших досліджень у цьому напрямку.
Внески авторів:
Торбенко Є.Л. – концептуалізація, дослідження, написання – початковий проєкт, написання – рецензування та редагування;
Літус В.І. – методологія, дослідження, написання – початковий проєкт, написання – рецензування та редагування, дослідження, формальний аналіз.
Фінансування. Роботу виконано за рахунок власних коштів дослідників, а також за підтримки наукової діяльності здобувачів Національного університету охорони здоров’я України ім. П.Л. Шупика.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів.
REFERENCES
1. Arnold M, Singh D, Laversanne M, Vignat J, Vaccarella S, Meheus F, et al. Global burden of cutaneous melanoma in 2020 and projections to 2040. JAMA Dermatol. 2022;158(5):495-503. doi: https://doi.org/10.1001/jamadermatol.2022.0160
2. Whiteman DC, Green AC, Olsen CM. The growing burden of invasive melanoma: projections of incidence rates and numbers of new cases in six susceptible populations to 2031. J Invest Dermatol. 2016;136(6):1161-71. doi: https://doi.org/10.1016/j.jid.2016.01.035
3. International Agency for Research on Cancer (IARC). Global Cancer Observatory: Melanoma of skin [Internet]. Lyon: IARC; 2022 [cited 2025 Dec 15]. Available from: https://gco.iarc.fr/
4. World Health Organization. Ultraviolet radiation [Internet]. Geneva: WHO; 2020 [cited 2025 Dec 15]. Available from:
https://www.who.int/health-topics/ultraviolet-radiation
5. WHO Classification of Tumours Editorial Board. Skin Tumours. WHO Classification of Tumours [Internet]. 5th ed. Vol 12. Lyon: IARC; 2025 [cited 2025 Dec 15]. Available from: https://publications.iarc.who.int/Book-And-Report-Series/Who-Classification-Of-Tumours/Skin-Tumours-2025
6. Berglund S, Johansson Backman E, Baldawi Z, Horn L, Arbin Borsiin R, Marjanovic M, et al. Incomplete excisions of melanocytic lesions: rates and risk factors. Acta Derm Venereol. 2021;101(3):adv00421. doi: https://doi.org/10.2340/00015555-3784
7. Castagna RD, Stramari JM, Chemello RML. The recurrent nevus phenomenon. An Bras Dermatol. 2017;92(4):531-3.
doi: https://doi.org/10.1590/abd1806-4841.20176190
8. Heck R, Ferrari T, Cartell A, Bakos RM. Clinical and dermoscopic (in vivo and ex vivo) predictors of recurrent nevi. Eur J Dermatol. 2019;29(2):179-84. doi: https://doi.org/10.1684/ejd.2019.3530
9. Yélamos O, Braun RP, Liopyris K, Wolner ZJ, Kerl K, Gerami P, et al. Dermoscopy and dermatopathology correlates of cutaneous neoplasms. J Am Acad Dermatol. 2019;80(2):341-63. doi: https://doi.org/10.1016/j.jaad.2018.07.073
10. Kittler H, Marghoob AA, Argenziano G, Carrera C, Curiel-Lewandrowski C, Hofmann-Wellenhof R, et al. Standardization of terminology in dermoscopy/ dermatoscopy: results of the third consensus conference of the International Society of Dermoscopy. J Am Acad Dermatol. 2016;74(6):1093-106. doi: https://doi.org/10.1016/j.jaad.2015.12.038
11. Nachbar F, Stolz W, Merkle T, Cognetta AB, Vogt T, Landthaler M, et al. The ABCD rule of dermatoscopy: high prospective value in the diagnosis of doubtful melanocytic skin lesions. J Am Acad Dermatol. 1994;30(4):551-9.
doi: https://doi.org/10.1016/S0190-9622(94)70061-3
12. Annessi G, Bono R, Sampogna F, Faraggiana T, Abeni D. Sensitivity, specificity, and diagnostic accuracy of three dermoscopic algorithmic methods in the diagnosis of doubtful melanocytic lesions. J Am Acad Dermatol. 2007;56(5):759-67. doi: https://doi.org/10.1016/j.jaad.2007.01.035
13. Argenziano G, Fabbrocini G, Carli P, De Giorgi V, Sammarco E, Delfino M. Epiluminescence microscopy for the diagnosis of doubtful melanocytic skin lesions: comparison of the ABCD rule of dermatoscopy and a new 7-point checklist. Br J Dermatol. 1998;139(6):1113-9. doi: https://doi.org/10.1046/j.1365-2133.1998.02506.x
14. Argenziano G, Zalaudek I, Corona R, Sera F, Cicale L, Petrillo G, et al. Seven-point checklist of dermoscopy revisited. Br J Dermatol. 2011;164(4):785-90. doi: https://doi.org/10.1111/j.1365-2133.2010.10194.x
15. Soyer HP, Argenziano G, Chimenti S, Ruocco V. Three-point checklist of dermoscopy: a new screening method for early detection of melanoma. Dermatology. 2004;208(1):27-31. doi: https://doi.org/10.1159/000075042
16. Vestergaard ME, Macaskill P, Holt PE, Menzies SW. Dermoscopy compared with naked eye examination for the diagnosis of primary melanoma: a meta-analysis of studies performed in a clinical setting. Br J Dermatol. 2008;159(3):669-76. doi: https://doi.org/10.1111/j.1365-2133.2008.08713.x
17. Dinnes J, Deeks JJ, Chuchu N, Ferrante di Ruffano L, Matin RN, Thomson DR, et al. Dermoscopy, with and without visual inspection, for diagnosing melanoma in adults. Cochrane Database Syst Rev. 2018;12(12):CD011902. doi: https://doi.org/10.1002/14651858.CD011902.pub2
18. Navarrete-Dechent C, Cordova M, Liopyris K, Rishpon A, Aleissa S, Rossi AM, et al. Reflectance confocal microscopy and dermoscopy aid in evaluating repigmentation within or adjacent to lentigo maligna melanoma surgical scars. J Eur Acad Dermatol Venereol. 2020;34(1):74-81. doi: https://doi.org/10.1111/jdv.15819
19. Camini L, Manzoni APD, Weber MB, Luzzatto L, Soares AS, Bonamigo RR. Shave excision versus elliptical excision of nonpigmented intradermal melanocytic nevi: comparative assessment of recurrence and cosmetic outcomes. Dermatol Surg. 2021;47(2):e21-e25. doi: https://doi.org/10.1097/DSS.0000000000002666
20. Goodson AG, Florell SR, Boucher KM, Grossman D. Low rates of clinical recurrence following biopsy of benign to moderately atypical dysplastic melanocytic nevi. J Am Acad Dermatol. 2010;62(4):591-6. doi: https://doi.org/10.1016/j.jaad.2009.06.044
21. Fleming NH, Egbert BM, Kim J, Swetter SM. Reexamining the threshold for reexcision of histologically transected dysplastic nevi. JAMA Dermatol. 2016;152(12):1327-34. doi: https://doi.org/10.1001/jamadermatol.2016.2869
22. Engeln K, Peters K, Ho J, Jedrych J, Winger D, Ferris LK, et al. Dysplastic nevi with severe atypia: long-term outcomes in patients with and without re-excision. J Am Acad Dermatol. 2017;76(2):244-9. doi: https://doi.org/10.1016/j.jaad.2016.08.054
23. Fleming NH, Shaub AR, Bailey E, Swetter SM. Outcomes of surgical re-excision versus observation of severely dysplastic nevi: a single-institution retrospective cohort study. J Am Acad Dermatol. 2020;82(1):238-40. doi: https://doi.org/10.1016/j.jaad.2019.07.033
24. Pampena R, Kyrgidis A, Lallas A, Moscarella E, Argenziano G, Longo C. A meta-analysis of nevus-associated melanoma: prevalence and practical implications. J Am Acad Dermatol. 2017;77(5):938-945.e4. doi: https://doi.org/10.1016/j.jaad.2017.06.149
25. Dessinioti C, Befon A, Stratigos AJ. The association of nevus-associated melanoma with common or dysplastic melanocytic nevus: systematic review and meta-analysis. Cancers (Basel). 2023;15(3):856. doi: https://doi.org/10.3390/cancers15030856
26. Kaiser I, Pfahlberg AB, Uter W, Heppt MV, Veierød MB, Gefeller O. Risk prediction models for melanoma: systematic review on heterogeneity in model development and validation. Int J Environ Res Public Health. 2020;17(21):7919. doi: https://doi.org/10.3390/ijerph17217919
27. Errichetti E, Stinco G. Dermoscopy in general dermatology: a practical overview. Dermatol Ther (Heidelb). 2016;6(4):471-507. doi: https://doi.org/10.1007/s13555-016-0141-6
28. Wang YK, Gao YJ, Liu J, Zhu QL, Wang JC, Qin J, et al. Comparative study of melanocytic nevi classification with dermoscopy and high-frequency ultrasound. Skin Res Technol. 2022;28(2):265-73. doi: https://doi.org/10.1111/srt.13123
29. Garbe C, Amaral T, Peris K, Hauschild A, Arenberger P, Basset-Seguin N, et al. European consensus-based interdisciplinary guideline for melanoma. Part 1: diagnostics update 2022. Eur J Cancer. 2022;170:236-55. doi: https://doi.org/10.1016/j.ejca.2022.03.008
30. Garbe C, Peris K, Hauschild A, Amaral T, Arenberger P, Bastholt L, et al. European consensus-based interdisciplinary guideline for melanoma. Part 2: treatment update 2022. Eur J Cancer. 2022;170:256-84. doi: https://doi.org/10.1016/j.ejca.2022.04.018
31. Aubert H, Pere M, Bellier-Waast F, Perrot P, Barbarot S; Groupe de Recherche en Dermatologie Pédiatrique. Management of congenital melanocytic naevi in children: a French national survey. Acta Derm Venereol. 2020;100(19):adv00341. doi: https://doi.org/10.2340/00015555-3695
32. Rasner CJ, Zhou Y, Giubellino A. Recurrent nevus phenomenon developing within a keloid. Dermatopathology (Basel). 2023;10(3):201-6. doi: https://doi.org/10.3390/dermatopathology10030028
33. Cappilli S, Ribero S, Cornacchia L, Catapano S, Del Regno L, Quattrini L, et al. Melanocytic lesions with peripheral globules: proposal of an integrated management algorithm. Dermatol Pract Concept. 2023;13(1):e2023010. doi: https://doi.org/10.5826/dpc.1301a10
34. Jayasinghe D, Naranpanawa N, Ashley DP, Ingvar Å, Betz-Stablein B, Soyer HP, et al. Systematic review of nevus counting and reporting methodologies in contemporary studies of the general population. Dermatol Pract Concept. 2024;14(4):e2024223. doi: https://doi.org/10.5826/dpc.1404a223
35. Posada MIM, Gutiérrez Gómez M, Vásquez-Trespalacios EM, Garces Abad MA, Londoño García AM, González Álvarez T. Dermoscopic changes in melanocytic lesions during 5-year digital follow-up in patients with atypical nevus syndrome. Actas Dermosifiliogr. 2024;115(2):e1-e8. doi: https://doi.org/oi:10.1016/j.ad.2023.11.018
36. Mihulecea CRJ, Frățilă S, Rotaru M. Clinical-dermoscopic similarities between atypical nevi and early stage melanoma. Exp Ther Med. 2021;22(2):854. doi: https://doi.org/10.3892/etm.2021.10286
37. Gonzalez Matheus G, Robins CP, Muir J. Guide to shave procedures in general practice. Aust J Gen Pract. 2024;53(6):398-402.
doi: https://doi.org/10.31128/AJGP-06-23-6872
38. Guo Z, Ge L, Li Y, Gu Y, Wang W, Wei C, et al. History and prospect of melanocytic nevus treatment. J Dermatol Treat. 2023;34(1):2170010. doi: https://doi.org/10.1080/09546634.2022.2170010
39. Okada MAMU, Heck R, Marchiori Bakos R. Histological and immunohistochemical findings in recurrent melanocytic nevus. An Bras Dermatol. 2025;100(6):e501241. doi: https://doi.org/10.1016/j.abd.2025.501241
40. Kittler H, Rosendahl C, Cameron A, Tschandl P. Dermatoscopy: An algorithmic method based on pattern analysis. 2nd ed. Vienna: Facultas; 2016. 394 p.
41. Lorentzen H, Weismann K, Kenet RO, Secher L, Larsen FG. The dermatoscopic ABCD rule does not improve diagnostic accuracy of malignant melanoma. Acta Derm Venereol. 1999;79(6):469-72. doi: https://doi.org/10.1080/000155599750010256
42. Zalaudek I, Argenziano G, Soyer HP, Corona R, Sera F, Blum A, et al. Three-point checklist of dermoscopy: an open internet study. Br J Dermatol. 2006;154(3):431-7.
doi: https://doi.org/10.1111/j.1365-2133.2005.06983.x
43. Kittler H, Pehamberger H, Wolff K, Binder M. Diagnostic accuracy of dermoscopy. Lancet Oncol. 2002;3(3):159-65. doi: https://doi.org/10.1016/S1470-2045(02)00679-4
44. Rosendahl C, Cameron A, McColl I, Wilkinson D. Dermatoscopy in routine practice - 'chaos and clues'. [Internet]. Aust Fam Physician. 2012 [cited 2025 Dec 15];41(7):482-7. Available from: https://www.racgp.org.au/afp/2012/july/dermatoscopy-in-routine-practice
45. Tschandl P, Rinner C, Apalla Z, Argenziano G, Codella N, Halpern A, et al. Human-computer collaboration for skin cancer recognition. Nat Med. 2020;26(8):1229-34. doi: https://doi.org/10.1038/s41591-020-0942-0
46. Dinnes J, Deeks JJ, Saleh D, Chuchu N, Bayliss SE, Patel L, et al. Reflectance confocal microscopy for diagnosing cutaneous melanoma in adults. Cochrane Database Syst Rev. 2018;12(12):CD013190. doi: https://doi.org/10.1002/14651858.CD013190
47. Dinnes J, Deeks JJ, Grainge MJ, Chuchu N, Ferrante di Ruffano L, Matin RN, et al. Visual inspection for diagnosing cutaneous melanoma in adults. Cochrane Database Syst Rev. 2018;12(12):CD013194. doi: https://doi.org/10.1002/14651858.CD013194
48. Walsh T, Macey R, Riley P, Glenny AM, Schwendicke F, Worthington HV, et al. Imaging modalities to inform the detection and diagnosis of early caries. Cochrane Database Syst Rev. 2021;3(3):CD014545. doi: https://doi.org/10.1002/14651858.CD014545
49. Hryshchenko RV, Bohomolets OV, Stepanenko VI. [Benign and malignant (melanocytic and non-melanocytic) skin neoplasms: classification, clinical features, diagnostics, treatment strategy]. Ukrainskyi zhurnal dermatolohii, venerolohii, kosmetolohii. 2023;4:20-7. Ukrainian. doi: https://doi.org/10.30978/UJDVK2023-4-20
50. Rosendahl C, Voloshynovych MS, Hirnyk HYe, et al. [Algorithmic method of dermoscopic image analysis “Prediction without pigment” and its implementation in clinical practice]. Ukrainskyi zhurnal dermatolohii, venerolohii, kosmetolohii. 2020;3:62-68. Ukrainian. doi: https://doi.org/10.30978/UJDVK2020-3-62
51. Teledermatoscopy Study Group. [Comparative characteristics of dermoscopy and teledermoscopy in the diagnosis of pigmented skin lesions]. Ukrainskyi zhurnal dermatolohii, venerolohii, kosmetolohii. 2018;1:17-22. Ukrainian. doi: https://doi.org/10.30978/UJDVK2018-1-17
52. Makurina HI, Cherneda LO. [Algorithm for the use of a topical oxidizing agent in the treatment of seborrheic keratosis based on ultrasound and pathomorphological characteristics]. Ukrainskyi zhurnal dermatolohii, venerolohii, kosmetolohii. 2022;1-2(84-85):41-46. Ukrainian. doi: https://doi.org/10.30978/UJDVK2022-1-2-41
53. Hortynska OM. [Combined therapy of patients with skin neoplasms: clinical material and algorithmic approach]. Ukrainskyi zhurnal dermatolohii, venerolohii, kosmetolohii. 2022;1-2(84-85):22-28. Ukrainian. doi: https://doi.org/10.30978/UJDVK2022-1-2-22
54. Voloshynovych MS, et al. [Skin melanoma: from almost invisible to visually indisputable. Some principles of guidance and clinical cases review]. Ukrainskyi medychnyi chasopys. 2020;3(137):45-52. Ukrainian. doi: https://doi.org/10.32471/umj.1680-3051.137.179285
Key words: esophageal leiomyoma, postoperative complications, thoracoscopic surgery, enucleation; minimally invasive surgery, benign esophageal tumors, anastomotic leak, endoscopic vacuum therapy
Ключові слова: лейоміома стравоходу, післяопераційні ускладнення, торакоскопічна хірургія, енуклеація, малоінвазивна хірургія, доброякісні пухлини стравоходу, анастомотична негерметичність, ендоскопічна вакуум-терапія
Esophageal leiomyomas are the most common benign tumors of the esophagus. While surgical resection is the definitive treatment for symptomatic cases, it carries a risk of postoperative complications. This study presents a case series on the surgical management of esophageal leiomyomas, with a particular emphasis on postoperative complications and their management. This retrospective case series, conducted at the National Cancer Institute (Kyiv, Ukraine), analyzed patients who underwent surgical treatment for symptomatic esophageal leiomyoma between 2021 and 2024 and developed postoperative complications classified as Clavien-Dindo grade III or higher. Data were collected from medical records, including demographics, tumor characteristics, surgical details, postoperative course, complications, management strategies, and outcomes. The total number of observations was n=3. Three cases with Clavien-Dindo III-IV postoperative complications were analyzed. Complications included anastomotic leakage following Ivor Lewis esophagectomy (managed with endoscopic stenting and endoscopic vacuum therapy – EVT), esophageal perforation during enucleation leading to mediastinitis (managed with stenting and endoscopic vacuum therapy), and a complex case involving hemopericardium, post-cardiac arrest syndrome, peritonitis and diaphragmatic herniation requiring multiple reinterventions. Despite the severity of these complications, multidisciplinary management led to complete recovery of all patients. Histopathological evaluation confirmed benign leiomyoma in all cases. Surgical management of esophageal leiomyomas, particularly for large tumors, is often associated with significant postoperative complications. While minimally invasive techniques may reduce these risks, they do not eliminate them entirely. Endoscopic therapy plays a critical role in the non-surgical management of anastomotic leakage and esophageal perforation. Vigilant postoperative monitoring and a multidisciplinary approach are essential for achieving favorable outcomes in these complex cases.
Реферат
Ускладнення хірургічного лікування лейоміом стравоходу: серія випадків. Козак Є., Кондрацький Ю., Насташенко І., Добржанський О., Пепенін М., Колесник А., Шудрак Є., Городецький А., Турчак В., Коваль Н., Свічкар Я., Українець І., Бліжнікова С. Лейоміоми стравоходу є найпоширенішими доброякісними пухлинами стравоходу. Головним методом лікування симптомних випадків є хірургічне втручання, однак воно пов’язане з ризиком післяопераційних ускладнень. У цій роботі подано серію клінічних випадків хірургічного лікування лейоміом стравоходу з особливим акцентом на післяопераційні ускладнення та їх ведення. Ретроспективна серія випадків, проведена в Національному інституті раку (Київ, Україна), включала пацієнтів, яким у 2021-2024 роках виконано хірургічне лікування симптомної лейоміоми стравоходу та в яких розвинулися післяопераційні ускладнення класу Clavien–Dindo III або вище. Дані отримували з медичної документації; вони включали характеристику пухлини, деталі операції, перебіг післяопераційного періоду, ускладнення, стратегії лікування та результати. Загальна кількість спостережень – n=3. Проаналізовано три випадки з післяопераційними ускладненнями Clavien-Dindo III-IV. Серед ускладнень відзначено: неспроможність анастомозу після операції Льюїса (ендоскопічне стентування та ендоскопічна ВАК-терапія), перфорацію стравоходу під час енуклеації з розвитком медіастиніту (стентування та ендоскопічна ВАК-терапія), а також складний випадок із розвитком гемоперикарда, синдромом після зупинки серця, перитонітом і діафрагмальною грижею, що потребував багаторазових повторних втручань. Попри тяжкість ускладнень, мультидисциплінарний підхід до лікування забезпечив повне одужання всіх пацієнтів. Гістологічне дослідження у всіх випадках підтвердило доброякісну лейоміому. Хірургічне лікування лейоміом стравоходу, особливо великих пухлин, часто супроводжується значними післяопераційними ускладненнями. Мінімально інвазивні методики можуть зменшувати ці ризики, але не усувають їх повністю. Ендоскопічні методи (зокрема стентування та ендоскопічна ВАК-терапія) відіграють ключову роль у консервативному веденні неспроможності анастомозу та перфорації стравоходу. Пильний післяопераційний моніторинг і мультидисциплінарний підхід є визначальними для досягнення сприятливих результатів у таких складних клінічних ситуаціях.
Esophageal leiomyomas are the most common benign tumors of the esophagus, arising from the smooth muscle cells of the esophageal wall. Although the true incidence remains uncertain due to their frequently asymptomatic nature and incidental detection, these lesions are rare, accounting for less than 1% of all esophageal neoplasms. Typically slow-growing and having low malignant potential, esophageal leiomyomas are predominantly submucosal and may occur at any site along the esophagus, with a predilection for the lower two-thirds, corresponding to the greater abundance of smooth muscle tissue in this region [1].
Aim – to characterize the spectrum, timing, and severity (Clavien–Dindo grade III–IV) of postoperative complications following surgical management of symptomatic esophageal leiomyoma at the National Cancer Institute (Kyiv, 2021-2024), and to delineate the diagnostic and therapeutic algorithms employed, with particular emphasis on the role and effectiveness of endoscopic strategies – self-expanding stent placement and endoscopic vacuum therapy (EVT) – in organ-preserving management of anastomotic leakage and esophageal perforation.
Advancements in diagnostic imaging, particularly the increasing use of endoscopy, endoscopic ultrasonography, and cross-sectional imaging modalities, have led to more frequent identification of these tumors [2, 3]. A barium contrast study remains a valuable, noninvasive initial investigation, while endoscopic ultrasonography has emerged as a critical modality for evaluating the intramural characteristics of the tumor and assessing for associated lymphadenopathy [4].
Surgical resection remains the definitive treatment for symptomatic tumors, with the primary objective being complete excision while preserving esophageal integrity and function [5]. Traditional open thoracotomy has been largely supplanted by minimally invasive approaches, particularly thoracoscopic surgery, which offers the advantages of reduced postoperative morbidity, shorter hospital stays, and diminished wound complications [6, 7, 8]. Recently, endoscopic techniques such as submucosal dissection and enucleation have gained prominence, particularly for smaller tumors [9, 10, 11].
Histopathological evaluation characteristically reveals well-circumscribed lesions composed of intersecting fascicles of spindle cells with abundant cytoplasm. Immunohistochemical staining typically demonstrates positivity for desmin and alpha-smooth muscle actin, while typically negative for CD34, CD117, and S100, aiding in the differentiation from gastrointestinal stromal tumors [12]. Although many esophageal leiomyomas are asymptomatic, larger tumors may present with symptoms such as dysphagia, chest pain, retrosternal discomfort, heartburn, and regurgitation, occasionally mimicking malignant esophageal lesions and posing diagnostic challenges [13].
This case series describes our experience in the surgical management of esophageal leiomyomas, with a specific focus on the complications encountered and the strategies employed for their resolution. Despite the generally favorable prognosis associated with esophageal leiomyomas, surgical intervention carries a risk of complications, including esophageal perforation and anastomotic leak, necessitating careful perioperative planning and management.
MATERIALS AND METHODS OF RESEARCH
This is a retrospective case series conducted at the National Cancer Institute, Kyiv, Ukraine. The analysis included patients who underwent surgical treatment for esophageal leiomyoma between 2021 and 2024. Diagnosis was established based on clinical, radiological, endoscopic, and histopathological evaluations. We included patients with symptomatic esophageal leiomyoma confirmed by imaging who underwent surgical resection (either excision or enucleation), with subsequent histopathological confirmation of leiomyoma, and who experienced Clavien–Dindo grade III-IV complications.
Preoperative diagnostic evaluation included esophagogastroduodenoscopy (EGD), endoscopic ultrasonography (EUS), and contrast-enhanced computed tomography (CT) of the chest and abdomen. EUS-guided fine-needle aspiration biopsy was performed to facilitate diagnosis. Immunohistochemical staining was utilized to differentiate leiomyomas from gastrointestinal stromal tumors (GISTs) and other mesenchymal neoplasms. The choice of surgical approach was individualized based on tumor size, location, and involvement of surrounding structures. Data were retrospectively extracted from medical records, including patient demographics, comorbidities, tumor characteristics, surgical details, postoperative complications, and management strategies. The total number of observations was n=3. Statistical analysis: only descriptive statistics were applied. Continuous variables are presented as median and range (min–max); categorical variables as counts and percentages. No inferential tests were performed. No software was used.
We graded postoperative complications using the Clavien-Dindo classification and applied ECCG consensus definitions for esophagectomy-related complications. Esophageal leaks/perforations were managed with endoscopic vacuum therapy (EVT) following published techniques. The Ivor Lewis approach is cited as originally described. Reporting follows the PROCESS guidelines for surgical case series.
The study protocol was reviewed and approved by the Bioethics Commission of the National Cancer Institute, Kyiv, Ukraine (Protocol No. 1347, Meeting date: 03.07.2025). The study complied with the Declaration of Helsinki (2013 revision). All data were de-identified prior to analysis.
The requirement for individual informed consent was waived by the Bioethics Commission due to the retrospective design, use of de-identified data, and minimal risk to participants (Protocol No. 1347, 03.07.2025).
Case presentation
Case 1.
A 38-year-old Caucasian male was admitted with complaints of dysphagia, a globus sensation in the throat, intermittent heartburn, and periodic right upper quadrant abdominal pain. He reported symptoms persisting for several months without prior treatment.
Comorbidities included stage II arterial hypertension, chronic heart disease (stage I chronic heart failure). A congenital urinary tract anomaly-specifically, incomplete duplication of the left renal calyceal-pelvic system – as also noted.
Specific diagnostic procedures
Endoscopic examination revealed a rounded lesion measuring up to 3.5 cm in greatest dimension with an unaltered overlying mucosa. The tumor was located in the lower third of the esophagus and extended into the cardia of the stomach along the posterior wall.
Chest, abdomen, and pelvis CT scan with intravenous enhancement demonstrated a mass originating from the esophageal wall (Fig. 1).
Endoscopic ultrasound (EUS) visualized a hypoechoic lesion originating from the muscular layer of the esophageal wall. The lesion measured 18 mm in basal diameter, extended caudally along the gastric wall, and had a maximum length of 73 mm. It displayed a bean-shaped contour, homogeneous echotexture, and well-defined margins. Fine-needle aspiration biopsy was performed, but did not yield a definitive diagnosis.
Treatment
Due to the size and extent of the lesion, surgical enucleation was deemed technically infeasible. A two-stage treatment strategy was employed. The first stage involved diagnostic laparoscopy with biopsy of an enlarged perigastric lymph node and ligation of the left gastric artery. No histological evidence of malignancy was found. Subsequently, a minimally invasive Ivor Lewis esophagectomy and feeding jejunostomy placement were performed.
Postoperative complications
The patient was transferred from the ICU to a specialized surgical ward on postoperative day (POD) 1, after a chest X-ray confirmed no complications. Postoperative care included multimodal analgesia with epidural analgesia, antibiotic therapy (cefazolin, levofloxacin, and metronidazole), antifungal therapy (fluconazole), stimulation of gastrointestinal motility, jejunal feeding, and supplementary parenteral nutrition for 48 hours.
On POD 3, the patient developed fever, and subsequent CT revealed bilateral pneumonia and left-sided hydrothorax, prompting modification of the antibiotic regimen.
By POD 6, persistent fever has necessitated transition to broad-spectrum antibiotic therapy with colistimethate sodium and meropenem trihydrate. Nil by mouth was initiated with the switch to parenteral nutrition. An anastomotic leak at the esophagogastric junction was diagnosed on POD 7 via endoscopy, prompting stent placement. Initially, satisfactory stent placement was confirmed by CT. On POD 11, ultrasound detected pleural effusion, which was drained. On POD 13, due to persistent fever, the stent was removed. Further endoscopy revealed a defect involving one-third of the anastomotic circumference. CT demonstrated persistent dehiscence (6 mm) along the posterior wall and a second 4 mm defect, with bilateral hydrothorax and right-sided empyema. On POD 23, endoscopic vacuum therapy (EVT) was initiated under general anesthesia (Fig. 2). The EVT system was replaced ten times over the subsequent six weeks, resulting in gradual improvement. CT and endoscopy confirmed gradual improvement. A final endoscopy showed complete closure of the anastomotic defect with no evidence of passage obstruction. The patient was discharged in satisfactory condition on POD 41 for outpatient follow-up.
Complications included an anastomotic leak at the esophagogastric junction (Clavien-Dindo grade IIIb), bilateral lower lobe hospital-acquired pneumonia, external esophagocutaneous fistula, and mediastinitis.
Pathology: histopathological examination revealed a tumor with focal necrosis. Morphological features were most consistent with a gastrointestinal stromal tumor (GIST); however, immunohistochemical (IHC) analysis was required for confirmation. The resection margins were clear of tumor involvement, and all twelve regional lymph nodes were negative for malignancy. IHC demonstrated strong positivity for smooth muscle actin and desmin, supporting a smooth muscle origin. Ki-67 antigen expression was less than 1%. Markers for neurogenic differentiation (S-100) and gastrointestinal stromal tumors (CD34) were negative. In conclusion, the lesion was identified as a large benign leiomyoma of the esophagus.
Case 2.
A 24-year-old Caucasian female was admitted with Grade 4 dysphagia, postprandial fullness, weight loss, and moderate general weakness. She had been experiencing symptoms for six months and had previously sought medical attention for nausea, vomiting, chest pain, and weakness. The patient received inpatient care at her local healthcare facility.
Comorbidities included chronic cholecystitis.
Specific diagnostic procedures
Endoscopic examination revealed a rounded lesion externally compressing an 8 cm segment in the lower third of the esophagus along the right lateral wall, with intact mucosa. Erosions measuring 3-5 mm with semicircular distribution were observed at the gastroesophageal junction, accompanied by reactive hyperplasia of the gastric mucosa (Fig. 3).
Contrast-enhanced CT of the chest, abdomen, and pelvis showed circumferential thickening and distortion of the abdominal esophagus and gastric cardia, with a mass measuring 48×78 mm and a density of 60-63 Hounsfield units (Fig. 4). perigastric lymph nodes were not radiologically visible. Isolated para-aortic lymph nodes up to 13 mm were noted.
Endoscopic ultrasound (EUS) revealed an irregular, predominantly hypoechoic submucosal lesion measuring approximately 48×48 mm and extending over 80 mm in length in the lower esophagus. The lesion had clear contours, heterogeneous parenchyma, and multiple vascular loci by Doppler imaging, originating from the muscular layer without mucosal invasion. Transesophageal fine-needle biopsy (FNB) was consistent with leiomyoma.
Treatment.
Due to lesion size and extent, surgical enucleation was technically unfeasible. Minimally invasive Ivor Lewis esophagectomy with jejunostomy feeding tube placement was performed (Fig. 5).
On POD 1, chest radiography revealed a pericardial effusion, necessitating pericardial drainage (Fig. 6a). Subsequently, the patient developed acute clinical deterioration due to hemopericardium, a complication of the drainage procedure, resulting in asystole. Cardiopulmonary resuscitation was performed, successfully restoring spontaneous circulation. The patient's condition rapidly declined, characterized by hypotension, cardiovascular and respiratory failure, and severe chest pain. Contrast-enhanced computed tomography following drainage revealed hydropericardium with imaging suggestive of Budd-Chiari syndrome.
A massive transfusion protocol was initiated. Emergency surgical intervention was performed, consisting of thoracotomy, pericardiotomy, hemostasis via suture ligation of the marginal coronary vein, pericardial fenestration, and drainage of the right pleural cavity (Fig. 6 b). On postoperative day (POD) 6, tracheostomy was performed due to prolonged mechanical ventilation. By POD 14, the patient demonstrated clinical signs of peritonitis with localized guarding in the right iliac fossa, prompting urgent diagnostic laparoscopy with abdominal and pelvic cavity drainage and sanitation. On POD 19, computed tomography revealed herniation of the colon into the left pleural cavity through the esophageal hiatus. Emergency re-laparoscopy was undertaken, including repositioning of the colon into the abdominal cavity, crurorrhaphy, and comprehensive sanitation with drainage. The patient’s condition gradually improved, with resolution of multiple organ dysfunction syndrome (MODS) and hepatic dysfunction. Bedside mobilization commenced, supported by comprehensive care in the intensive care unit (ICU), including mechanical ventilation, renal replacement therapy, intravenous fluid administration, and pharmacologic management. The patient was transferred from the ICU to the surgical ward on POD 26, began oral nutrition, and was discharged in stable condition with outpatient follow-up on POD 34.
Complications: multiple organ dysfunction syndrome (MODS) involving cardiovascular, respiratory, hepatic, and renal failure; post–cardiac arrest syndrome; hemopericardium; intrapericardial hematoma; superior and inferior vena cava syndrome; diaphragmatic herniation; colon translocation into the left pleural cavity; peritonitis; postoperative acute pancreatitis; acute kidney injury; ischemic hepatitis; internal jugular and subclavian vein thrombosis; post-pulmonary embolism syndrome; thoracic stomach syndrome (TSS); and bilateral hospital-acquired pneumonia.
Pathology: histopathological examination confirmed a benign leiomyoma of the esophagus. All ten regional lymph nodes examined were negative for tumor involvement (Fig. 7).
Case 3.
A 55-year-old Caucasian male was admitted with complaints of heartburn and persistent epigastric pain unresponsive to treatment with omeprazole and ranitidine. The patient reported experiencing symptoms for ten months.
The patient’s comorbidities included stage I, grade I essential hypertension (moderate cardiovascular risk) and nodular goiter in a euthyroid state.
Specific diagnostic procedures
Endoscopic examination revealed a polypoid, elastic, mobile lesion approximately 3 cm in diameter, located 32 cm from the incisors. The overlying mucosa appeared intact.
A barium swallow demonstrated a round filling defect on the posterior wall of the lower third of the esophagus, measuring 39×29 mm, with well-defined margins and intramural calcifications. Contrast-enhanced CT of the chest, abdomen, and pelvis showed a well-circumscribed lesion measuring 25×22×30 mm in the middle third of the esophagus, narrowing the esophageal lumen to a slit-like configuration. The external contour of the esophageal wall remained intact (Fig. 8a).
Treatment
Due to its size and location, enucleation was deemed technically feasible. Thoracoscopic enucleation of the esophageal leiomyoma was performed. A mucosal defect occurred at the site of the prior endoscopic biopsy and was closed with interrupted sutures. The right pleural cavity was drained via the seventh intercostal space.
Postoperative complications
On postoperative day (POD) 1, the patient was diagnosed with esophageal perforation complicated by mediastinitis. Leakage was confirmed by assessing drain output after oral administration of a contrast dye. CT imaging of the chest, abdomen, and pelvis revealed signs of esophageal wall perforation. Endoscopic clipping and esophageal stent placement were performed, and a nasojejunal feeding tube was inserted for enteral nutrition. On POD 6, fluid collections in both pleural cavities were drained under ultrasound guidance. Follow-up endoscopy on POD 7 revealed a persistent esophageal wall defect with dense fibrin deposition above the stent. By POD 10, granulation tissue formation was observed at the defect site. On POD 18, CT imaging revealed an isolated esophago-atmospheric fistula extending to a drainage tract through the sixth intercostal space on the right. The stent was removed, and the esophageal defect had decreased to 7 mm. Endoscopic vacuum therapy (EVT) was initiated under general anesthesia. On POD 21, the EVT system was replaced and subsequently removed on POD 23. Fistulography was performed, followed by thrice-daily irrigation of the fistulous tract with antiseptic solutions. Daily drainage from the mediastinum amounted to approximately 85 mL of serous, saliva-mixed exudate. The drain was connected to a pleural aspirator. The patient received enteral feeding with 1000 mL of nutritional formula and 1500 mL of water per day. At discharge on POD 64, the patient was in satisfactory condition. He was afebrile, communicative, and reported no significant complaints. Sutures had been removed, and surgical drains remained in place and functional. The patient was transferred to a military hospital for continuation of care until complete closure of the esophago-atmospheric fistula.
Complications included esophageal perforation, bilateral lower-lobe hospital-acquired pneumonia, external esophagocutaneous fistula, and mediastinitis.
Pathology: a benign esophageal leiomyoma was identified, measuring 3.0×2.0×1.5 cm.
RESULTS AND DISCUSSION
Esophageal leiomyomas are rare benign tumors that originate from the smooth muscle layer of the esophageal wall. Although they generally follow an indolent course and are associated with an excellent prognosis after surgical resection, their management may be complicated, particularly in cases involving large tumors or those located near critical anatomical structures. In this case series, we reported three patients who underwent surgical treatment for esophageal leiomyomas, each of whom experienced significant postoperative complications that required active clinical management.
Minimally invasive approaches, such as thoracoscopic surgery and laparoscopic-assisted esophagectomy, have largely supplanted open thoracotomy in the treatment of esophageal leiomyomas. These techniques are favored due to reduced postoperative pain, lower rates of pulmonary complications, and shorter hospital stays. However, as demonstrated in this series, these benefits do not entirely eliminate the risk of serious complications.
The most critical complication observed was anastomotic leakage, which occurred in two patients following Ivor Lewis esophagectomy. Anastomotic leakage is a serious and potentially life-threatening postoperative complication that can lead to prolonged hospitalization, increased morbidity, and the need for additional interventions (Table). In both cases, endoscopic management – including esophageal stenting and endoscopic vacuum therapy (EVT) – was successfully employed to control the leaks non-operatively. EVT, in particular, proved highly effective in promoting defect closure and controlling mediastinal contamination, consistent with current literature supporting its utility in anastomotic leak management [14].
Another major complication was postoperative mediastinitis secondary to esophageal perforation – an infrequent but dangerous adverse event following enucleation. Prompt diagnosis and a multimodal approach incorporating endoscopic stenting, drainage, and EVT were critical for successful patient recovery.
One patient in our series developed an unusually complex combination of complications, including hemopericardium, post-cardiac arrest syndrome, peritonitis, and diaphragmatic herniation with translocation of the colon into the pleural cavity. This case required multiple surgical interventions and comprehensive multidisciplinary care. Despite the severity of these complications, the patient ultimately recovered, emphasizing the importance of vigilant monitoring and timely intervention for delayed or progressive postoperative issues.
Esophageal leiomyoma is the most common benign esophageal tumor; for symptomatic disease, enucleation remains standard, and minimally invasive approaches reduce peri-operative morbidity in contemporary series [15]. For large or unfavorably located tumors, conversion to esophagectomy may be required when safe dissection is not feasible or malignancy cannot be excluded. In our single-center series (n=3), major complications included an intrathoracic anastomotic leak after Ivor Lewis esophagectomy; reported leak incidences vary widely (~3-30%), emphasizing the need for standardized definitions [16]. We therefore graded complications with the Clavien-Dindo system and applied ECCG consensus definitions to enhance comparability [17, 18]. Management relied on self-expanding stents and endoscopic vacuum therapy (EVT); meta-analytic and comparative data show high EVT success and, in several analyses, superiority to stents, supporting its use alone or in hybrid strategies [19, 20]. Complete recovery in all cases underscores the value of early detection, timely endoscopic rescue, source control/drainage, nutritional support, and coordinated multidisciplinary care.
Case number Postoperative complications (Clavien-Dindo Grade) Case 1 Anastomotic leak (Grade IIIb), bilateral lower lobe hospital-acquired pneumonia (Grade II), esophagocutaneous fistula (Grade IIIb), mediastinitis (Grade II). Case 2 Hemopericardium (Grade IVa), cardiac arrest syndrome (Grade IVa), peritonitis (Grade IIIb), postoperative acute pancreatitis (Grade II), MODS (cardiovascular failure, respiratory failure, liver failure, renal failure) (Grade IVb), PE (Grade II), translocation of the colon into the left pleural cavity (Grade IIIb), hospital-acquired bilateral pneumonia (Grade II). Case 3 Esophageal perforation (Grade IIIb), pneumonia (Grade II), esophagocutaneous fistula (Grade IIIb), mediastinitis (Grade II).
Our findings highlight the increasing complexity of surgical management as tumor size and esophageal wall involvement grow. While enucleation remains the preferred treatment for small, well-circumscribed tumors, larger or more invasive leiomyomas may necessitate esophagectomy – an approach associated with higher perioperative risks.
Histopathological analysis in all cases confirmed the diagnosis of benign leiomyoma. Immunohistochemistry played a key role in differentiating these lesions from gastrointestinal stromal tumors (GISTs), which require distinct therapeutic strategies.
The outcomes in our patients underscore that while minimally invasive surgical techniques offer significant benefits, they require a high level of technical skill and meticulous perioperative planning to avoid complications. Additionally, the integration of endoscopic modalities into postoperative care has greatly enhanced the management of complications such as leaks and fistulas, contributing to improved patient outcomes [22, 23].
CONCLUSION
This study is limited by the small sample size, which reflects the rarity of symptomatic esophageal leiomyoma, and by its retrospective design. Nonetheless, the cases presented offer valuable insight into the complexities of surgical decision-making and complication management in this patient population.
Contributors:
Kozak Ye., Kondratskyi Yu., Nastashenko I., Dobrzhanskyi O., Pepenin M., Kolesnyk A., Shudrak Ye., Horodetskyi A., Turchak V., Koval N., Svichkar Ya., Ukrainets I., Blizhnikova S. – contributed to the retrospective data collection, statistical analysis and manuscript writing. Each author has reviewed and approved the final version of the manuscript.
Funding. This research received no external funding.
Conflict of interests. The authors declare no conflict of interest.
REFERENCES
1. Gowrie S, Noel A, Wooten C, Powel J, Gielecki J, Zurada A, et al. Slicing Through the Options: A Systematic Review of Esophageal Leiomyoma Management. Cureus. 2025;17(4):e81614. doi: https://doi.org/10.7759/cureus.81614
2. Impellizzeri G, Donato G, De Angelis C, Pagano N. Diagnostic Endoscopic Ultrasound (EUS) of the Luminal Gastrointestinal Tract. Diagnostics (Basel). 2024;14(10):996. doi: https://doi.org/10.3390/diagnostics14100996
3. Asaf BB, Bishnoi S, Puri HV, et al. Robotic enucleation of oesophageal leiomyoma: technique and surgical outcomes. J Minim Access Surg. 2022;18(1):84-9. doi: https://doi.org/10.4103/jmas.JMAS_263_20
4. Li W, Shao M, Hu S, Xie S, He B. The diagnostic value of endoscopic ultrasound for esophageal subepithelial lesions: a review. Medicine (Baltimore). 2024;103(46):e40419. doi: https://doi.org/10.1097/MD.0000000000040419
5. Tien TPD, Trung LV, Nguyen HN. Minimally Invasive Enucleation of Esophageal Leiomyoma: Experience From a Single Institution. Cureus. 2024;16(10):e71384. doi: https://doi.org/10.7759/cureus.71384
6. A-Lai GH, Hu JR, Yao P, Lin YD. Surgical Treatment for Esophageal Leiomyoma: 13 Years of Experience in a High-Volume Tertiary Hospital. Frontiers in Oncology. 2022;12:876277. doi: https://doi.org/10.3389/fonc.2022.876277
7. Mishra S, Jain N, Soni B, et al. Thoracoscopic enucleation of oesophageal submucosal tumours in prone position gives excellent long-term outcome: A single-centre experience. J Minim Access Surg. 2022;18(3):401-7. doi: https://doi.org/10.4103/jmas.JMAS_169_21
8. Tun KM, Dhindsa BS, Dossaji Z, et al. Efficacy and safety of submucosal tunneling endoscopic resection…: a systematic review and meta-analysis of 2900 patients. iGIE. 2023;2(4):529-537.e2. doi: https://doi.org/10.1016/j.igie.2023.08.005
9. Liapis SC, Baloyiannis I, Perivoliotis K, et al. Submucosal Tunneling Endoscopic Resection for Upper Gastrointestinal Subepithelial Lesions: A Systematic Review and Meta-Analysis. Journal of Gastrointestinal Cancer. 2025;56:110.
doi: https://doi.org/10.1007/s12029-025-01235-7
10. Kinney T, Waxman I. Treatment of benign esophageal tumors by endoscopic techniques. Semin Thorac Cardiovasc Surg. 2003;15(1):27-34. doi: https://doi.org/10.1016/S1043-0679(03)00004-2
11. Daitch ZE, Heller SJ. Endoscopic ultrasonography in esophageal carcinoma: a narrative review. Annals of Esophagus. 2023;6:14.
doi: https://doi.org/10.21037/aoe-21-25
12. Triantafyllou A, Mela E, Theodoropoulos C, et al. Addressing Anastomotic Leak After Esophagectomy: Insights from a Specialized Unit. J Clin Med. 2025;14(11):3694. doi: https://doi.org/10.3390/jcm14113694
13. Wang R, Guo Y, Duan X, Jiang H. Robot-assisted resection of oesophageal leiomyoma: a single-centre retrospective analysis of 57 cases. ANZ Journal of Surgery. 2025;95(3):356-62. doi: https://doi.org/10.1111/ans.70022
14. Ubels S, Lubbers M, Verstegen MHP, et al. Treatment of anastomotic leak after esophagectomy: insights of an international case vignette survey and expert discussions. Diseases of the Esophagus. 2022;35(12):doac020. doi: https://doi.org/10.1093/dote/doac020
15. Milito P, Asti E, Aiolfi A, et al. Clinical Outcomes of Minimally Invasive Enucleation of Leiomyoma of the Esophagus and Esophagogastric Junction. J Gastrointest Surg. 2020;24(3):499-504. doi: https://doi.org/10.1007/s11605-019-04210-3
16. Ubels S, Verstegen MHP, Rosman C, Reynolds JV. Anastomotic leakage after esophagectomy for esophageal cancer: risk factors and operative treatment. Annals of Esophagus. 2021;4:8. doi: https://doi.org/10.21037/aoe-2020-18
17. Clavien PA, Barkun J, de Oliveira ML, et al. The Clavien–Dindo classification of surgical complications. Annals of Surgery. 2009;250(2):187-96. doi: https://doi.org/10.1097/SLA.0b013e3181b13ca2
18. Low DE, Alderson D, Cecconello I, et al. International consensus on standardization of data collection for complications associated with esophagectomy. Annals of Surgery. 2015;262(2):286-94. doi: https://doi.org/10.1097/SLA.0000000000001098
19. Livingstone I, Maloney A, Chowdhury A, Caddy G. Current Status of Endoscopic Vacuum Therapy in the Management of Esophageal Perforations and Post-Operative Leaks. Clinical Endoscopy. 2021;54(6):789-97. doi: https://doi.org/10.5946/ce.2021.240
20. Han S, Girotra M, Abdi M, et al. Endoscopic vacuum therapy. iGIE. 2024;3(3):333-41. doi: https://doi.org/10.1016/j.igie.2024.06.003
21. Papadakos SP, Argyrou A, Katsaros I, et al. The Impact of EndoVAC in Addressing Post-Esophagectomy Anastomotic Leak in Esophageal Cancer Management. Journal of Clinical Medicine. 2024;13(23):7113. doi: https://doi.org/10.3390/jcm13237113
22. Goenka MK, Goenka U. Endotherapy of leaks and fistula. World Journal of Gastrointestinal Endoscopy. 2015;7(7):702-13. doi: https://doi.org/10.4253/wjge.v7.i7.702
23. Vohra I, Gopakumar H, Sharma NR, Puli SR. Efficacy of endoscopic vacuum therapy in esophageal luminal defects: systematic review and meta-analysis. Clinical Endoscopy. 2025;58(1):53-62. doi: https://doi.org/10.5946/ce.2023.282
Ключові слова: хронічне обструктивне захворювання легень у молодому віці, констриктивний бронхіоліт, бойові дії
Key words: young chronic obstructive pulmonary disease, obliterative bronchiolitis, hostilities
Підтвердження діагнозу хронічного обструктивного захворювання легень (ХОЗЛ) у пацієнтів молодого віку є складним, але важливим викликом для респіраторної медицини, адже це ключ до призначення коректної терапії захворювання, та відіграє значущу медико-соціальну роль. Термін «ХОЗЛ у молодому віці», або ж «молодий ХОЗЛ», використовується в Глобальній стратегії з діагностики, менеджменту та запобігання ХОЗЛ 2026 GOLD Report для позначення пацієнтів з ХОЗЛ у віці 20-50 років. Метою роботи було описати особливості діагностики ХОЗЛ у молодому віці та систематизувати новітні дані щодо диференційної діагностики з констриктивним бронхіолітом. Для цього був проведений пошук літератури за відповідною тематикою та ключовими словами в наукових базах даних PubMed, Google Scholar, Scopus та Web of Science. Після детального аналізу було відібрано й опрацьовано 53 літературних джерела, 90% яких були опубліковані протягом останніх 5 років та містили найактуальнішу інформацію. Встановлено, що в розвитку ХОЗЛ у пацієнтів молодого віку спостерігається переважання генетичних чинників над впливом факторів навколишнього середовища, серед яких найпоширенішою причиною є вроджений дефіцит альфа-1 антитрипсину. Привертає увагу й тенденція до зростання пошкодження дихальних шляхів унаслідок куріння сучасних пристроїв для вживання нікотину та тютюну – електронних сигарет нових поколінь та пристроїв для нагрівання тютюну, які особливо популярні серед молоді. Діагноз ХОЗЛ в осіб молодше 50 років можна розглянути за наявності не лише задокументованої персистуючої бронхіальної обструкції на спірометрії, яка не зникає після прийому бронхолітика, але і при тривалому стажі тютюнопаління (≥10 пачко-років) та типових змін на комп’ютерній томографії легень (емфізема та аномалії дрібних чи крупних бронхів). В умовах активних бойових дій важливим конкурентним діагнозом у таких пацієнтів виступає констриктивний (облітеруючий) бронхіоліт. Це захворювання проявляється зовнішньою компресією та іноді облітерацією бронхіол, і його варто розглядати через поєднання п’яти факторів, що включають нетиповий для ХОЗЛ молодий вік пацієнта, типові симптоми, персистуючу бронхіальну обструкцію, формування симптому "повітряних пасток" на комп’ютерній томографії легень, без ознак емфіземи та анамнестично підтверджене вдихання токсичних речовин. Таким чином, підтвердження діагнозу ХОЗЛ в осіб молодше 50 років потребує комплексного оцінювання стану пацієнта, що повинно включати вивчення легеневої функції (спірометрія), візуалізаційні дослідження (комп’ютерна томографія легень) та генетичне тестування (дефіцит альфа-1 антитрипсину). Зважаючи на те, що в умовах активних бойових дій, пов’язаних з Війною за Незалежність України, як військовослужбовці, так і цивільні громадяни можуть зазнавати суттєвого негативного впливу токсичних та подразнювальних речовин на респіраторну систему, обов’язковою складовою диференційної діагностики в пацієнтів молодого віку повинен розглядатись констриктивний бронхіоліт. Для верифікації діагнозу констриктивного бронхіоліту вирішальними є дані комп’ютерної томографії легень та підтвердження вдихання токсичних речовин. Але в певних клінічних ситуаціях відрізнити ці два діагнози дозволяє лише дослідження біоптатів легень.
Young chronic obstructive lung disease or constrictive bronchiolitis: difficulties in differential diagnosis in the context of hostilities. Feshchenko Y.I., Ostrovskyy M.M., Poberezhets V.L., Horovenko N.G., Pertseva T.O. Confirmation of the diagnosis of chronic obstructive pulmonary disease (COPD) in young patients is a difficult but important challenge for respiratory physicians, as it is the key to prescribing the correct therapy and has an important medical and social role. The term “young COPD” is used in the Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Lung Disease 2026 GOLD Report to refer to patients with COPD aged 20-50 years. The aim of the study was to describe the features of the diagnosis of young COPD and to systematize the latest data on the differential diagnosis with obliterative bronchiolitis. We conducted a literature search on the relevant topics and keywords in the scientific databases PubMed, Google Scholar, Scopus and Web of Science. After a detailed analysis, 53 literature sources were selected and evaluated, 90% of which were published over the past 5 years and contained the most up-to-date information. It has been established that genetic factors prevail over the influence of environmental factors in the development of COPD in young patients, among which the most common cause is congenital alpha-1 antitrypsin deficiency. However, there is a growing trend of airway damage as a result of smoking modern devices for nicotine and tobacco use, such as new generations of e-cigarettes and tobacco heating devices, which are especially popular among youth. The diagnosis of COPD in people younger than 50 years can be considered if the patient has not only persistent post-bronchodilator obstruction, but also presents a long history of smoking (≥10 pack-years) and typical changes on computed tomography of the lungs (emphysema and abnormalities of small or large bronchi). In the context of active hostilities, an important competitive diagnosis in such patients is obliterative bronchiolitis. This disease is manifested by external compression and sometimes obliteration of bronchioles, and should be considered when five factors are combined, including an atypical young age for COPD, typical symptoms, persistent bronchial obstruction on spirometry, the formation of the “air trapping” symptom on computed tomography of the lungs, no signs of emphysema, and an anamnesis of inhalation of toxic substances. Thus, confirmation of the diagnosis of COPD in people under 50 years of age requires a comprehensive assessment of the patient's condition, which should include pulmonary function testing (spirometry), imaging studies (computed tomography of the lungs), and genetic testing (alpha-1 antitrypsin deficiency). Given that in the context of active hostilities related to the War for Independence of Ukraine, both military personnel and civilians may be exposed to significant negative effects of toxic and irritating substances on the respiratory system, obliterative bronchiolitis should be considered as a mandatory component of the differential diagnosis in young patients. To verify the diagnosis of obliterative bronchiolitis, computed tomography of the lungs and confirmation of inhalation of toxic substances are crucial. However, in certain clinical situations, only lung biopsy assessment can distinguish between these two diagnoses.
«ХОЗЛ у молодому віці» – це термін, який був запропонований Глобальною ініціативою з хронічного обструктивного захворювання легень (GOLD) для позначення пацієнтів із хронічним обструктивним захворюванням легень у віці 20-50 років [1]. Питання діагностики хронічного обструктивного захворювання легень (ХОЗЛ) в осіб молодого віку є надзвичайно актуальним, зважаючи на певні парадокси в діагностиці. Адже, згідно з даними різних досліджень із залученням як пацієнтів із ХОЗЛ, так і некропсій, було встановлено, що типові для ХОЗЛ морфологічні зміни (емфізема та ремоделювання дихальних шляхів) починають розвиватись у хворих саме після 40 років та проявляються клінічно після 50 років [2]. Однак у популяції хворих на ХОЗЛ все ж є частка пацієнтів молодого віку [3]. Так, згідно з оцінками систематичного аналізу глобального тягаря від ХОЗЛ, поширеність ХОЗЛ в осіб молодого віку в таких країнах, як Китай та США, коливається в діапазоні 1,1-1,64% [4]. І ці пацієнти не повинні ігноруватись лікарями, адже, незважаючи на молодий вік, у них можуть спостерігатись суттєві зміни дифузійної здатності легень та розвиватись значна гіперінфляція, а ризик розвитку коморбідних станів та смертність є значно вищою, ніж у загальній популяції [5, 6]. Важливо також розуміти й відмінності терміна «ХОЗЛ у молодому віці» від «пре-ХОЗЛ», який було введено як термін для привертання нашої уваги до осіб з типовими симптомами, наявністю певних змін, виявлених методами візуалізаційного дослідження чи функції легень, але які не відповідають критеріям ХОЗЛ. Та все ж такі пацієнти належать до групи найвищого ризику розвитку ХОЗЛ у найближчий час [7]. Для успішної діагностики ХОЗЛ важливо також провести коректний диференційний діагноз, адже симптоми ХОЗЛ можуть зустрічатись при сотнях інших патологій. У цій статті ми б хотіли зупинитись на питанні диференційної діагностики ХОЗЛ саме з констриктивним бронхіолітом, адже в переважної більшості лікарів відомості щодо цього захворювання є досить обмеженими через недостатнє висвітлення у вітчизняній літературі. Це потенційно може створити проблему надмірної діагностики ХОЗЛ у хворих саме з цим діагнозом [8].
Саме тому метою нашої роботи було здійснити аналіз сучасної наукової літератури щодо особливостей діагностики ХОЗЛ у молодому віці; систематизувати новітні дані щодо диференційної діагностики ХОЗЛ у молодому віці саме з констриктивним бронхіолітом з урахуванням впливу факторів бойових дій в Україні, пов'язаних з Війною за Незалежність України.
Нами був проведений пошук літератури у відкритій базі даних біомедичної літератури PubMed, пошуковій системі вільного доступу наукових публікацій Google Scholar та баз даних наукових досліджень Scopus та Web of Science щодо механізмів формування ХОЗЛ у молодому віці, клінічних особливостей та стратегій лікування ХОЗЛ у когорти пацієнтів цього віку, а також особливостей диференційної діагностики ХОЗЛ з констриктивним бронхіолітом.
Під час аналізу було відібрано й опрацьовано 53 літературних джерела, переважна більшість (90%) містили найактуальнішу інформацію, тобто були опубліковані протягом останніх 5 років. Для пошуку літератури перш за все залучались англомовні та україномовні публікації, використовувались синоніми та комбінації ключових слів: «хронічне обструктивне захворювання легень», «ХОЗЛ», «молодий вік», «диференційна діагностика», «констриктивний бронхіоліт», «облітеруючий бронхіоліт», «бойові дії». У ході дослідження були використані такі методи: бібліографічний пошук, системний підхід, формально-логічний і метод узагальнення, аналітичний метод.
З аналізу виключались літературні джерела та публікації, які не були пов’язані з темою дослідження або були опубліковані іншими мовами, окрім як українською чи англійською. Публікації, що були опубліковані більше ніж 5 років тому, були включені в аналіз лише за умови, що вони є фундаментальними дослідженнями, без яких неможливо розглянути визначену проблематику. Також авторами було проведено детальний аналіз звіту Глобальної ініціативи з хронічного обструктивного захворювання легень «2026 GOLD Report». Це дослідження не залучало лабораторних тварин, пацієнтів чи здорових добровольців, тому не потребувало схвалення локальної біоетичної комісії.
Перш за все варто зрозуміти, які механізми лежать в основі виникнення ХОЗЛ, та визначити ті, які можуть бути визначальними незалежно від віку пацієнта. Виділяють такі процеси, які можуть призвести до формування ХОЗЛ у людини:
1. Порушення розвитку легень:
2. Надмірне пошкодження легень:
3. Ремоделювання дихальних шляхів:
4. Недостатнє відновлення дихальних шляхів:
Зважаючи на те, що в сучасному розумінні ХОЗЛ є гетерогенним станом, який виникає як результат взаємодії генетичних факторів із чинниками довкілля, то ми розуміємо, що в однієї особи може бути поєднання декількох перелічених процесів ураження дихальних шляхів.
Розберемо кожен з цих механізмів окремо.
1. Порушення розвитку легень
Порушення розвитку легень може виникнути на будь-якому етапі формування цього органа, починаючи із 17 тижня гестації і до 20-25 років, коли досягається максимальна легенева функція. Після досягнення максимуму протягом близько 10 років функція легень залишається без змін, формуючи так зване «плато легеневої функції», та в подальшому розпочинається фізіологічний процес зниження функції [9]. Порушеннями, що можуть збільшити ризик розвитку ХОЗЛ, є недостатня маса тіла при народженні [10], пасивне паління в дитячому віці [11], обтяжений сімейний анамнез захворювань органів дихання та часті госпіталізації у віці до 5 років [12,13].
Найбільш поширеним генетичним фактором ризику виникнення ХОЗЛ є мутація в гені SERPINA1. Ця мутація призводить до дефіциту альфа-1 антитрипсину, який є первинним плазменним та легеневим інгібітором серинових протеїназ, що захищає легеневу тканину від протеолітичного руйнування нейтрофілами. Саме тому дефіцит альфа-1 антитрипсину збільшує імовірність розвитку емфіземи, причому супутнє тютюнопаління в рази підвищує імовірність її виникнення. Однак є частина пацієнтів з дефіцитом альфа-1 антитрипсину, у яких розвивається емфізема і без супутнього тютюнопаління. Типовою є саме бібазальна панлобулярна емфізема. Іншим проявом дефіциту альфа-1 антитрипсину є ураження печінки. Ця мутація зустрічається з частотою 1 випадок на 2000-6000 осіб, але серед хворих на ХОЗЛ поширеність значно вища і становить 1-2% пацієнтів із ХОЗЛ. За приблизними підрахунками у світі проживає близько трьох мільйонів осіб з тяжким дефіцитом альфа-1 антитрипсину. Саме тому ВООЗ рекомендує всім без виключення хворим на ХОЗЛ хоча б раз у житті проходити скринінг на дефіцит альфа-1 антитрипсину [14, 15]. Однак дані глобального аналізу генетичного матеріалу від хворих на ХОЗЛ вказують на значення й інших генетичних факторів, адже у хворих на ХОЗЛ наявне тотальне переважання генетичних факторів, що відповідають за руйнування легеневої тканини, над її регенерацією [16, 17].
2. Надмірне пошкодження легень
Тютюнопаління є головним пошкоджувальним фактором, який негативно впливає на здоров’я легень у будь-якому віці. Так, тривалість фази «плато легеневої функції» може суттєво скоротитись під впливом тютюнопаління [9]. Стаж тютюнопаління ≥10 пачко/років розглядається як мінімальний стаж тютюнопаління, який може викликати ураження дихальних шляхів. Пришвидшене спадання легеневої функції, яке виражається в річному спаданні ОФВ1 більше ніж на 60 мл, може бути однією з ознак ХОЗЛ у молодому віці. Такий темп спадання був визначений як подвоєний темп нормального спадання ОФВ1 у здорових осіб, які ніколи не палили (25-30 мл/рік) [18]. Важливим є розуміння того, що механізми розвитку ХОЗЛ у молодих осіб, у яких функція легень не досягнула свого піку, та в тих, у кого виникло пришвидшене спадання легеневої функції, суттєво відрізняються, що може вимагати й різних терапевтичних стратегій ведення таких хворих [19].
Використання сучасних пристроїв для паління, таких як електронні сигарети різних поколінь чи пристрої для нагрівання тютюну, є новою загрозою для поширення ХОЗЛ, особливо серед молоді, серед якої відзначається надзвичайно висока популярність таких методів вживання нікотину [20]. Українська молодь не залишається осторонь, адже нещодавно проведені в Україні дослідження серед студентів українських ЗВО вказують на високу поширеність використання тютюнових і нікотиновмісних виробів для куріння, що коливається від 32,5% до 40,7% опитаних [21]. Найпоширенішими серед усіх можливих способів куріння були саме електронні сигарети, які використовували близько 2/3 усіх опитаних. Крім того, спостерігається чітка тенденція до все більшої популяризації такого виду вживання нікотину – зростання із 40,9% опитаних курців у 2022 році до 73,3% у 2025 році [22]. І хоча в сучасній науці існує мало відомостей про довготривалі ефекти використання сучасних пристроїв для паління, але все ж наявні дані вже підтверджують їх суттєву роль у формуванні гіперреактивності дихальних шляхів та інших негативних ефектів на легеневу функцію [23, 24].
Варто зазначити, що іноді в молодих осіб основним фактором розвитку ХОЗЛ може виступати забруднення повітря, а не паління [25]. Також не варто нехтувати й негативним впливом вірусних респіраторних інфекцій у формуванні ХОЗЛ у дорослих, однак дослідження все ж показують більше значення цього фактора саме в дитячому віці до досягнення максимальної легеневої функції [10].
3. Ремоделювання дихальних шляхів
Патологічні зміни дихальних шляхів, які виникають унаслідок бронхіальної астми, особливо в дитячому віці, можуть призвести до порушення розвитку максимальної легеневої функції, скорочення плато або пришвидшеного спадання ОФВ1. Саме тому в осіб, які хворіють на бронхіальну астму з дитинства, у віці понад 60 років ризик розвитку ХОЗЛ у більше ніж шість разів вищий, ніж у загальній популяції [26, 27]. Тож варто розуміти, що діагноз ХОЗЛ не виключає наявність бронхіальної астми в пацієнта, а часто є наслідком ремоделювання дихальних шляхів, зумовленого астмою.
4. Недостатнє відновлення дихальних шляхів
У нормі наш організм прямує до гомеостазу та намагається відновити пошкодження дихальних шляхів після негативного впливу респіраторних інфекцій, тютюнового диму чи вдихання забрудненого повітря. Але в певних ситуаціях таке відновлення є недостатнім. Одним з таких чинників є недостатнє надходження поживних речовин, наприклад унаслідок голодування, що може сприяти розвитку емфіземи [28, 29].
Діагностика ХОЗЛ у молодому віці
Діагностичні критерії для встановлення діагнозу ХОЗЛ у молодому віці такі ж, як і для інших пацієнтів – тобто передбачається наявність зафіксованого на спірометрії постбронходилятаційного співвідношення ОФВ1/ФЖЄЛ <0,7.
Якщо ж у пацієнта співвідношення ОФВ1/ФЖЄЛ після інгаляції бронхолітика є в межах норми, але хворого турбують типові симптоми ХОЗЛ та/або структурні зміни на комп’ютерній томографії (КТ) (емфізема) та/або порушення легеневої функції (зниження ОФВ1, «повітряні пастки», гіперінфляція, зниження дифузійної здатності легень чи швидке спадання ОФВ1), то це не дає нам можливості сформувати діагноз ХОЗЛ. Але ці хворі є в групі ризику розвитку бронхіальної обструкції в найближчий час, і тому вони об’єднані спільним терміном «пре-ХОЗЛ», який не є діагнозом.
Але, звичайно, не лише ХОЗЛ притаманна наявність постбронходилятаційного співвідношення ОФВ1/ФЖЄЛ <0,7. Тому є некоректним обґрунтування діагнозу ХОЗЛ виключно за даними спірометричного обстеження. Необхідно ретельно провести диференційну діагностику з іншими захворюваннями, беручи до уваги анамнестичні дані, оцінку симптомів, вплив тютюнопаління, забруднення повітря та дані інших інструментальних методів діагностики.
Потенційний діагноз ХОЗЛ в осіб молодше 50 років можна розглянути за наявності таких критеріїв:
Різке спадання ОФВ1 (≥60 мл/рік) за даними серійної спірометрії, що переважає спадання ФЖЄЛ, також може підтвердити розвиток захворювання в молодому віці, але також зустрічається і в курців без ХОЗЛ [17]. Таким хворим обов’язково слід пройти обстеження для скринінгу на дефіцит альфа-1 антитрипсину, який при позитивному результаті свідчить про переважний генетичний чинник у розвитку ХОЗЛ.
Ознаки ХОЗЛ на КТ
Визначення типових змін на КТ є важливим, адже дозволяє виявити ініціальні ознаки ХОЗЛ ще до появи клінічних симптомів та в деяких ситуаціях може використовуватись як метод скринінгу на ХОЗЛ [30, 31].
Розвиток бронхіальної обструкції при ХОЗЛ відбувається за рахунок певних структурних змін у легенях, які можна виявити при проведенні КТ ОГК, а саме:
Тобто типовими змінами на КТ для ХОЗЛ є емфізема та ураження дихальних шляхів (потовщення стінок бронхів та патологія дрібних бронхів). Важливо розуміти, що не в усіх хворих усі ці зміни будуть однаково виражені, адже, залежно від фенотипу ХОЗЛ, буде переважати або емфізема, або ураження дихальних шляхів. Розглянемо кожну з цих ознак окремо:
1. Емфізема легень є найпоширенішою ознакою ХОЗЛ, яку можна виявити на комп'ютерній томографії. Як і хронічний бронхіт, емфізема легень у сучасному розумінні не є окремим захворюванням, а є формою ХОЗЛ. Механізм виникнення емфіземи полягає в ураженні (збільшенні повітряного простору та руйнуванні стінок) легеневих ацинусів – структурних одиниць легень після розгалуження термінальних бронхіол, тобто респіраторних бронхіол, альвеолярних ходів та мішечків, альвеол [32]. Залежно від того, яка частина ацинуса переважно є ураженою, виділяють такі підтипи емфіземи:
Ураження легеневого ацинуса відбувається внаслідок активації клітин запалення, таких як макрофаги та нейтрофіли, що секретують різноманітні протеїнази як елемент захисту нашої імунної системи. Для протидії пошкоджувальним властивостям протеїназ у наших легенях існують антипротеолітичні механізми, основним з яких є утворення альфа-1 антитрипсину, що пригнічує активність нейтрофільної еластази [14].
2. Потовщення стінок дихальних шляхів є наслідком ремоделювання дихальних шляхів при ХОЗЛ, яке також можна визначити за допомогою комп’ютерної томографії легень високої роздільної здатності. Однак можливості комп’ютерної томографії дозволяють нам візуально оцінити лише стінки крупних бронхів. Якщо йде мова про патологію дрібних бронхів, яка є переважною причиною підвищення резистентності дихальних шляхів при ХОЗЛ, то наявні можливості комп’ютерної томографії, навіть найбільшої роздільної здатності, не дають нам змоги оцінити товщину бронхіол. Але ми можемо оцінити наявність патології дрібних дихальних шляхів (діаметром <2 мм) опосередковано за рахунок формування так званого симптому «повітряних пасток». Повітряні пастки – «gas trapping» визначаються як відсутність зменшення об'єму конкретної ділянки легені після видиху, тобто ділянки з низьким затуханням на експіраторній комп’ютерній томографії [30].
У хворих на ХОЗЛ на КТ можна також досить часто виявити бронхоектази та слизові пробки. Ці зміни патогенетично не пов’язані з формуванням персистуючої бронхіальної обструкції, проте можуть суттєво погіршувати перебіг захворювання:
Цікавим є те, що типові для ХОЗЛ зміни на КТ можуть виникати значно раніше, ніж виникнуть вентиляційні порушення, про що свідчать дані досліджень активних курців молодого віку з нормальною спірограмою [37].
За відсутності типових змін на КТ, тривалого тютюнопаління або впливу забруднення повітря діагноз ХОЗЛ є малоймовірним і його варто диференціювати з іншими захворюваннями. Типові для ХОЗЛ зміни на спірометрії можуть бути викликані й іншими захворюваннями легень, а саме:
На питання щодо складності діагностики ХОЗЛ намагалась дати відповідь міжнародна робоча група з діагностики ХОЗЛ COPDGene 2025 та CanCOLD [38]. У результаті нещодавнього масштабного дослідження група вказує на можливість упровадження в клінічну практику нового багатовимірного алгоритму діагностики ХОЗЛ, де основним діагностичним критерієм також визначається наявність постбронходилятаційного співвідношення ОФВ1/ФЖЄЛ <0,7 та принаймні 1 з 5 другорядних критеріїв:
або наявність виключно другорядного діагностичного критерію: при наявності щонайменше 3 з 5 другорядних критеріїв (які повинні обов’язково включати емфізему та потовщення стінки бронхів в осіб з респіраторними симптомами).
Констриктивний або ж облітеруючий бронхіоліт характеризується субепітеліальним фіброзом, зовнішньою компресією та іноді облітерацією бронхіол – дрібних дихальних шляхів, діаметром менше 2 мм, які не мають хрящів та підслизових залоз. Викликаний цей стан впливом чинників зовнішнього середовища, таких як токсичні або подразнювальні речовини, що вдихаються, включаючи випари, гази, продукти горіння. Також констриктивний бронхіоліт може бути асоційований з автоімунними захворюваннями, трансплантацією органів чи кісткового мозку, виникати як постінфекційне ускладнення після інфікування нижніх дихальних шляхів Mycoplasma pneumoniae чи аденовірусом, або навіть виникати без очевидної причини [39, 40, 41].
Найперші випадки констриктивного бронхіоліту були описані ще під час Першої світової війни як наслідок вдихання бойових газів – SO2, гідроген сульфіду та іприту [42]. Але цим подібні спостереження не завершились, і випадки такого ураження легень часто зустрічались у військовослужбовців різних країн, що брали участь у збройних конфліктах протягом минулого століття та військових конфліктах початку XXI століття в Іраку та Афганістані [43]. Пізніше також було описано і розвиток захворювання внаслідок вдихання попелу, діацетилу (ароматизатор для попкорну, який у 2000-х роках викликав високу захворюваність на бронхіоліт серед працівників фабрики з виробництва попкорну для мікрохвильової печі, що дало впізнавану назву ураження «попкорнова легеня») та скловолокна. Найтиповішими ознаками ураження є кашель, задишка та зниження толерантності до фізичного навантаження [44]. Окремі дослідження вказують на можливість розвитку констриктивного бронхіоліту також унаслідок контакту зі специфічними хімічними складовими диму при курінні електронних сигарет [45].
Зважаючи на те, що в наш час досить часто подібні симптоми зустрічаються саме в молодих військовослужбовців Сил оборони України, які під час участі в бойових діях контактували зі шкідливими випарами чи газами, то, на нашу думку, саме в констриктивному бронхіоліті й варто шукати причину подібного стану та з ним варто проводити диференційну діагностику ХОЗЛ. Клінічні спостереження в Україні, проведені під час теперішньої Війни за Незалежність України, вказують на достатньо високу поширеність констриктивного бронхіоліту серед військовослужбовців, що тривало контактували з продуктами згоряння – від 4% до 14%. А проспективне дослідження із включенням військовослужбовців Сил оборони України, які мали ознаки хронічних неспецифічних захворювань легень, встановило поширеність констриктивного бронхіоліту на рівні 2,8% [46]. Хоча цивільне населення України також може піддаватись негативному впливу на дихальну систему продуктів горіння внаслідок ракетно-дронових атак країною-агресором.
Поширеність констриктивного бронхіоліту важко оцінити, зважаючи на складність у діагностиці, однак у такій специфічній групі, як пацієнти, що перенесли трансплантацію легень, протягом 5 найближчих років після трансплантації бронхіоліт розвивається в більше ніж половини осіб [47]. Якщо ж мова йде про дітей реципієнтів гемопоетичних стовбурових клітин, то констриктивний бронхіоліт уражає 4,5-8,3% таких пацієнтів і зазвичай розвивається через 3 місяці після трансплантації [40].
Щодо поширеності постінфекційного констриктивного бронхіоліту, то варто зазначити, що переважна більшість таких випадків описана саме в дітей після інфікування аденовірусом, або мікоплазмою, а відомості щодо виникнення в дорослих є суттєво обмеженими [48, 49]. Цікаво, що найбільша поширеність постінфекційного констриктивного бронхіоліту відзначена в окремих країнах Латинської Америки, таких як Аргентина та Чилі, що потребує подальших досліджень для виявлення генетичної схильності саме в цих популяціях.
Унаслідок вдихання подразнювальних факторів або впливу інших чинників розвивається імунна дисфункція, що призводить до запалення субепітеліальних структур та порушення відновних процесів у дрібних дихальних шляхах і завершується фібропроліферативними процесами [50]. Важливою особливістю констриктивного бронхіоліту, на відміну від ХОЗЛ, є відсутність суттєвого ураження альвеол та легеневої паренхіми, тобто відсутність або мінімальні прояви емфіземи.
Для підтвердження діагнозу обов'язковим є виконання спірометрії, під час якої виявляється бронхіальна обструкція, яка не зникає після інгаляції стандартної дози бронхолітика – негативний тест на чутливість до бронхолітика, що ідентичне ХОЗЛ. Але на КТ можна виявити типові лише для констриктивного бронхіоліту ознаки: потовщення стінок бронхіол, мозаїчний патерн з плямистими ділянками гіпоатенуації, тобто ознаки формування «повітряних пасток» (табл. 1).
ХОЗЛ
Констриктивний бронхіоліт
Потовщення стінок дихальних шляхів
Потовщення стінок бронхіол
Симптом «повітряних пасток»
Симптом «повітряних пасток»
Центрилобулярна емфізема (або панацинарна при дефіциті альфа-1 антитрипсину)
-
Слизові пробки чи циліндричні бронхоектази, розташовані білатерально в нижніх частках легень
-
Таким чином, для верифікації констриктивного бронхіоліту, як конкурентного діагнозу до ХОЗЛ молодого віку, є необхідним поєднання п’яти основних компонентів – пентагональна діагностична модель Островського М.М.-Побережця В.Л. (2026): 1) вік пацієнта; 2) типові симптоми; 3) незворотня бронхіальна обструкція при спірометрії; 4) формування симптому «повітряних пасток» на КТ, без ознак емфіземи; 5) анамнестично підтверджене вдихання токсичних речовин.
Окремим пацієнтам, у яких діагностика навіть з використанням КТ становить труднощі, з метою підтвердження діагнозу може бути виконана біопсія легень. Гістопатологічна картина біоптатів легень у таких пацієнтів зазвичай представлена комбінацією патологічних змін саме в дистальній частині легень: фіброзна перебудова дрібних дихальних шляхів, дифузний фіброеластоз в альвеолярній тканині, васкулопатія та запалення/фіброз вісцеральної плеври [51]. Хоча патологічні зміни біоптатів легень можуть залежати від виду пошкоджувального чинника, що викликав захворювання, але все ж вони чітко відрізняються від ураження дрібних бронхів при ХОЗЛ, де типовими ознаками є закупорювання просвіту слизом, метаплазія келихоподібних клітин, нейтрофільна інфільтрація та прогресуюча втрата опорних альвеолярних кріплень (табл. 2) [52, 53].
ХОЗЛ
Констриктивний бронхіоліт
Слизові пробки
Фіброзна перебудова бронхіол
Метаплазія келихоподібних клітин
Дифузний фіброеластоз в альвеолярній тканині
Нейтрофільна інфільтрація
Васкулопатія
Прогресуюча втрата опорних альвеолярних кріплень
Запалення/фіброз вісцеральної плеври
На цей час, згідно з МКХ-10, чітко визначеного шифру для констриктивного бронхіоліту не існує, але цьому діагнозу може бути присвоєно один з таких шифрів: J44.8 – Інші уточнені обструктивні легеневі хвороби, J68.4 – Хронічні респіраторні захворювання, спричинені хімічними речовинами, газами, димом і парами, J84.8 – Інші уточнені інтерстиціальні легеневі хвороби [54]. Але вже згідно з МКХ-11, яка незабаром буде впроваджена в Україні, відповідним шифром буде CA26.0 «Хронічний облітеруючий бронхіоліт» [55].
ВИСНОВКИ
1. Діагноз хронічне обструктивне захворювання легень потрібно з обережністю встановлювати особам молодше 50 років, адже з великою імовірністю клінічний стан пацієнта може бути викликаний іншою патологією.
2. При підозрі на хронічне обструктивне захворювання легень у молодому віці пацієнту необхідно виконати ряд обов’язкових обстежень: постбронходилятаторна спірометрія, комп’ютерна томографія легень високої роздільної здатності, визначення рівня альфа-1 антитрипсину.
3. За наявності персистуючої бронхіальної обструкції, але за відсутності стажу тютюнопаління ≥10 пачко/років або впливу забрудненого повітря, типових змін на комп’ютерній томографії, нормального рівня альфа-1 антитрипсину, діагноз хронічного обструктивного захворювання легень є малоймовірним і його варто диференціювати з іншими захворюваннями, переважно з бронхіальною астмою та констриктивним бронхіолітом.
4. Зважаючи на високу інтенсивністю бойових дій, пов’язаних із Війною за Незалежність України, існує значна можливість контакту великої кількості військовослужбовців та цивільних осіб з токсичними речовинами, що має підвищити нашу настороженість щодо констриктивного бронхіоліту в цих осіб.
5. Для верифікації констриктивного бронхіоліту, як конкурентного діагнозу до хронічного обструктивного захворювання легень в осіб молодого віку, є необхідним поєднання п’яти основних компонентів: 1) вік пацієнта; 2) типові симптоми; 3) незворотня бронхіальна обструкція при спірометрії; 4) формування симптому «повітряних пасток» на комп’ютерній томографії без ознак емфіземи; 5) анамнестично підтверджене вдихання токсичних речовин.
Внески авторів:
Фещенко Ю.І. – концептуалізація, методологія, адміністрування проєкту, нагляд, написання – перегляд та редагування;
Островський М.М. – концептуалізація, методологія, адміністрування проєкту, нагляд, написання – перегляд та редагування;
Побережець В.Л. – концептуалізація, методологія, адміністрування проєкту, написання – оригінальний проєкт;
Горовенко Н.Г. – концептуалізація, методологія, нагляд, написання – перегляд та редагування;
Перцева Т.О. – концептуалізація, методологія, нагляд, написання – перегляд та редагування.
Фінансування. Дослідження не має зовнішніх джерел фінансування.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів.
1. 2026 GOLD Report and Pocket Guide. Global Initiative for Chronic Obstructive Lung Disease – GOLD [Internet]. 2026 [cited 2025 Nov 19]. Available from: https://goldcopd.org/2026-gold-report-and-pocket-guide/
2. Rennard SI, Drummond MB. Early chronic obstructive pulmonary disease: definition, assessment, and prevention. Lancet. 2015 May 2;385(9979):1778-88. doi: https://doi.org/10.1016/S0140-6736(15)60647-X
3. Li Y, Tang X, Zhang R, Lei Y, Wang D, Wang Z, et al. Research progress in early states of chronic obstructive pulmonary disease: a narrative review on PRISm, pre-COPD, young COPD and mild COPD. Expert Rev Respir Med. 2025 Oct;19(10):1063-79. doi: https://doi.org/10.1080/17476348.2025.2526775
4. Zhu Y, Shen T, Guo R, Liu K, Cao X, Yang X, et al. Global, regional, and national burden of young COPD, 1990-2021, with forecasts to 2050: a systematic analysis for the global burden of disease study 2021. BMC Public Health. 2025 Jan 22;25(1):276. doi: https://doi.org/10.1186/s12889-025-21414-2
5. Tan L, Li Y, Wang Z, Wang Z, Liu S, Lin J, et al. Comprehensive appraisal of lung function in young COPD patients: a single center observational study. BMC Pulm Med. 2024 Jul 24;24(1):358. doi: https://doi.org/10.1186/s12890-024-03165-9
6. Divo MJ, Marin JM, Casanova C, Cabrera LopezC, Pinto-Plata VM, Marin-Oto M, et al. Comorbidities and mortality risk in adults younger than 50 years of age with chronic obstructive pulmonary disease. Respir Res. 2022 Sep 27;23(1):267. doi: https://doi.org/10.1186/s12931-022-02191-7
7. Lee BY, Han MK. Understanding Early COPD. Respir Care. 2023 July;68(7):881-8. doi: https://doi.org/10.4187/respcare.10612
8. Yakovenko OK, Yakovenko TL. [Young COPD in the context of complex differential diagnosis]. Ukrainian Pulmonology Journal. 2025 Sep 8;33(3):47-47. Ukrainian. doi: https://doi.org/10.31215/2306-4927-2025-33-3-47-58
9. Tager IB, Segal MR, Speizer FE, Weiss ST. The natural history of forced expiratory volumes. Effect of cigarette smoking and respiratory symptoms. Am Rev Respir Dis. 1988 Oct;138(4):837-49. doi: https://doi.org/10.1164/ajrccm/138.4.837
10. Barker DJ, Godfrey KM, Fall C, Osmond C, Winter PD, Shaheen SO. Relation of birth weight and childhood respiratory infection to adult lung function and death from chronic obstructive airways disease. BMJ. 1991 Sep 21;303(6804):671-5. doi: https://doi.org/10.1136/bmj.303.6804.671
11. Svanes C, Omenaas E, Jarvis D, Chinn S, Gulsvik A, Burney P. Parental smoking in childhood and adult obstructive lung disease: results from the European Community Respiratory Health Survey. Thorax. 2004 Apr;59(4):295-302. doi: https://doi.org/10.1136/thx.2003.009746
12. Cosío BG, Pascual-Guardia S, Borras-Santos A, Peces-Barba G, Santos S, Vigil L, et al. Phenotypic characterisation of early COPD: a prospective case-control study. ERJ Open Res. 2020 Oct;6(4):00047-2020. doi: https://doi.org/10.1183/23120541.00047-2020
13. Çolak Y, Afzal S, Nordestgaard BG, Lange P, Vestbo J. Importance of Early COPD in Young Adults for Development of Clinical COPD: Findings from the Copenhagen General Population Study. Am J Respir Crit Care Med. 2021 May 15;203(10):1245-56. doi: https://doi.org/10.1164/rccm.202003-0532OC
14. Meseeha M, Sankari A, Attia M. Alpha-1 Antitrypsin Deficiency. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 [cited 2025 Nov 19]. Available from: http://www.ncbi.nlm.nih.gov/books/NBK442030/
15. Barrecheguren M, Hidalgo PP, Gonçalves JMF, de Miguel Díez J. Diagnosis of Alpha-1 Antitrypsin Deficiency (AATD) in Primary Care. Open Respir Arch. 2024;6(2):100310. doi: https://doi.org/10.1016/j.opresp.2024.100310
16. Cha SR, Jang J, Park SM, Ryu SM, Cho SJ, Yang SR. Cigarette Smoke-Induced Respiratory Response: Insights into Cellular Processes and Biomarkers. Antioxidants (Basel). 2023 Jun 3;12(6):1210. doi: https://doi.org/10.3390/antiox12061210
17. Kim SH, Lee H, Jo YS, Yoo J, Choi JY. Genome-Wide Association Analysis of Rapid Decline in Lung Function: Analysis From the Korean Genome and Epidemiology Study. J Korean Med Sci. 2024 Nov 4;39(42):e275. doi: https://doi.org/10.3346/jkms.2024.39.e275
18. Lange P, Celli B, Agustí A, Boje Jensen G, Divo M, Faner R, et al. Lung-Function Trajectories Leading to Chronic Obstructive Pulmonary Disease. N Engl J Med. 2015 Jul 9;373(2):111-22. doi: https://doi.org/10.1056/NEJMoa1411532
19. Martinez FJ, Agusti A, Celli BR, Han MK, Allinson JP, Bhatt SP, et al. Treatment Trials in Young Patients with Chronic Obstructive Pulmonary Disease and Pre-Chronic Obstructive Pulmonary Disease Patients: Time to Move Forward. Am J Respir Crit Care Med. 2022 Feb 1;205(3):275-87. doi: https://doi.org/10.1164/rccm.202107-1663SO
20. Mohd Shoaib SM, Ahmad N, Mahmud A. Prevalence and determinants of e-cigarette use among vocational college students: A cross-sectional study. PLoS One. 2025;20(6):e0311585. doi: https://doi.org/10.1371/journal.pone.0311585
21. Pylypiv LI, Piskur ZI, Pylypiv OH. [Prevalence of the Use of Modern Tobacco and Nicotine-Containing Products Among Students of Leading Universities in Lviv]. Tuberculosis, Lung Diseases, HIV Infection. 2023 Nov 30;(4):77-84. Ukrainian. doi: https://doi.org/10.30978/TB-2023-4-77.
22. Harkusha V, Poberezhets V, Demchuk A, Slobodian V. Trends in prevalence and motivation of tobacco use among youth 2022-2025. Eur Respir J. 2025;66(Suppl 69):PA5873. doi: https://doi.org/10.1183/13993003.congress-2025.PA5873
23. Amjad MA, Ocazionez Trujillo D, Estrada-Y-Martin RM, Cherian SV. E-Cigarette or Vaping Product Use-Associated Lung Injury: A Comprehensive Review. Int J Environ Res Public Health. 2025 May 17;22(5):792. doi: https://doi.org/10.3390/ijerph22050792
24. Shabil M, Malvi A, Khatib MN, Ganesan S, Kaur M, Srivastava M, et al. Association of electronic cigarette use and risk of COPD: a systematic review and meta-analysis. NPJ Prim Care Respir Med. 2025 Jul 7;35(1):31. doi: https://doi.org/10.1038/s41533-025-00438-6
25. Liao J, Zeng L, Huang X, Huang H, Shen C, Li J, et al. Burden of Chronic Obstructive Pulmonary Disease in China: A Global Burden of Disease Study on Temporal Trends, Risk Factor Contributions, and Projected Disease Burden from 1990 to 2030. COPD. 2025 Jul 7;22(1):2531016. doi: https://doi.org/10.1080/15412555.2025.2531016
26. Chang AB, Gray DM, Boonjindasup W, Irwin RS, Feng W, Beltetón E, et al. The impact of child and adolescent health on adult respiratory health: the evidence, gaps and priorities. Eur Respir Rev. 2025 Jul;34(177):250044. doi: https://doi.org/10.1183/16000617.0044-2025
27. Garcia-Aymerich J, de Las Heras M, Carsin AE, Accordini S, Agustí A, Bui D, et al. General population-based lung function trajectories over the life course: an accelerated cohort study. Lancet Respir Med. 2025 Jul;13(7):611-22. doi: https://doi.org/10.1016/S2213-2600(25)00043-8
28. Trethewey RE, Spartano NL, Vasan RS, Larson MG, O’Connor GT, Esliger DW, et al. Body mass index across adulthood and the development of airflow obstruction and emphysema. Chron Respir Dis. 2022 Nov 9;19:14799731221139294. doi: https://doi.org/10.1177/14799731221139294
29. Nitsch A, Kearns M, Mehler P. Pulmonary complications of eating disorders: a literature review. J Eat Disord. 2023 Jan 30;11:12. doi: https://doi.org/10.1186/s40337-023-00735-w
30. Labaki WW, Agusti A, Bhatt SP, Bodduluri S, Criner GJ, Fabbri LM, et al. Leveraging Computed Tomography Imaging to Detect Chronic Obstructive Pulmonary Disease and Concomitant Chronic Diseases. Am J Respir Crit Care Med. Am J Respir Crit Care Med. 2024 Aug 1;210(3):281-7. doi: https://doi.org/10.1164/rccm.202402-0407PP
31. Calverley PMA. Do You Believe in Magic? Computed Tomography, Artificial Intelligence, and Chronic Obstructive Pulmonary Disease. Am J Respir Crit Care Med. 2025 Jul;211(7):1112-3. doi: https://doi.org/10.1164/rccm.202502-0521ED
32. Pahal P, Avula A, Afzal M. Emphysema. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 [cited 2025 Nov 19]. Available from: http://www.ncbi.nlm.nih.gov/books/NBK482217/
33. Martínez-García MÁ, de la Rosa-Carrillo D, Soler-Cataluña JJ, Catalan-Serra P, Ballester M, Roca Vanaclocha Y, et al. Bronchial Infection and Temporal Evolution of Bronchiectasis in Patients With Chronic Obstructive Pulmonary Disease. Clin Infect Dis. 2021 Feb 1;72(3):403-10. doi: https://doi.org/10.1093/cid/ciaa069
34. da Silva SMD, Moreira MM, Paschoal IA, Pereira MC. Bronchiectasis associated with severe COPD: Clinical, functional, microbiological and tomographic features. Lung India. 2022;39(6):502-9. doi https://doi.org/10.4103/lungindia.lungindia_160_22
35. Alam MA, Mangapuram P, Fredrick FC, Singh B, Singla A, Kumar A, et al. Bronchiectasis-COPD Overlap Syndrome: A Comprehensive Review of its Pathophysiology and Potential Cardiovascular Implications. Ther Adv Pulm Crit Care Med. 2024;19:29768675241300808. doi: https://doi.org/10.1177/29768675241300808
36. Diaz AA, Orejas JL, Grumley S, Nath HP, Wang W, Dolliver WR, et al. Airway-Occluding Mucus Plugs and Mortality in Patients With Chronic Obstructive Pulmonary Disease. JAMA. 2023 Jun 6;329(21):1832-9. doi: https://doi.org/10.1001/jama.2023.2065
37. Ritchie AI, Donaldson GC, Hoffman EA, Allinson JP, Bloom CI, Bolton CE, et al. Structural Predictors of Lung Function Decline in Young Smokers with Normal Spirometry. Am J Respir Crit Care Med. 2024 May 15;209(10):1208-18. doi: https://doi.org/10.1164/rccm.202307-1203OC
38. COPDGene 2025 Diagnosis Working Group and CanCOLD Investigators, Bhatt SP, Abadi E, Anzueto A, Bodduluri S, Casaburi R, et al. A Multidimensional Diagnostic Approach for Chronic Obstructive Pulmonary Disease. JAMA. 2025 Jun 24;333(24):2164-75. doi: https://doi.org/10.1001/jama.2025.7358
39. Teper A, Colom AJ, Schubert R, Jerkic PS. Update in postinfectious bronchiolitis obliterans. Pediatr Pulmonol. 2024 Sep;59(9):2338-48. doi: https://doi.org/10.1002/ppul.26570
40. Shanthikumar S, Gower WA, Srinivasan S, Rayment JH, Robinson PD, Bracken J, et al. Detection of Bronchiolitis Obliterans Syndrome after Pediatric Hematopoietic Stem Cell Transplantation: An Official American Thoracic Society Clinical Practice Guideline. Am J Respir Crit Care Med. 2024 Aug 1;210(3):262-80. doi: https://doi.org/10.1164/rccm.202406-1117ST
41. Gutor SS, Richmond BW, Du RH, Wu P, Lee JW, Ware LB, et al. Characterization of Immunopathology and Small Airway Remodeling in Constrictive Bronchiolitis. Am J Respir Crit Care Med. 2022 Aug 1;206(3):260-70. doi: https://doi.org/10.1164/rccm.202109-2133OC
42. Krishna R, Anjum F, Oliver TI. Bronchiolitis Obliterans. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 [cited 2025 Nov 19]. Available from: http://www.ncbi.nlm.nih.gov/books/NBK441865/
43. Prodanchuk MG, Basanets AV, Kurdil NV. [Respiratory diseases caused by exposure to chemical air pollutants in territory of hostilities]. Ukrainian Pulmonology Journal. 2023;31(1):49-56. Ukrainian. doi: https://doi.org/10.31215/2306-4927-2023-31-1-49-56
44. Banks DE, Morris MJ. Inhalational Constrictive Bronchiolitis: The Evolution of our Understanding of this Disease. Lung. 2021 Aug;199(4):327-34. doi: https://doi.org/10.1007/s00408-021-00466-2
45. Carey L, Johnson K, Villalba J, Baqir M. Vaping-associated constrictive bronchiolitis. Respir Med Case Rep. 2024;51:102062. doi: https://doi.org/10.1016/j.rmcr.2024.102062
46. Feshchenko YI, Kurik LM, Prymushko NA, Kanarskyi OA, Krylach OI, Turchyna IP. [Inhalation risks in the war: chronic lung injury as a result of combat service]. Ukrainian Pulmonology Journal. 2025 Jun 20;33(2):5-5. Ukrainian.
doi: https://doi.org/10.31215/2306-4927-2025-33-2-5-16
47. Arjuna A, Olson MT, Walia R, Bremner RM, Smith MA, Mohanakumar T. An update on current treatment strategies for managing bronchiolitis obliterans syndrome after lung transplantation. Expert Rev Respir Med. 2021 Mar;15(3):339-50. doi: https://doi.org/10.1080/17476348.2021.1835475
48. Wan L, Wang Z. Postinfectious Bronchiolitis Obliterans in Children. Can Respir J. 2025;2025:7790381. doi: https://doi.org/10.1155/carj/7790381
49. Traunero A, Ghirardo S, Aldeco M, Pascolo P, Basilicata S, Mazzari L, et al. Outbreak of Post-Infectious Bronchiolitis Obliterans (PIBO) After Adenovirus Infection: A Case Series and Review of the Literature. Pediatr Pulmonol. 2025 Apr;60(4):e71080. doi: https://doi.org/10.1002/ppul.71080
50. Deng K, Lu G. Immune dysregulation as a driver of bronchiolitis obliterans. Front Immunol. 2024;15:1455009. doi: https://doi.org/10.3389/fimmu.2024.1455009
51. Gutor SS, Miller RF, Blackwell TS, Polosukhin VV. Environmental and occupational bronchiolitis obliterans: new reality. EBioMedicine. 2023 Sep;95:104760. doi: https://doi.org/10.1016/j.ebiom.2023.104760
52. Gutor SS, Richmond BW, Du RH, Wu P, Lee JW, Ware LB, et al. Characterization of Immunopathology and Small Airway Remodeling in Constrictive Bronchiolitis. Am J Respir Crit Care Med. 2022 Aug 1;206(3):260-70. doi: https://doi.org/10.1164/rccm.202109-2133OC
53. Polosukhin VV, Gutor SS, Du RH, Richmond BW, Massion PP, Wu P, et al. Small airway determinants of airflow limitation in chronic obstructive pulmonary disease. Thorax. 2021 Nov;76(11):1079-88. doi: https://doi.org/10.1136/thoraxjnl-2020-216037
54. ICD-10 Version: 2019 [Internet]. 2019 [cited 2026 Jan 17]. Available from: https://icd.who.int/browse10/2019/en
55. ICD-11 [Internet]. [cited 2026 Jan 17]. Available from: https://icd.who.int/en/