Ключові слова: меланоцитарний невус, дерматоскопія, патоморфологія, зворотний невус, рецидив, методи лікування
Key words: melanocytic nevus, dermoscopy, histopathology, recurrent nevus, recurrence, treatment methods
Реферат
Доброякісні меланоцитарні невуси є одними з найпоширеніших новоутворень шкіри та часто потребують діагностичних і лікувальних втручань у практиці лікаря-дерматолога. Незважаючи на широке впровадження дерматоскопії, зберігаються труднощі диференційної діагностики різних клініко-морфологічних форм невусів і вибору оптимальної лікувальної тактики. Неповне видалення пігментних утворень асоціюється з розвитком зворотного (рецидивного) невуса, формуванням рубців і появою діагностично складних пігментних змін, що зумовлює необхідність узагальнення сучасних наукових даних щодо клініко-дерматоскопічних і патоморфологічних кореляцій. Метою дослідження було проаналізувати та обґрунтувати сучасні наукові дані щодо клінічних, дерматоскопічних і патоморфологічних особливостей різних клініко-морфологічних форм доброякісних меланоцитарних невусів шкіри для обґрунтування індивідуалізованого вибору методу лікування, спрямованого на зниження частоти розвитку зворотного невуса, мінімізацію післяопераційних ускладнень і досягнення оптимального косметичного результату. Огляд виконано у форматі наративного аналітичного огляду з елементами систематизованого пошуку відповідно до рекомендацій PRISMA. У роботі застосовано бібліографічний, аналітичний, синтетичний, порівняльний методи, а також методи систематизації та узагальнення даних. Аналіз літератури проведено в базах даних PubMed/MEDLINE та PubMed Central у часовому інтервалі 2009-2025 років. У ході первинного пошуку ідентифіковано 312 публікацій, після виключення дублікатів проаналізовано 268 джерел, за результатами скринінгу назв й анотацій відібрано 97 статей, з яких 54 публікації включено до фінального якісного аналізу. Критеріями включення були оглядові, клінічні та клініко-морфологічні дослідження, а також міжнародні консенсусні рекомендації, що містили дані щодо дерматоскопічних і патоморфологічних характеристик доброякісних меланоцитарних невусів та методів їх лікування. Критеріями виключення були ізольовані клінічні випадки без аналітичного узагальнення, публікації, присвячені виключно меланомі, а також роботи без доступу до повного тексту. Як ключові слова використовували такі: «меланоцитарні невуси», «дерматоскопія», «патоморфологічні кореляції», «рецидивний невус», «методи лікування». За результатами аналізу встановлено, що дерматоскопічні патерни доброякісних меланоцитарних невусів відображають особливості їх патоморфологічної організації та змінюються залежно від віку пацієнта, тривалості існування й анатомічної локалізації утворення. Виявлено тісний зв’язок між дерматоскопічними ознаками та глибиною розташування меланоцитарних компонентів, що має принципове значення для вибору методу лікування. Часткові методи видалення, зокрема shave-ексцизія та аблятивні методики, асоційовані з вищою частотою репігментації та розвитку рецидивного невуса, тоді як повне хірургічне висічення забезпечує найвищу діагностичну безпеку за рахунок можливості первинної гістологічної верифікації, хоча може супроводжуватися більш вираженим рубцюванням. Отримані результати свідчать про доцільність індивідуалізованого підходу до лікування доброякісних меланоцитарних невусів на основі інтеграції клінічних, дерматоскопічних і патоморфологічних даних з метою зниження частоти рецидивів, мінімізації діагностичних труднощів і покращення косметичних результатів.
Abstract
Clinico-dermoscopic and histopathological correlations of benign melanocytic nevi of the skin as a basis for the choice of treatment and recurrence prevention (literature review). Torbenko Ye.L., Litus V.I. Benign melanocytic nevi are among the most common skin lesions and frequently require diagnostic and therapeutic interventions in dermatological practice. Despite the widespread implementation of dermoscopy, difficulties in the differential diagnosis of various clinico-morphological types of nevi and in the selection of optimal treatment strategies persist. Incomplete removal of pigmented lesions is associated with the development of the recurrent nevus phenomenon, scar formation, and diagnostically challenging pigmentation changes, highlighting the need for a comprehensive synthesis of current evidence on clinico-dermoscopic and histopathological correlations. The aim of the study was to analyze and substantiate current scientific data on the clinical, dermatoscopic, and pathomorphological features of various clinical and morphological forms of benign melanocytic skin nevi to justify the individualized choice of treatment method aimed at reducing the frequency of inverse nevus development, minimizing postoperative complications, and achieving optimal cosmetic results. The review was conducted as a narrative analytical with elements of a one structured search in accordance with PRISMA recommendations. Bibliographic, analytical, synthetic, and comparative methods, as well as data systematization and generalization techniques, were applied. The literature search was performed in the PubMed/MEDLINE and PubMed Central databases, covering the period from 2009 to 2025. A total of 312 publications were identified during the initial search. After duplicates removal, 268 records were screened, and 97 articles were selected based on title and abstract evaluation. Following full-text assessment, 54 publications were included in the final qualitative analysis. Inclusion criteria comprised review articles, clinical and clinico-morphological studies, as well as international consensus recommendations that reported data on dermoscopic and histopathological characteristics of benign melanocytic nevi and treatment methods. Exclusion criteria included isolated case reports without analytical synthesis, publications focused exclusively on melanoma, and studies without full-text availability. The keywords used were “melanocytic nevi,” “dermoscopy,” “histopathological correlations,” “recurrent nevus,” and “treatment methods.” The analysis demonstrated that dermoscopic patterns of benign melanocytic nevi reflect their underlying histopathological architecture and vary depending on patient age, lesion duration, and anatomical localization. A strong association was identified between specific dermoscopic features and the depth of melanocytic components, which is of critical importance for treatment selection. Partial removal techniques, including shave excision and ablative procedures, were associated with a higher risk of repigmentation and recurrent nevus development, whereas complete surgical excision provided the highest diagnostic reliability due to the possibility of primary histopathological verification, but it may be accompanied by a more pronounced scarring. The findings support the rationale for an individualized management strategy for benign melanocytic nevi based on the integration of clinical, dermoscopic, and histopathological data, aiming to reduce recurrence rates, minimize diagnostic uncertainty, and improve cosmetic outcomes.
Доброякісні меланоцитарні невуси шкіри є одними з найпоширеніших пігментних новоутворень у загальній популяції та становлять значну частку об’єктів клінічного оцінювання в дерматологічній практиці. За даними епідеміологічних досліджень, понад 80% дорослого населення мають принаймні один меланоцитарний невус, а у 20-30% осіб виявляються множинні утворення, кількість і розподіл яких залежать від віку, фототипу шкіри, генетичних чинників та рівня ультрафіолетового опромінення [1, 2]. Клінічна значущість меланоцитарних невусів виходить за межі їх поширеності, оскільки вони розглядаються як фенотипічний маркер підвищеного ризику розвитку меланоми – однієї з найбільш агресивних злоякісних пухлин шкіри [3].
Згідно з даними Всесвітньої організації охорони здоров’я та Міжнародного агентства з вивчення раку (IARC, GLOBOCAN), захворюваність на меланому шкіри у світі демонструє стійку тенденцію до зростання, особливо в регіонах із переважанням світлого фототипу населення [4]. У країнах Європи стандартизовані показники захворюваності в окремих регіонах перевищують 20-30 випадків на 100 000 населення, що зумовлює підвищену увагу до пігментних утворень як потенційних маркерів онкологічного ризику [5]. Хоча більшість меланом не розвивається безпосередньо з наявних невусів, численні та атипові меланоцитарні утворення розглядаються як незалежні фактори підвищеного ризику, що обґрунтовує необхідність їх ретельного оцінювання та обґрунтованого лікування [6].
В Україні проблема діагностики та лікування пігментних утворень шкіри, зокрема доброякісних меланоцитарних невусів, набуває особливої актуальності у зв’язку з нерівномірним упровадженням дерматоскопічних методів, обмеженим доступом до спеціалізованої допомоги та відсутністю уніфікованих національних рекомендацій щодо вибору методу лікування. За даними вітчизняних авторів, у клінічній практиці досі широко застосовуються деструктивні та часткові методи видалення пігментних утворень, зокрема shave-ексцизія та коагуляційні методики, нерідко без подальшої патоморфологічної верифікації, що підвищує ризик розвитку зворотного невуса та ускладнює подальшу диференційну діагностику пігментних змін у зоні рубця [13, 14]. Окремі українські дослідження також підкреслюють недостатню інтеграцію дерматоскопічних даних з патоморфологічними висновками та значну варіабельність клінічних підходів залежно від спеціальності лікаря й рівня закладу охорони здоров’я [15].
У сучасній дерматології дерматоскопія визнана стандартним неінвазивним методом первинного оцінювання пігментних утворень шкіри, що суттєво підвищує точність диференційної діагностики порівняно з клінічним оглядом неозброєним оком завдяки візуалізації підепідермальних структур і патернів росту [7]. Водночас її діагностична ефективність значною мірою залежить від коректної інтерпретації ознак та розуміння їх патоморфологічних корелятів, що стало підґрунтям для розробки міжнародних консенсусів й уніфікованої дерматоскопічної термінології [8].
Попри прогрес у діагностиці, вибір оптимального методу лікування доброякісних меланоцитарних невусів залишається предметом наукової дискусії. Часткові методи видалення, хоча й привабливі з косметичної точки зору, асоційовані з підвищеним ризиком неповного видалення меланоцитарної тканини та розвитку зворотного (recurrent) невуса [9]. За даними клініко-патологічних досліджень, частота неповних висічень меланоцитарних утворень навіть при первинному намірі радикального втручання може сягати 8-12%, тоді як після часткових методів видалення ризик репігментації та формування зворотного невуса зростає в кілька разів [10]. Відсутність первинної патоморфологічної верифікації після косметичного або часткового видалення суттєво ускладнює подальшу діагностичну тактику та часто зумовлює необхідність повторних або більш агресивних втручань [11, 12].
Таким чином, проблема лікування доброякісних меланоцитарних невусів має міждисциплінарний характер і потребує інтеграції клінічних, дерматоскопічних і патоморфологічних даних. Відсутність уніфікованого підходу до вибору методу лікування зумовлює варіабельність клінічних рішень і неоднозначність результатів, що визначає актуальність систематизації сучасних доказів та формування індивідуалізованої, алгоритмізованої моделі ведення пацієнтів.
Мета дослідження – проаналізувати та обгрунтувати сучасні наукові дані щодо клінічних, дерматоскопічних і патоморфологічних особливостей різних клініко-морфологічних форм доброякісних меланоцитарних невусів шкіри для обґрунтування індивідуалізованого вибору методу лікування, спрямованого на зниження частоти розвитку зворотного невуса, мінімізацію післяопераційних ускладнень і досягнення оптимального косметичного результату.
МАТЕРІАЛИ ТА МЕТОДИ ДОСЛІДЖЕНЬ
Цей огляд виконано у форматі систематизованого огляду літератури з елементами наративного аналізу відповідно до принципів доказової медицини та рекомендацій PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses). Процес відбору джерел відповідав основним етапам рекомендацій PRISMA; формування повноцінної PRISMA-діаграми не здійснювалося у зв’язку з оглядовим характером дослідження та відсутністю кількісного метааналізу.
Методологія дослідження була спрямована на всебічний і відтворюваний пошук, відбір та критичний аналіз наукових джерел, присвячених клінічним, дерматоскопічним і патоморфологічним особливостям доброякісних меланоцитарних невусів шкіри, а також результатам застосування різних методів їх лікування.
Для досягнення поставленої мети в процесі проведення дослідження застосовано такі методи: бібліографічний (систематизований пошук і відбір наукових джерел), аналітичний (критичний аналіз й оцінювання отриманих даних), синтетичний (узагальнення результатів окремих досліджень), порівняльний (зіставлення клінічних, дерматоскопічних і патоморфологічних характеристик, а також результатів різних методів лікування), системно-структурний та формально-логічний методи, а також методи систематизації та узагальнення наукової інформації.
Електронний пошук наукових публікацій здійснювали в міжнародних біомедичних базах даних PubMed/MEDLINE, Google Scholar та Scopus у часовому інтервалі 2009-2025 років. Пошукову стратегію формували з використанням комбінацій ключових слів і MeSH-термінів англійською мовою, зокрема: melanocytic nevi, benign melanocytic nevi, dermoscopy, clinico-dermoscopic correlation, histopathological correlation, recurrent nevus phenomenon, shave excision, surgical excision, treatment outcomes. Пошукові запити комбінувалися за допомогою логічних операторів AND та OR, що дозволяло розширювати або звужувати вибірку відповідно до завдань огляду. Додатково здійснювався ручний перегляд бібліографічних списків ключових оглядових статей, міжнародних консенсусних документів і рекомендацій професійних дерматологічних асоціацій.
Відбір публікацій проводився в кілька етапів. На етапі первинного пошуку ідентифіковано 312 публікацій. Після виключення дублікатів проаналізовано 268 джерел. За результатами скринінгу назв і анотацій відібрано 97 статей, з яких після повнотекстового аналізу 54 публікації включено до фінального якісного огляду відповідно до рекомендацій PRISMA.
Критеріями включення були оглядові та систематичні статті, міжнародні консенсусні рекомендації, клінічні, клініко-дерматоскопічні та клініко-патоморфологічні дослідження, у яких аналізувалися дерматоскопічні ознаки доброякісних меланоцитарних невусів, їх патоморфологічні кореляції та результати різних методів лікування з оцінкою частоти розвитку зворотного невуса і косметичних наслідків. Критеріями виключення були ізольовані клінічні випадки без аналітичного узагальнення, публікації, присвячені виключно злоякісним меланоцитарним новоутворенням без аналізу доброякісних невусів, експериментальні дослідження без клінічної верифікації, а також роботи без доступу до повного тексту або опубліковані в нерецензованих джерелах.
Оцінювання відібраних публікацій здійснювали шляхом якісного критичного аналізу з урахуванням дизайну досліджень, характеристик вибірок, клінічного контексту, застосованих діагностичних методів і терапевтичних підходів. Отримані результати систематизували за тематичними напрямами, що дало змогу провести порівняльний аналіз, виявити узгоджені та суперечливі положення літератури й сформулювати обґрунтовані висновки, релевантні для клінічної практики та подальших наукових досліджень.
Дослідження виконано з дотриманням принципів біоетики, викладених у Гельсінській декларації «Етичні принципи медичних досліджень за участю людей» та «Загальній декларації про біоетику та права людини» (ЮНЕСКО). Проведення дослідження схвалено локальною комісією з питань біоетики (протокол № 9 від 24.12.2025, Національний університет охорони здоров’я України).
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
Доброякісні меланоцитарні невуси шкіри є гетерогенною групою новоутворень, що демонструють значну варіабельність клінічних проявів і морфологічної структури. У фундаментальних роботах, присвячених біології невусів, показано, що їх формування відбувається за принципом послідовної міграції меланоцитів від дермо-епідермального з’єднання (dermo-epidermal junction, DEJ) до дерми з подальшим клітинним дозріванням, що лягло в основу класичної клініко-морфологічної класифікації [24, 25]. Саме ця концепція пояснює існування пограничних, складних і інтрадермальних форм невусів та їх відмінності в клінічній і дерматоскопічній картині.
Клініко-морфологічні форми доброякісних меланоцитарних невусів шкіри та їх клінічне значення
Клініко-морфологічна класифікація доброякісних меланоцитарних невусів є фундаментальною складовою сучасної дерматології, оскільки безпосередньо визначає особливості клінічного перебігу, дерматоскопічної картини та тактику лікування. Сучасні багатоцентрові дослідження та узагальнені огляди підтверджують, що різні морфологічні типи невусів демонструють характерні дерматоскопічні патерни, які корелюють з глибиною та архітектурою меланоцитарних компонентів [24, 25].
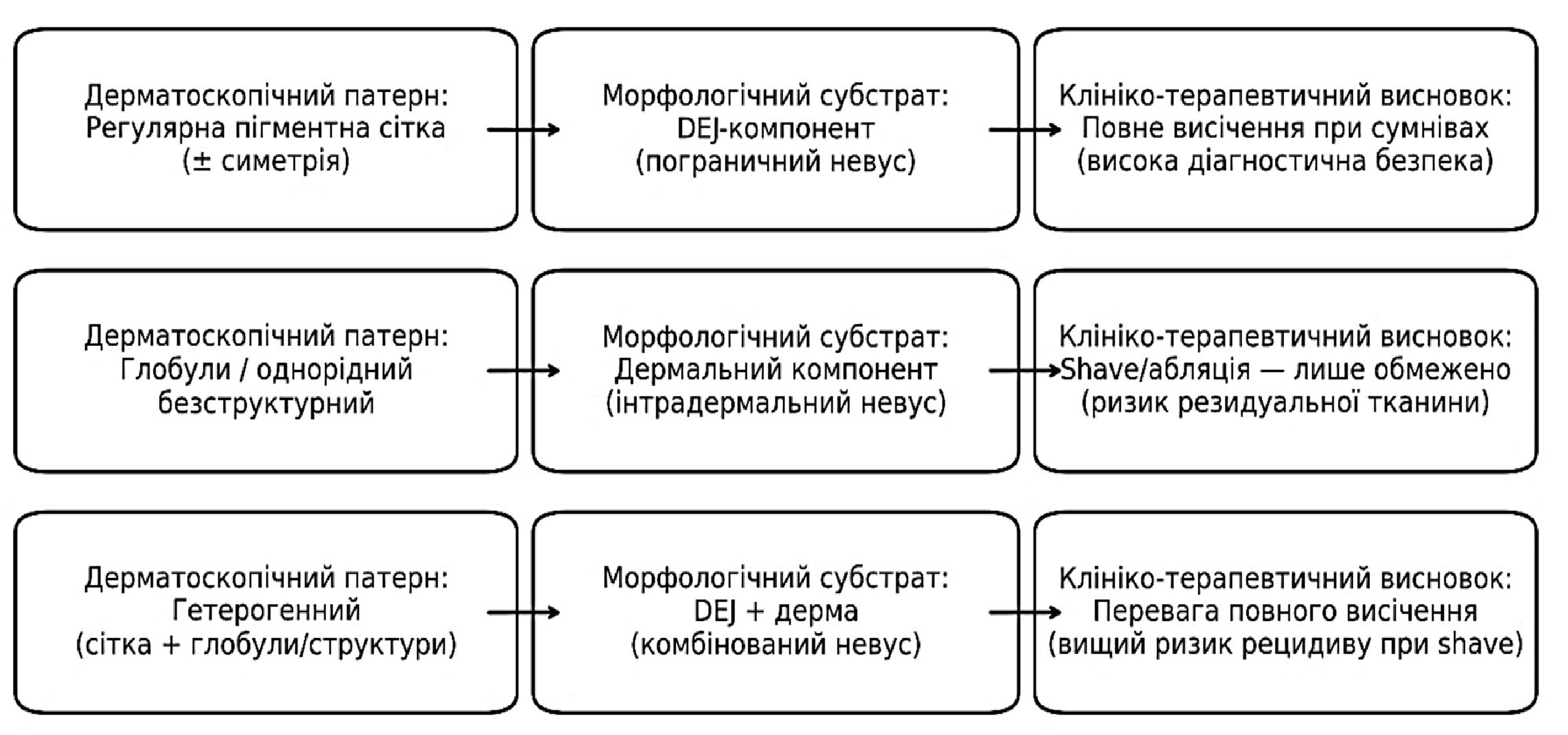
Установлено, що дерматоскопічні патерни доброякісних меланоцитарних невусів корелюють з глибиною та архітектурою меланоцитарного компонента, що має принципове значення для прогнозування ризику неповного видалення та вибору методу лікування (рис. 1).
Пігментна сітка відповідає поверхневому (пограничному) розташуванню меланоцитів на рівні дермо-епідермального з’єднання; глобулярні та безструктурні патерни корелюють з інтрадермальним компонентом; гетерогенні патерни характерні для комбінованих форм невусів. Схему розроблено авторами на основі узагальнення даних літератури [11, 12, 25]
За даними систематизованого аналізу дерматоскопічних патернів, пограничні меланоцитарні невуси частіше виявляються в молодих пацієнтів і зазвичай характеризуються регулярною пігментною сіткою та симетричною архітектурою [21]. Водночас сучасні дослідження свідчать, що в 15-25% таких утворень можуть бути наявні дерматоскопічні ознаки атипії, зокрема фокальна асиметрія або варіабельність товщини сітки, що істотно ускладнює їх диференціацію з ранніми формами меланоми, особливо за відсутності динамічного дерматоскопічного спостереження [22].
Комбіновані (складні) меланоцитарні невуси, за даними сучасних оглядів, демонструють значно більшу дерматоскопічну гетерогенність. У таких утвореннях часто поєднуються мереживні, глобулярні та безструктурні елементи, що відображає наявність меланоцитарних компонентів як на рівні дермо-епідермального з’єднання, так і в дермі [25, 33]. Саме ця морфологічна та дерматоскопічна неоднорідність зумовлює підвищену варіабельність діагностики і різні клінічні рішення лікарів щодо тактики ведення, зокрема у випадках косметичного видалення [24].
Інтрадермальні невуси залишаються найбільш поширеною клініко-морфологічною формою в дорослій популяції. За даними сучасних клінічних серій, вони становлять до 50-60% усіх меланоцитарних невусів, що підлягають видаленню в дерматологічній практиці [13]. Дерматоскопічно ці утворення переважно представлені глобулярними або однорідними безструктурними патернами з мінімальною архітектурною атипією, що загалом відповідає їх доброякісному морфологічному перебігу. Водночас саме інтрадермальні та комбіновані невуси найчастіше піддаються частковому видаленню з косметичною метою, що має суттєві клінічні наслідки [13, 30].
Окрему клінічну та прогностичну проблему становлять диспластичні (атипові) меланоцитарні невуси. Згідно із сучасними систематичними оглядами та метааналізами, наявність множинних диспластичних невусів асоціюється зі статистично значущим підвищенням ризику розвитку меланоми, однак абсолютний ризик трансформації окремого невуса залишається низьким [19, 20]. Саме диспластичні невуси найчастіше створюють складні діагностичні ситуації та є причиною як надмірних хірургічних втручань, так і недостатнього клінічного контролю.
Клініко-морфологічна форма невуса має безпосередній вплив не лише на діагностику, а й на результати лікування. За даними сучасних досліджень, ризик неповного видалення та розвитку зворотного невуса є статистично значуще вищим при поверхневих і комбінованих формах у разі застосування часткових методів, зокрема shave-ексцизії, порівняно з повним хірургічним висіченням [6, 13, 26]. Частота репігментації в зоні рубця в таких випадках може досягати 20-30%, що підтверджує необхідність урахування морфологічної структури утворення при виборі методу лікування [26].
Таким чином, дані сучасних досліджень переконливо свідчать, що клініко-морфологічна класифікація меланоцитарних невусів має не лише описовий, а й прогностичний характер. Вона визначає особливості дерматоскопічної картини, ризик діагностичних помилок і ймовірність розвитку зворотного невуса після лікування. Інтеграція морфологічних уявлень із сучасними дерматоскопічними критеріями є ключовою передумовою персоналізованого вибору тактики ведення пацієнтів з доброякісними меланоцитарними невусами шкіри [24, 30].
Узагальнення клініко-дерматоскопічних і патоморфологічних характеристик основних форм меланоцитарних невусів та їх значення для вибору методу лікування наведено в таблиці 1.
Клініко-морфологічна форма Типовий дерматоскопічний патерн Морфологічний субстрат Рекомендований метод лікування Ризик рецидиву Пограничний невус Регулярна пігментна сітка Меланоцити в DEJ Повне висічення Низький Комбінований невус Гетерогенний (сітка + глобули) DEJ + дерма Повне висічення Середній Інтрадермальний невус Глобулярний/ безструктурний Дермальний компонент Shave (обмежено)/ висічення Підвищений при shave Диспластичний невус Асиметрія, атипія Архітектурна атипія Висічення з гістологією Вищий
при сумнівах
У вітчизняному контексті проблема ведення пігментних утворень шкіри має додаткові детермінанти, пов’язані з нерівномірною доступністю дерматоскопії, відсутністю уніфікованих національних алгоритмів тактики та зростанням навантаження на систему охорони здоров’я в умовах воєнного часу. Українські автори підкреслюють актуальність дерматоонкологічних захворювань і потребу в організаційно-діагностичних рішеннях для зменшення частоти пізньої верифікації та тактичних помилок, що безпосередньо стосується і «сірої зони» пігментних утворень, де косметичні втручання нерідко виконуються без морфологічного підтвердження [49, 50].
Окремим практичним наслідком є підвищення частоти ситуацій, коли репігментація в рубці після часткового видалення потребує повторної діагностичної тактики (до повного висічення), оскільки первинної гістологічної верифікації не було [49]. У цьому аспекті українські оглядові роботи з біопсії шкіри наголошують на ключовій ролі морфологічного підтвердження в дерматоонкології, що має бути враховано при виборі методу видалення меланоцитарних утворень, особливо за наявності атипових ознак [51, 53, 54].
Додатково, українські хірургічні публікації, присвячені пігментним пухлинам у дитячій популяції, акцентують на необхідності методик, які забезпечують мінімізацію рецидивів і діагностичну визначеність, що логічно підтримує концепцію обґрунтованого вибору між косметичними частковими методами та повним висіченням з контролем країв/морфологічною верифікацією [51, 52].
Дерматоскопічні патерни доброякісних меланоцитарних невусів та їх патоморфологічні кореляції
Дерматоскопія суттєво розширила можливості неінвазивної диференційної діагностики пігментних утворень завдяки візуалізації структур, які мають морфологічний субстрат. Проте практична цінність дерматоскопії прямо залежить від уніфікованої мови опису. У межах третьої консенсус-конференції International Society of Dermoscopy (IDS) запропоновано стандартизовану рамку термінів (аналітичних/описових і метафоричних), а також продемонстровано, що серед учасників 23,5% переважно використовують описову термінологію, 20,1% – метафоричну, а 56,5% комбінують обидві; водночас значна частина нових термінів залишалася маловідомою для більшості респондентів [31]. Це підкреслює методологічну проблему: без стандартизації термінів зростає варіабельність діагностики, а отже – ризик різних клінічних рішень щодо того самого невуса.
З позицій доказовості, алгоритмізація дерматоскопічного оцінювання дозволила кількісно оцінювати діагностичну ефективність. Класичний приклад – ABCD-правило дерматоскопії, перспективно протестоване на 172 меланоцитарних пігментних утвореннях: за порогового значення Total Dermoscopic Score >5,45 як злоякісні класифікувалися 64/69 меланом (92,8%), тоді як серед утворень з нижчим балом як доброякісні класифікувалися 93/103 невуси (90,3%) [32]. Отже, навіть ранні алгоритми демонстрували високу інформативність в сумнівних клінічних ситуаціях, але їх обмеженням залишалася залежність від коректного визначення структури та кольорів і, відповідно, від навченості лікаря.
Подальший розвиток отримали чек-листки, які поєднують структурний аналіз із сумарною оцінкою ознак. У класичному порівняльному дослідженні Argenziano et al. 7-пунктовий чек-листок продемонстрував чутливість 95% і специфічність 75%, тоді як ABCD-правило 85% і 66% відповідно (у загальному порівнянні методик на навчальній/тестовій вибірках), що дало підстави розглядати 7-пунктовий підхід як більш чутливий інструмент для виявлення меланоми в сумнівних випадках [33]. Важливо, що автори також показали різницю між підходами залежно від досвіду лікаря, що напряму пов’язує результати дерматоскопії з питанням стандартизації навчання та інтерпретації.
Надалі ці алгоритми були переоцінені в умовах сучасної клініки, коли лікар частіше бачить ранні меланоми та множинні атипові невуси, а не лише «класичні» форми. У дослідженні «Seven-point checklist revisited» (8 експертів; набори: 100 висічених меланом, 100 висічених невусів, 100 невусів під спостереженням) показано, що за pattern analysis 82% меланом були правильно оцінені як такі, що підлягають висіченню, а 87,5% моніторованих невусів як доброякісні [34]. Для 7-пунктового чек-листка перехід до зниженого порогу (revised threshold) підвищував частку рекомендацій щодо висічення в групі меланом із 77,9% до 87,8%, але зменшував частку рекомендацій «не висікати» у групі моніторингу з 85,6% до 74,5% [34]. Ці цифри добре ілюструють принципову дилему: підвищення чутливості в реальній практиці часто супроводжується «ціною» у вигляді більшої кількості втручань у доброякісних випадках, що особливо важливо при плануванні тактики для невусів з урахуванням косметичних очікувань пацієнта.
Окреме практичне значення має 2-кроковий підхід, де першим завданням є класифікація утворення як меланоцитарного або немеланоцитарного. У дослідженні Tschandl et al. (707 послідовних випадків) чутливість першого кроку становила 97,1% в пацієнтів з Австралії та 96,8% в пацієнтів з Центральної Європи, однак специфічність була низькою й різнилася між популяціями (33,6% та 67,9% відповідно) [35]. Автори деталізували причини помилок: зокрема, пігментна сітка в немеланоцитарних ураженнях була причиною помилкової класифікації в 68 випадках (25,2%), а відсутність характерних дерматоскопічних ознак – у 69 випадках (25,6%) немеланоцитарних утворень [35]. Для клінічної практики це означає, що високочутливий скринінговий перший крок може навмисно «перестраховуватися», але без другого кроку (оцінки патернів/ознаки атипії) він не забезпечує достатньої точності рішень щодо лікування.
Ключовим підґрунтям для побудови дерматоскопічних критеріїв лікувальної тактики є саме клініко-дерматоскопічно-патоморфологічні кореляції. У роботі Woltsche et al. запропоновано узагальнений погляд на доброякісні невуси, які підкреслюють, що дерматоскопічні патерни відображають конкретні гістологічні субстрати, формуючи міст між клінічною оцінкою та морфологічною верифікацією [36]. У практичному сенсі це підтримує концепцію, що вибір методу видалення (повне висічення з верифікацією країв vs часткові косметичні методи) має ґрунтуватися не лише на зовнішньому вигляді, а й на прогнозованій глибині/архітектурі меланоцитарного компонента, яку частково можна оцінити через патерн-аналіз та узгоджені дерматоскопічні критерії [31, 36].
Дерматоскопічні ознаки, що визначають вибір методу лікування та ризик розвитку зворотного невуса
Одним з ключових практичних завдань сучасної дерматології є трансляція дерматоскопічних даних в обґрунтоване клінічне рішення щодо вибору методу лікування меланоцитарного невуса. На відміну від діагностичних алгоритмів, спрямованих передусім на виявлення меланоми, лікувальна тактика потребує оцінювання не лише ступеня дерматоскопічної атипії, а й прогнозованої морфологічної структури утворення, глибини залягання меланоцитарного компонента та ризику його неповного видалення.
Сучасні дослідження підтверджують, що певні дерматоскопічні патерни мають тісний зв’язок з гістологічною архітектурою невусів. Регулярна пігментна сітка частіше корелює з поверхневим (пограничним) розташуванням меланоцитів, тоді як глобулярні та однорідні безструктурні патерни асоціюються з інтрадермальними або комбінованими формами [21, 25]. З клінічної точки зору це має принципове значення, оскільки поверхневі та комбіновані утворення при застосуванні часткових методів видалення частіше залишають резидуальну меланоцитарну тканину, що створює умови для розвитку зворотного (recurrent) невуса [6, 13].
За даними сучасних клінічних серій і ретроспективних аналізів, частота репігментації в зоні рубця після shave-ексцизії меланоцитарних невусів коливається в межах 20-30% залежно від морфологічного типу утворення та анатомічної локалізації, тоді як після повного хірургічного висічення цей показник є статистично значуще нижчим [13, 26]. В інших дослідженнях також показано, що поєднання поверхневого дерматоскопічного патерна з косметичними методами видалення є одним з найважливіших предикторів розвитку зворотного невуса та повторних втручань [6, 11].
Особливої клінічної уваги потребує дерматоскопічна оцінка рубцевих змін після попередніх втручань. Сучасні дослідження демонструють, що репігментація в межах рубця після неповного видалення невуса може мати асиметричний характер і включати безструктурні зони, сіро-коричневі ділянки або нерівномірні глобули, що морфологічно відповідає залишковій або реактивній меланоцитарній проліферації [8, 9]. Водночас ключовим диференційно-діагностичним критерієм між зворотним невусом і рецидивом меланоми вважається поширення пігментації за межі рубця, що підтверджено як дерматоскопічними, так і гістологічними даними [9, 26].
У дослідженнях, присвячених аналізу діагностичних помилок, показано, що відсутність первинного гістологічного висновку після косметичного або часткового видалення істотно підвищує діагностичну невизначеність при появі пігментації в рубці. У таких клінічних ситуаціях більшість сучасних рекомендацій розглядають повне хірургічне висічення як метод вибору незалежно від початкової дерматоскопічної оцінки [6, 14, 26]. Це підкреслює важливий практичний аспект: дерматоскопічні ознаки не можуть інтерпретуватися ізольовано від анамнестичних і морфологічних даних, а первинний вибір методу лікування має довготривалі діагностичні наслідки.
Косметичний аспект лікування меланоцитарних невусів, хоча й не є первинним з онкологічної точки зору, суттєво впливає на клінічні рішення. Порівняльні сучасні дослідження свідчать, що shave-ексцизія асоціюється з менш вираженим первинним рубцем і швидшим загоєнням, однак ці переваги часто нівелюються в разі розвитку рецидиву, який потребує повторного, більш радикального та травматичного втручання [13]. Таким чином, короткостроковий косметичний виграш може трансформуватися в гірший довгостроковий клінічний та естетичний результат.
Порівняльні характеристики основних методів видалення меланоцитарних невусів з урахуванням ризику рецидиву та косметичних результатів узагальнено в таблиці 2.
Системний аналіз літератури також демонструє, що ризик неповного видалення та рецидиву залежить не лише від вибраного методу, а й від анатомічної локалізації утворення. У ділянці голови та шиї, а також на тулубі частота маргінальних або неповних резекцій є вищою, що пов’язано як з анатомічними особливостями, так і з прагненням мінімізувати косметичний дефект [6, 11]. Це додатково підкреслює необхідність індивідуалізованого підходу до вибору методу лікування з урахуванням дерматоскопічних, клінічних і морфологічних характеристик невуса.
Метод Переваги Недоліки Частота рецидиву Косметичний результат Shave-ексцизія Швидко, мінімальний рубець Неповне видалення 10-30% Короткостроково кращий Еліптичне висічення Повнота, гістологія Рубець <5% Довгостроково стабільний Лазер Косметика Без гістології Невідомо Варіабельний
Узагальнюючи наведені дані, можна стверджувати, що дерматоскопія відіграє ключову роль не лише в диференційній діагностиці доброякісних меланоцитарних невусів, а й у стратифікації ризику їх неповного видалення та розвитку зворотного невуса. Проте її ефективність як інструменту вибору лікувальної тактики реалізується лише за умови інтеграції з клінічними параметрами, морфологічними уявленнями та чітким усвідомленням обмежень часткових методів втручання. Саме такий інтегрований підхід розглядається в сучасній літературі як основа персоналізованого ведення пацієнтів з доброякісними меланоцитарними невусами шкіри [21, 36].
Перспективи індивідуалізованого підходу до лікування доброякісних меланоцитарних невусів шкіри
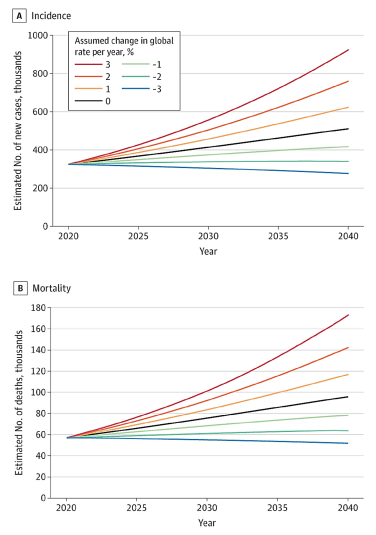
Актуальність удосконалення підходів до ведення меланоцитарних невусів посилюється глобальними онкоепідеміологічними трендами. За оцінками Всесвітньої організації охорони здоров’я, надмірна експозиція ультрафіолетового випромінювання у 2020 році була асоційована приблизно з 325 000 випадків меланоми шкіри та 57 000 смертей у світі [3]. Додатково, за даними Міжнародного агентства з вивчення раку (IARC), у 2022 році у світі було зареєстровано близько 331 700 нових випадків і 58 700 смертей від меланоми, причому понад 80% випадків були атрибутовані ультрафіолетовому опроміненню (267 тис. із 332 тис.) [4]. Хоча меланома не є безпосереднім об’єктом цього огляду, ці дані формують важливий контекст: точна оцінка пігментних утворень й обґрунтований вибір тактики щодо меланоцитарних невусів є складовою ширшої системи раннього виявлення та профілактики злоякісних новоутворень шкіри. Прогностичні розрахунки свідчать про суттєве зростання глобального тягаря меланоми в найближчі десятиліття. Очікується, що до 2040 року кількість уперше виявлених випадків цього захворювання може перевищити півмільйона, що відповідає приросту більше ніж на 50% порівняно з показниками 2020 року. Паралельно прогнозується істотне збільшення летальності: орієнтовна кількість смертей від меланоми може зрости майже на дві третини з приблизно 57 тис. у 2020 році до близько 96 тис. у 2040 році, за умови відсутності змін у поточних вікових показниках ризику. Важливо зазначити, що наведені прогнози базуються виключно на демографічних чинниках, зокрема зростанні чисельності населення та його старінні, і не враховують можливих змін у віковоспецифічній захворюваності на рівні окремих країн або регіонів. За таких умов лише стійке глобальне зниження показників захворюваності та смертності більше ніж на 2% могло б запобігти абсолютному зростанню кількості випадків меланоми у 2040 році (рис. 2) [1].
Незважаючи на стандартизацію дерматоскопічної «мови», реальна клінічна практика демонструє суттєву варіабельність у використанні термінології та існування різних «шкіл» опису. У консенсусі International Society of Dermoscopy щодо стандартизації термінології показано, що 23,5% фахівців переважно використовують описову термінологію, 20,1% – метафоричну, тоді як 56,5% комбінують обидві; при цьому значна частина нових термінів після попереднього консенсусу залишалася маловідомою для більшості учасників [31]. Це має прямі практичні наслідки: різне «кодування» однакових дерматоскопічних структур може призводити до різної оцінки ризику та, відповідно, до різних клінічних рішень щодо спостереження або вибору методу видалення.
З позицій доказової медицини дерматоскопія, порівняно з оглядом неозброєним оком, демонструє значно вищу діагностичну інформативність у клінічних умовах. У метааналізі Vestergaard et al. відносне діагностичне відношення шансів для виявлення меланоми при використанні дерматоскопії становило 15,6 (95% ДІ 2,9-83,7), а після корекції на викиди – 9,0 (95% ДІ 1,5-54,6) [32]. Для теми цього огляду принципово важливо, що ця перевага стосується саме підозрілих утворень тієї зони клінічної невизначеності, де виникає найбільше тактичних помилок при веденні меланоцитарних невусів.
Водночас ключова прогалина полягає в тому, що більшість дерматоскопічних алгоритмів розроблялися для виявлення меланоми, а не для прогнозування ризику неповного видалення або рецидиву доброякісних невусів. Навіть перший крок двокрокового алгоритму – класифікація «меланоцитарне/немеланоцитарне» – характеризується дуже високою чутливістю (97,1% в Австралії та 96,8% в Центральній Європі), але демонструє істотну варіабельність специфічності (33,6% і 67,9 % відповідно) [35]. Аналіз структури помилок показав, що наявність пігментної сітки в немеланоцитарних ураженнях зумовлювала хибну класифікацію у 25,2% випадків, а відсутність характерних ознак – у 25,6 % [35]. Це свідчить про те, що навіть високочутливий інструмент первинної ідентифікації не гарантує оптимального вибору лікувальної тактики без інтеграції з прогнозуванням морфологічної структури утворення.
Найбільш значущою практичною проблемою залишається неповне видалення меланоцитарних утворень і пов’язані з цим рецидиви або феномен зворотного невуса. У великому дослідженні Berglund et al. (2782 послідовні висічення) 9,7% меланоцитарних уражень були видалені неповно; серед факторів ризику виділялися локалізація в ділянці голови та шиї, а також організаційні й технічні чинники [6]. Це підтверджує системний характер проблеми: навіть за наміру радикального лікування в реальній практиці зберігається суттєва частка маргінальних резекцій, що створює передумови для рецидивів і повторних втручань.
Водночас частота клінічно помітного повернення невуса після часткового видалення може бути відносно низькою, але стабільно асоціюється саме з технікою shave. У дослідженні Goodson et al. рецидив був зафіксований у 3,6% диспластичних і 3,3% звичайних невусів, причому статистично значуща асоціація спостерігалася саме з shave-технікою, а не зі ступенем дисплазії чи позитивними краями резекції [33].
Порівняльні дослідження методів видалення також демонструють різницю не лише в косметичних результатах, а й у частоті рецидивів. У роботі Camini et al. рецидиви (11,7%) виникали виключно після shave-ексцизії, причому в 94,1% випадків уже на 3-місячному контролі; при цьому shave-метод асоціювався з частішим залученням латеральних і глибоких країв, тоді як еліптичне висічення формувало більші рубці [13].
Окрему групу доказів становлять дані щодо ведення диспластичних невусів з позитивними краями. У дослідженні Fleming et al. частота рецидиву в групі спостереження становила 3,3%, тоді як у групі реексцизії 0% при середній тривалості спостереження 5,5 року (p=0,02) [34]. Це підкреслює, що навіть відносно невелика частка рецидивів має накопичувальний клінічний ефект, оскільки кожна репігментація в рубці перетворюється на діагностичну подію з потенційною потребою повторного втручання.
У сукупності наведені дані свідчать, що ключова прогалина сучасної практики полягає не у відсутності дерматоскопічних алгоритмів як таких, а в нестачі валідованих дерматоскопічних критеріїв лікувального вибору, які б інтегрували прогнозовану морфологію і глибину невуса, анатомічну локалізацію, техніку видалення та ризик рецидиву або формування рубця в єдину практичну модель [6, 13, 31, 35]. Саме розробка й впровадження таких критеріїв дозволяє перейти від емпіричної тактики до прогнозованого, відтворюваного та персоналізованого підходу, що мінімізує повторні втручання та забезпечує оптимальний косметичний результат.
Доброякісні меланоцитарні невуси шкіри є біологічно та морфологічно гетерогенною групою новоутворень, що відображається в значній варіабельності їх клінічних проявів, дерматоскопічних патернів і результатів лікування. Отримані в ході цього огляду результати підтверджують положення класичної концепції поетапної міграції меланоцитів від дермо-епідермального з’єднання до дерми з подальшим клітинним дозріванням, яка лежить в основі поділу невусів на пограничні, комбіновані та інтрадермальні форми (Yélamos et al., 2019) [9], (Wang et al., 2022) [28].
Аналіз сучасних публікацій свідчить, що дерматоскопічні патерни мають чіткий морфологічний субстрат. Регулярна пігментна сітка найчастіше корелює з поверхневим розташуванням меланоцитарних гнізд у межах дермо-епідермального з’єднання, тоді як глобулярні та однорідні безструктурні патерни відповідають дермальному компоненту невуса (Errichetti, Stinco, 2016) [27], (Zalaudek et al., 2019) [32]. Ці спостереження узгоджуються з результатами порівняльних досліджень дерматоскопії та високочастотного ультразвуку, де було продемонстровано, що глибина залягання меланоцитарного компонента може бути частково прогнозована за допомогою дерматоскопічного аналізу (Wang et al., 2022) [28].
Практичне значення зазначених кореляцій полягає в можливості прогнозування ризику неповного видалення невуса при застосуванні часткових методів лікування. У клінічній практиці shave-ексцизія та інші косметичні методики широко використовуються з огляду на кращу короткострокову переносимість і менш виражене первинне рубцювання. Водночас результати порівняльних досліджень переконливо демонструють, що саме ці методи асоційовані з вищою частотою репігментації та розвитку феномену зворотного невуса (Camini et al., 2021) [19]. Аналогічні висновки отримали Goodson et al. (2010) [20], які показали, що клінічні рецидиви частіше виникають після shave-біопсії незалежно від ступеня дисплазії невуса.
Системний характер проблеми неповного видалення меланоцитарних утворень підтверджено у великому клініко-патологічному дослідженні Berglund et al. (2021) [6], де частота маргінальних або неповних резекцій становила близько 10% навіть за умови первинного наміру радикального втручання. Основними факторами ризику були анатомічна локалізація (ділянка голови та шиї) та технічні обмеження, пов’язані з прагненням мінімізувати косметичний дефект. Ці дані узгоджуються з результатами Rasner et al. (2023) [32], які описали розвиток зворотного невуса навіть у складних рубцевих структурах, що підкреслює важливість первинного вибору методу лікування.
Окремої уваги заслуговує проблема диференціації зворотного невуса та рецидиву меланоми в зоні рубця. За даними Heck et al. (2019) [8], дерматоскопічні ознаки репігментації після неповного видалення можуть включати асиметрію, нерівномірні глобули та сіро-коричневі безструктурні зони, що морфологічно відповідає залишковій або реактивній меланоцитарній проліферації. Navarrete-Dechent et al. (2020) [18] додатково продемонстрували, що вирішальним диференційно-діагностичним критерієм між зворотним невусом і рецидивом меланоми є поширення пігментації за межі рубця, тоді як ізольована репігментація в його межах частіше має доброякісний характер.
Водночас дані щодо ведення диспластичних невусів з позитивними краями резекції залишаються неоднозначними. Fleming et al. (2016) [21] та Engeln et al. (2017) [22] повідомляють про відносно низьку частоту клінічних рецидивів у разі динамічного спостереження без негайної реексцизії. Водночас Fleming et al. (2020) [23] показали, що повторне хірургічне висічення практично повністю усуває ризик рецидиву, що має особливе значення в умовах діагностичної невизначеності або за відсутності повного первинного гістологічного висновку. Розбіжності між результатами досліджень можуть бути зумовлені різними критеріями відбору пацієнтів, тривалістю спостереження та методологічними підходами до оцінювання рецидивів.
З позицій доказової медицини дерматоскопія демонструє суттєву перевагу порівняно з оглядом неозброєним оком у діагностиці меланоцитарних утворень. Метааналізи підтверджують її високу чутливість і специфічність у клінічних умовах (Vestergaard et al., 2008) [16], (Dinnes et al., 2018) [17]. Проте більшість дерматоскопічних алгоритмів, зокрема ABCD-правило, 7-пунктовий чек-листок та двоетапний підхід, були розроблені передусім для виявлення меланоми, а не для прогнозування ризику неповного видалення доброякісних невусів (Kittler et al., 2016) [40], (Tschandl et al., 2019) [33].
Таким чином, отримані результати та дані сучасної літератури свідчать, що ефективне ведення пацієнтів з доброякісними меланоцитарними невусами потребує переходу від емпіричного вибору методу лікування до алгоритмізованої, індивідуалізованої моделі. Така модель повинна інтегрувати клінічні характеристики, дерматоскопічні патерни, прогнозовану морфологічну структуру невуса, анатомічну локалізацію та анамнестичні дані. Саме комплексний підхід дозволяє знизити ризик розвитку зворотного невуса, мінімізувати діагностичні помилки та досягти оптимального довгострокового косметичного результату.
ВИСНОВКИ
1. Аналіз сучасної літератури свідчить, що доброякісні меланоцитарні невуси шкіри є надзвичайно поширеною патологією, а їх клінічне значення виходить за межі суто косметичної проблеми. З огляду на глобальні епідеміологічні тенденції меланоми та доведену роль ультрафіолетового опромінення, підвищення точності діагностики пігментних утворень й обґрунтованості лікувальної тактики щодо невусів має важливе профілактичне значення.
2. Дерматоскопія є високоефективним неінвазивним методом оцінювання меланоцитарних утворень, що достовірно перевершує огляд неозброєним оком за діагностичною інформативністю. Водночас більшість наявних дерматоскопічних алгоритмів і чек-листків розроблені переважно для виявлення меланоми та недостатньо адаптовані для прогнозування морфологічної структури доброякісних невусів і вибору оптимального методу їх лікування.
3. Дані клінічних і патоморфологічних досліджень переконливо демонструють, що ризик неповного видалення меланоцитарних утворень залишається суттєвим і може досягати близько 10% навіть у сучасній клінічній практиці, особливо при локалізації в ділянці голови та шиї. Часткові методи видалення, зокрема shave-ексцизія, асоціюються з вищою частотою репігментації та розвитку зворотного невуса, що в різних дослідженнях коливається від 3% до понад 20% залежно від морфологічного типу утворення, локалізації та термінів спостереження.
4. Зворотний (recurrent) невус становить не лише косметичну, а й серйозну діагностичну проблему, оскільки його клінічні та дерматоскопічні прояви можуть імітувати рецидив меланоми. Найбільш значущими диференційними ознаками визнано обмеження пігментації межами рубця, час появи репігментації та облік віку пацієнта і первинної гістологічної верифікації, відсутність якої суттєво ускладнює подальше клінічне рішення.
5. Наявні дані свідчать, що клініко-морфологічна форма невуса, його дерматоскопічний патерн, анатомічна локалізація та обраний метод лікування перебувають у тісному взаємозв’язку та визначають як ризик рецидиву, так і довгостроковий косметичний результат. Ігнорування морфологічного контексту при виборі методу втручання підвищує ймовірність повторних процедур і формування косметично несприятливих рубців.
6. Таким чином, сучасний стан проблеми свідчить про необхідність переходу від емпіричного та уніфікованого підходу до лікування меланоцитарних невусів до індивідуалізованої моделі, заснованої на інтеграції клінічних, дерматоскопічних і патоморфологічних даних. Розробка та впровадження валідованих дерматоскопічних критеріїв диференційної діагностики й вибору методу лікування має потенціал знизити частоту зворотного невуса, мінімізувати післяопераційні ускладнення та забезпечити прогнозований косметичний результат, що визначає перспективність подальших досліджень у цьому напрямку.
Внески авторів:
Торбенко Є.Л. – концептуалізація, дослідження, написання – початковий проєкт, написання – рецензування та редагування;
Літус В.І. – методологія, дослідження, написання – початковий проєкт, написання – рецензування та редагування, дослідження, формальний аналіз.
Фінансування. Роботу виконано за рахунок власних коштів дослідників, а також за підтримки наукової діяльності здобувачів Національного університету охорони здоров’я України ім. П.Л. Шупика.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів.
REFERENCES
1. Arnold M, Singh D, Laversanne M, Vignat J, Vaccarella S, Meheus F, et al. Global burden of cutaneous melanoma in 2020 and projections to 2040. JAMA Dermatol. 2022;158(5):495-503. doi: https://doi.org/10.1001/jamadermatol.2022.0160
2. Whiteman DC, Green AC, Olsen CM. The growing burden of invasive melanoma: projections of incidence rates and numbers of new cases in six susceptible populations to 2031. J Invest Dermatol. 2016;136(6):1161-71. doi: https://doi.org/10.1016/j.jid.2016.01.035
3. International Agency for Research on Cancer (IARC). Global Cancer Observatory: Melanoma of skin [Internet]. Lyon: IARC; 2022 [cited 2025 Dec 15]. Available from: https://gco.iarc.fr/
4. World Health Organization. Ultraviolet radiation [Internet]. Geneva: WHO; 2020 [cited 2025 Dec 15]. Available from:
https://www.who.int/health-topics/ultraviolet-radiation
5. WHO Classification of Tumours Editorial Board. Skin Tumours. WHO Classification of Tumours [Internet]. 5th ed. Vol 12. Lyon: IARC; 2025 [cited 2025 Dec 15]. Available from: https://publications.iarc.who.int/Book-And-Report-Series/Who-Classification-Of-Tumours/Skin-Tumours-2025
6. Berglund S, Johansson Backman E, Baldawi Z, Horn L, Arbin Borsiin R, Marjanovic M, et al. Incomplete excisions of melanocytic lesions: rates and risk factors. Acta Derm Venereol. 2021;101(3):adv00421. doi: https://doi.org/10.2340/00015555-3784
7. Castagna RD, Stramari JM, Chemello RML. The recurrent nevus phenomenon. An Bras Dermatol. 2017;92(4):531-3.
doi: https://doi.org/10.1590/abd1806-4841.20176190
8. Heck R, Ferrari T, Cartell A, Bakos RM. Clinical and dermoscopic (in vivo and ex vivo) predictors of recurrent nevi. Eur J Dermatol. 2019;29(2):179-84. doi: https://doi.org/10.1684/ejd.2019.3530
9. Yélamos O, Braun RP, Liopyris K, Wolner ZJ, Kerl K, Gerami P, et al. Dermoscopy and dermatopathology correlates of cutaneous neoplasms. J Am Acad Dermatol. 2019;80(2):341-63. doi: https://doi.org/10.1016/j.jaad.2018.07.073
10. Kittler H, Marghoob AA, Argenziano G, Carrera C, Curiel-Lewandrowski C, Hofmann-Wellenhof R, et al. Standardization of terminology in dermoscopy/ dermatoscopy: results of the third consensus conference of the International Society of Dermoscopy. J Am Acad Dermatol. 2016;74(6):1093-106. doi: https://doi.org/10.1016/j.jaad.2015.12.038
11. Nachbar F, Stolz W, Merkle T, Cognetta AB, Vogt T, Landthaler M, et al. The ABCD rule of dermatoscopy: high prospective value in the diagnosis of doubtful melanocytic skin lesions. J Am Acad Dermatol. 1994;30(4):551-9.
doi: https://doi.org/10.1016/S0190-9622(94)70061-3
12. Annessi G, Bono R, Sampogna F, Faraggiana T, Abeni D. Sensitivity, specificity, and diagnostic accuracy of three dermoscopic algorithmic methods in the diagnosis of doubtful melanocytic lesions. J Am Acad Dermatol. 2007;56(5):759-67. doi: https://doi.org/10.1016/j.jaad.2007.01.035
13. Argenziano G, Fabbrocini G, Carli P, De Giorgi V, Sammarco E, Delfino M. Epiluminescence microscopy for the diagnosis of doubtful melanocytic skin lesions: comparison of the ABCD rule of dermatoscopy and a new 7-point checklist. Br J Dermatol. 1998;139(6):1113-9. doi: https://doi.org/10.1046/j.1365-2133.1998.02506.x
14. Argenziano G, Zalaudek I, Corona R, Sera F, Cicale L, Petrillo G, et al. Seven-point checklist of dermoscopy revisited. Br J Dermatol. 2011;164(4):785-90. doi: https://doi.org/10.1111/j.1365-2133.2010.10194.x
15. Soyer HP, Argenziano G, Chimenti S, Ruocco V. Three-point checklist of dermoscopy: a new screening method for early detection of melanoma. Dermatology. 2004;208(1):27-31. doi: https://doi.org/10.1159/000075042
16. Vestergaard ME, Macaskill P, Holt PE, Menzies SW. Dermoscopy compared with naked eye examination for the diagnosis of primary melanoma: a meta-analysis of studies performed in a clinical setting. Br J Dermatol. 2008;159(3):669-76. doi: https://doi.org/10.1111/j.1365-2133.2008.08713.x
17. Dinnes J, Deeks JJ, Chuchu N, Ferrante di Ruffano L, Matin RN, Thomson DR, et al. Dermoscopy, with and without visual inspection, for diagnosing melanoma in adults. Cochrane Database Syst Rev. 2018;12(12):CD011902. doi: https://doi.org/10.1002/14651858.CD011902.pub2
18. Navarrete-Dechent C, Cordova M, Liopyris K, Rishpon A, Aleissa S, Rossi AM, et al. Reflectance confocal microscopy and dermoscopy aid in evaluating repigmentation within or adjacent to lentigo maligna melanoma surgical scars. J Eur Acad Dermatol Venereol. 2020;34(1):74-81. doi: https://doi.org/10.1111/jdv.15819
19. Camini L, Manzoni APD, Weber MB, Luzzatto L, Soares AS, Bonamigo RR. Shave excision versus elliptical excision of nonpigmented intradermal melanocytic nevi: comparative assessment of recurrence and cosmetic outcomes. Dermatol Surg. 2021;47(2):e21-e25. doi: https://doi.org/10.1097/DSS.0000000000002666
20. Goodson AG, Florell SR, Boucher KM, Grossman D. Low rates of clinical recurrence following biopsy of benign to moderately atypical dysplastic melanocytic nevi. J Am Acad Dermatol. 2010;62(4):591-6. doi: https://doi.org/10.1016/j.jaad.2009.06.044
21. Fleming NH, Egbert BM, Kim J, Swetter SM. Reexamining the threshold for reexcision of histologically transected dysplastic nevi. JAMA Dermatol. 2016;152(12):1327-34. doi: https://doi.org/10.1001/jamadermatol.2016.2869
22. Engeln K, Peters K, Ho J, Jedrych J, Winger D, Ferris LK, et al. Dysplastic nevi with severe atypia: long-term outcomes in patients with and without re-excision. J Am Acad Dermatol. 2017;76(2):244-9. doi: https://doi.org/10.1016/j.jaad.2016.08.054
23. Fleming NH, Shaub AR, Bailey E, Swetter SM. Outcomes of surgical re-excision versus observation of severely dysplastic nevi: a single-institution retrospective cohort study. J Am Acad Dermatol. 2020;82(1):238-40. doi: https://doi.org/10.1016/j.jaad.2019.07.033
24. Pampena R, Kyrgidis A, Lallas A, Moscarella E, Argenziano G, Longo C. A meta-analysis of nevus-associated melanoma: prevalence and practical implications. J Am Acad Dermatol. 2017;77(5):938-945.e4. doi: https://doi.org/10.1016/j.jaad.2017.06.149
25. Dessinioti C, Befon A, Stratigos AJ. The association of nevus-associated melanoma with common or dysplastic melanocytic nevus: systematic review and meta-analysis. Cancers (Basel). 2023;15(3):856. doi: https://doi.org/10.3390/cancers15030856
26. Kaiser I, Pfahlberg AB, Uter W, Heppt MV, Veierød MB, Gefeller O. Risk prediction models for melanoma: systematic review on heterogeneity in model development and validation. Int J Environ Res Public Health. 2020;17(21):7919. doi: https://doi.org/10.3390/ijerph17217919
27. Errichetti E, Stinco G. Dermoscopy in general dermatology: a practical overview. Dermatol Ther (Heidelb). 2016;6(4):471-507. doi: https://doi.org/10.1007/s13555-016-0141-6
28. Wang YK, Gao YJ, Liu J, Zhu QL, Wang JC, Qin J, et al. Comparative study of melanocytic nevi classification with dermoscopy and high-frequency ultrasound. Skin Res Technol. 2022;28(2):265-73. doi: https://doi.org/10.1111/srt.13123
29. Garbe C, Amaral T, Peris K, Hauschild A, Arenberger P, Basset-Seguin N, et al. European consensus-based interdisciplinary guideline for melanoma. Part 1: diagnostics update 2022. Eur J Cancer. 2022;170:236-55. doi: https://doi.org/10.1016/j.ejca.2022.03.008
30. Garbe C, Peris K, Hauschild A, Amaral T, Arenberger P, Bastholt L, et al. European consensus-based interdisciplinary guideline for melanoma. Part 2: treatment update 2022. Eur J Cancer. 2022;170:256-84. doi: https://doi.org/10.1016/j.ejca.2022.04.018
31. Aubert H, Pere M, Bellier-Waast F, Perrot P, Barbarot S; Groupe de Recherche en Dermatologie Pédiatrique. Management of congenital melanocytic naevi in children: a French national survey. Acta Derm Venereol. 2020;100(19):adv00341. doi: https://doi.org/10.2340/00015555-3695
32. Rasner CJ, Zhou Y, Giubellino A. Recurrent nevus phenomenon developing within a keloid. Dermatopathology (Basel). 2023;10(3):201-6. doi: https://doi.org/10.3390/dermatopathology10030028
33. Cappilli S, Ribero S, Cornacchia L, Catapano S, Del Regno L, Quattrini L, et al. Melanocytic lesions with peripheral globules: proposal of an integrated management algorithm. Dermatol Pract Concept. 2023;13(1):e2023010. doi: https://doi.org/10.5826/dpc.1301a10
34. Jayasinghe D, Naranpanawa N, Ashley DP, Ingvar Å, Betz-Stablein B, Soyer HP, et al. Systematic review of nevus counting and reporting methodologies in contemporary studies of the general population. Dermatol Pract Concept. 2024;14(4):e2024223. doi: https://doi.org/10.5826/dpc.1404a223
35. Posada MIM, Gutiérrez Gómez M, Vásquez-Trespalacios EM, Garces Abad MA, Londoño García AM, González Álvarez T. Dermoscopic changes in melanocytic lesions during 5-year digital follow-up in patients with atypical nevus syndrome. Actas Dermosifiliogr. 2024;115(2):e1-e8. doi: https://doi.org/oi:10.1016/j.ad.2023.11.018
36. Mihulecea CRJ, Frățilă S, Rotaru M. Clinical-dermoscopic similarities between atypical nevi and early stage melanoma. Exp Ther Med. 2021;22(2):854. doi: https://doi.org/10.3892/etm.2021.10286
37. Gonzalez Matheus G, Robins CP, Muir J. Guide to shave procedures in general practice. Aust J Gen Pract. 2024;53(6):398-402.
doi: https://doi.org/10.31128/AJGP-06-23-6872
38. Guo Z, Ge L, Li Y, Gu Y, Wang W, Wei C, et al. History and prospect of melanocytic nevus treatment. J Dermatol Treat. 2023;34(1):2170010. doi: https://doi.org/10.1080/09546634.2022.2170010
39. Okada MAMU, Heck R, Marchiori Bakos R. Histological and immunohistochemical findings in recurrent melanocytic nevus. An Bras Dermatol. 2025;100(6):e501241. doi: https://doi.org/10.1016/j.abd.2025.501241
40. Kittler H, Rosendahl C, Cameron A, Tschandl P. Dermatoscopy: An algorithmic method based on pattern analysis. 2nd ed. Vienna: Facultas; 2016. 394 p.
41. Lorentzen H, Weismann K, Kenet RO, Secher L, Larsen FG. The dermatoscopic ABCD rule does not improve diagnostic accuracy of malignant melanoma. Acta Derm Venereol. 1999;79(6):469-72. doi: https://doi.org/10.1080/000155599750010256
42. Zalaudek I, Argenziano G, Soyer HP, Corona R, Sera F, Blum A, et al. Three-point checklist of dermoscopy: an open internet study. Br J Dermatol. 2006;154(3):431-7.
doi: https://doi.org/10.1111/j.1365-2133.2005.06983.x
43. Kittler H, Pehamberger H, Wolff K, Binder M. Diagnostic accuracy of dermoscopy. Lancet Oncol. 2002;3(3):159-65. doi: https://doi.org/10.1016/S1470-2045(02)00679-4
44. Rosendahl C, Cameron A, McColl I, Wilkinson D. Dermatoscopy in routine practice - 'chaos and clues'. [Internet]. Aust Fam Physician. 2012 [cited 2025 Dec 15];41(7):482-7. Available from: https://www.racgp.org.au/afp/2012/july/dermatoscopy-in-routine-practice
45. Tschandl P, Rinner C, Apalla Z, Argenziano G, Codella N, Halpern A, et al. Human-computer collaboration for skin cancer recognition. Nat Med. 2020;26(8):1229-34. doi: https://doi.org/10.1038/s41591-020-0942-0
46. Dinnes J, Deeks JJ, Saleh D, Chuchu N, Bayliss SE, Patel L, et al. Reflectance confocal microscopy for diagnosing cutaneous melanoma in adults. Cochrane Database Syst Rev. 2018;12(12):CD013190. doi: https://doi.org/10.1002/14651858.CD013190
47. Dinnes J, Deeks JJ, Grainge MJ, Chuchu N, Ferrante di Ruffano L, Matin RN, et al. Visual inspection for diagnosing cutaneous melanoma in adults. Cochrane Database Syst Rev. 2018;12(12):CD013194. doi: https://doi.org/10.1002/14651858.CD013194
48. Walsh T, Macey R, Riley P, Glenny AM, Schwendicke F, Worthington HV, et al. Imaging modalities to inform the detection and diagnosis of early caries. Cochrane Database Syst Rev. 2021;3(3):CD014545. doi: https://doi.org/10.1002/14651858.CD014545
49. Hryshchenko RV, Bohomolets OV, Stepanenko VI. [Benign and malignant (melanocytic and non-melanocytic) skin neoplasms: classification, clinical features, diagnostics, treatment strategy]. Ukrainskyi zhurnal dermatolohii, venerolohii, kosmetolohii. 2023;4:20-7. Ukrainian. doi: https://doi.org/10.30978/UJDVK2023-4-20
50. Rosendahl C, Voloshynovych MS, Hirnyk HYe, et al. [Algorithmic method of dermoscopic image analysis “Prediction without pigment” and its implementation in clinical practice]. Ukrainskyi zhurnal dermatolohii, venerolohii, kosmetolohii. 2020;3:62-68. Ukrainian. doi: https://doi.org/10.30978/UJDVK2020-3-62
51. Teledermatoscopy Study Group. [Comparative characteristics of dermoscopy and teledermoscopy in the diagnosis of pigmented skin lesions]. Ukrainskyi zhurnal dermatolohii, venerolohii, kosmetolohii. 2018;1:17-22. Ukrainian. doi: https://doi.org/10.30978/UJDVK2018-1-17
52. Makurina HI, Cherneda LO. [Algorithm for the use of a topical oxidizing agent in the treatment of seborrheic keratosis based on ultrasound and pathomorphological characteristics]. Ukrainskyi zhurnal dermatolohii, venerolohii, kosmetolohii. 2022;1-2(84-85):41-46. Ukrainian. doi: https://doi.org/10.30978/UJDVK2022-1-2-41
53. Hortynska OM. [Combined therapy of patients with skin neoplasms: clinical material and algorithmic approach]. Ukrainskyi zhurnal dermatolohii, venerolohii, kosmetolohii. 2022;1-2(84-85):22-28. Ukrainian. doi: https://doi.org/10.30978/UJDVK2022-1-2-22
54. Voloshynovych MS, et al. [Skin melanoma: from almost invisible to visually indisputable. Some principles of guidance and clinical cases review]. Ukrainskyi medychnyi chasopys. 2020;3(137):45-52. Ukrainian. doi: https://doi.org/10.32471/umj.1680-3051.137.179285


 UK
UK  EN
EN